Forskere udvikler nanostrukturer for at forbedre immunsystemets evne til at bekæmpe kræft
I løbet af det sidste årti har forskere søgt mere effektive og varige kræftbehandlinger. Blandt de mange forskellige immunterapier er Stimulator of Interfron Genes activation (STING-agonisme) dukket op som en særlig lovende tilgang, der udnytter en patients immunsystem til at bekæmpe tumorer i hele kroppen.
Selvom det er potentielt revolutionerende, er der stadig kritiske hindringer, der skal overvindes, før STING-agonisme kan anvendes som behandlingsmulighed for patienter. For eksempel er intravenøs administration af STING-agonistlægemidler ofte ikke effektiv på grund af manglende lægemiddelstabilitet og dårlig optagelse af immunceller.
For at løse disse udfordringer direkte har efterforskere ved Brigham and Women's Hospital, et stiftende medlem af Mass General Brigham sundhedsvæsen, nu designet stimuli-responsive nanopartikelstrukturer, hvilket gør det muligt at frigive STING-agonistlægemidler, når de når målcellerne. I et papir offentliggjort i dag i Nature Nanotechnology , rapporterer forskerne, at stabiliserede nanoformuleringer ikke kun udryddede aktive tumorer i mus, men også trænede deres immunsystem til at genkende og eliminere fremtidige tumorer.
"Vores mål er at bruge STING-agonisme til at instruere immunsystemet til at behandle kræftceller som angribere, hvilket nødvendiggør design af stabile og potente nanostrukturer, der gør det muligt for STING at nå de rigtige organer og de rigtige celler," siger seniorforfatter Natalie Artzi, Ph. .D., en hovedefterforsker i Brigham's Department of Medicine.
Hovedforfatter Pere Dosta Pons, Ph.D., en instruktør i Brigham's Department of Medicine, fremhævede nyheden i deres tilgang:"Vi træner ikke kun immunsystemet til at målrette og eliminere kræftceller, men også til at generere immunhukommelse for forebyggelse af tilbagefald af kræft."
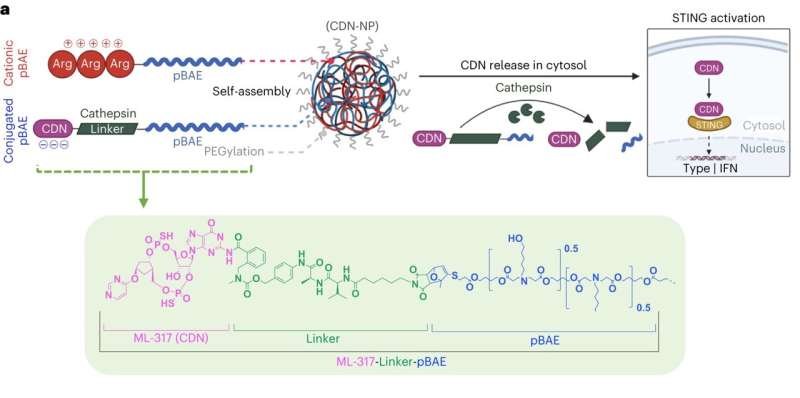
STING-agonisme involverer aktiveringen af et protein kaldet stimulatoren af interferon-gener (STING), som advarer immunsystemet om tilstedeværelsen af angribere. Når kroppen er inficeret af en virus eller en bakterieart, binder små budbringermolekyler kendt som cytosoliske cykliske dinukleotider (CDN) sig til STING. Denne aktivering foranlediger produktionen af proinflammatoriske cytokiner, som igen aktiverer immunceller såsom naturlige dræberceller, makrofager og T-celler, og rekrutterer dem til det berørte område for at fjerne infektionen.
Kræft unddrager sig denne STING-vej ved at forklæde sig som kroppens egne celler. Forskere har forsøgt at lære immunsystemet at identificere og angribe cancerceller ved at levere STING-agonister til immunceller i tumormikromiljøerne og tumordrænende lymfeknuder.
I deres nye papir beskriver Brigham-teamet en ny nanopartikelstruktur, der mere effektivt transporterer CDN-molekyler ind i immunceller. Denne struktur forbinder direkte laboratorieproducerede CDN'er til nanopartikler lavet af poly(beta-aminoestere) eller pBAE'er, hvilket gør forbindelsen mere stabil og potent, når den injiceres i kroppen, og derved forbedrer dens terapeutiske vindue. Nanostrukturen taxerer CDN-budbringerne direkte til tumorer og løsner kun lasten, når den når målcellerne.
For at evaluere effektiviteten af deres tilgang administrerede holdet CDN-nanopartikelforbindelserne (CDN-NP) til mus med melanom, tyktarmskræft og brystkræfttumorer. De bekræftede, at deres CDN-nanostrukturer blev optaget af målimmunceller i tumormikromiljøet og i sekundære lymfoide organer, hvilket giver mus langsigtet immunitet mod fremtidige tumorer. Når overlevende mus blev genindført med tumorer 60 dage efter deres første behandling, var de i stand til at afvise tumorerne på egen hånd.
Holdet udviklede et sæt designregler, der skal tages i betragtning ved levering af immunterapi, herunder hvilken rolle sekundære lymfoide organer spiller i at diktere terapeutiske resultater. De viste, at milten spiller en afgørende rolle i coaching af immunsystemet til at generere immunhukommelse.
Ud over at tage fat på grundlæggende spørgsmål om kræft og immunologi, viser undersøgelser som denne potentialet i at forbedre genterapi-leveringssystemer til behandling af sygdomme som kræft.
Ved at forklare betydningen af arbejdet sagde Artzi:"Vores forskning adresserer det grundlæggende samspil mellem immunsystemet og kræft gennem brugen af en ny struktur, der er designet til at være både stabil og potent. Desuden har vi vist, at målretning af sekundær lymfoid organer, såsom milten, er afgørende for at generere langvarig antitumorrespons, som har vigtige konsekvenser for, hvordan vi tænker på levering af immunterapi."
Flere oplysninger: Pere Dosta et al., Undersøgelse af den øgede antitumorstyrke af STING-agonist efter konjugation til polymernanopartikler, Nature Nanotechnology (2023). DOI:10.1038/s41565-023-01447-7
Journaloplysninger: Naturenanoteknologi
Leveret af Brigham and Women's Hospital
 Varme artikler
Varme artikler
-
 Det tætteste udvalg af kulstof nanorør, der er dyrket til datoScanningselektronmikroskopbilleder er af CNT-skove med lav og høj tæthed. Kredit:Hisashi Sugime/U.Cambridge Carbon nanorørs fremragende mekaniske, elektriske og termiske egenskaber gør dem til et
Det tætteste udvalg af kulstof nanorør, der er dyrket til datoScanningselektronmikroskopbilleder er af CNT-skove med lav og høj tæthed. Kredit:Hisashi Sugime/U.Cambridge Carbon nanorørs fremragende mekaniske, elektriske og termiske egenskaber gør dem til et -
 Nanoskala velcro brugt til molekyletransportImportér proteinovertrukket molekyle, der bevæger sig på den beskidte velcro. Kredit:Universitetet i Basel Biologiske membraner er som en bevogtet grænse. De adskiller cellen fra miljøet og kontro
Nanoskala velcro brugt til molekyletransportImportér proteinovertrukket molekyle, der bevæger sig på den beskidte velcro. Kredit:Universitetet i Basel Biologiske membraner er som en bevogtet grænse. De adskiller cellen fra miljøet og kontro -
 Nanoserede diamanter muliggør fremskridt i nethindeproteserForskningsgrupper i flere lande gør fremskridt inden for udvikling af nethindeproteser. Hvis de når deres mål, patienter, der er blevet blinde, på grund af tab af deres fotoreceptorer, kunne genvinde
Nanoserede diamanter muliggør fremskridt i nethindeproteserForskningsgrupper i flere lande gør fremskridt inden for udvikling af nethindeproteser. Hvis de når deres mål, patienter, der er blevet blinde, på grund af tab af deres fotoreceptorer, kunne genvinde -
 Forskere skaber kunstig virus i kampen mod superbugsKredit:CC0 Public Domain Forskere ved NPL, arbejder med partnere fra University of Cambridge, University of Exeter, Kings College London og University College London har udviklet en mekanisme for
Forskere skaber kunstig virus i kampen mod superbugsKredit:CC0 Public Domain Forskere ved NPL, arbejder med partnere fra University of Cambridge, University of Exeter, Kings College London og University College London har udviklet en mekanisme for
- Sådan læses Zener Diode Ratings
- Hvordan en nuklear nedsmeltning fungerer
- Forskere foretager første detaljerede målinger af nøglefaktorer relateret til høj temperatur sup…
- Ishavet kan have været dækket af en ishylde, der er næsten dobbelt så stor som Grønlands indlan…
- Sundhedseffekten af luftforurening fra trafik
- Ny forskning tyder på, at websteder med pensionsrådgivning skaber skævhed


