Den tætteste ikke-aminoglykosidligand til det bakterielle ribosomale RNA A-sted
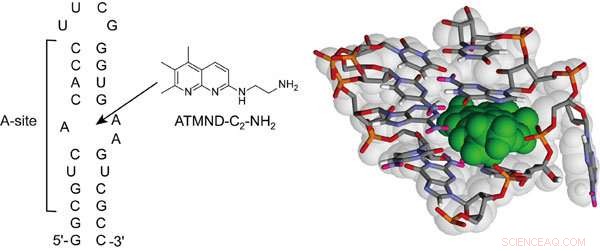
Kemisk struktur af ATMND-C 2 -NH 2 og sekvensen af den bakterielle (Escherichia coli) A-sted-holdige RNA-model anvendt i denne undersøgelse. Det viser også den mulige struktur af komplekset mellem ATMND-C 2 -NH 2 (grøn farve) og intern løkke af A-stedet. Kredit:Seiichi Nishizawa
En forskergruppe ved Tohoku University har gjort en betydelig opdagelse med positive konsekvenser for udviklingen af bakteriebekæmpende medicin. Aminoacyl-tRNA-stedet (A-stedet) i 16S RNA-afkodningsområdet i det bakterielle ribosom ser lovende ud for en ny æra med udvikling af antibiotika-lægemidler.
Traditionelle aminoglykosid-antibiotika er problematiske på grund af deres høje toksicitet og potentiale for resistensudvikling. Forskningen ved Tohoku University fokuserede på bakteriel A-site, der binder små ligander, hvis strukturer er forskellige fra aminoglycosidfamilien, som tilbyder potentiale for udvikling af nye lægemidler, der behandler bakterielle infektioner med en reduktion af problemerne forbundet med traditionelle antibiotika.
Forskergruppen ledet af Dr. Seiichi Nishizawa og Dr. Yusuke Sato (Kemisk Institut, Graduate School of Science) har rapporteret en ny lille ligand, ATMND-C 2 -NH 2 som har den strammeste bindingsaffinitet til det bakterielle A-sted blandt ikke-aminoglycosid-ligander.
ATMND-C 2 -NH 2 viser en signifikant fluorescerende quenching-respons ved selektiv binding til den indre sløjfe af det bakterielle (Escherichia coli) A-sted-holdige model-RNA.
ATMND-C 2 -NH 2 har også vist sig nyttig som en indikator til vurdering af ligand/A-sted interaktioner.
Resultaterne opnået af forskergruppen giver et rationelt grundlag for generering af nye A-site bindingsligander med henblik på nye antibiotika med mindre toksicitet og minimal resistensudvikling.
Sidste artikelModifikation af aminosyrer giver nyt udgangspunkt for udvikling af medicinske behandlinger
Næste artikelMedicin du kan bære
 Varme artikler
Varme artikler
-
 Nogle kan lide det kryogentGengivelse af First Element Fuels flydende brintstofpumpe til detailhandel. Pumpen indeholder en baldakin på toppen, og brændstoflageret er afbildet på bagsiden. Kredit:First Element Fuel Sandia N
Nogle kan lide det kryogentGengivelse af First Element Fuels flydende brintstofpumpe til detailhandel. Pumpen indeholder en baldakin på toppen, og brændstoflageret er afbildet på bagsiden. Kredit:First Element Fuel Sandia N -
 Nye nanoporøse metalskum bruger sollys til at rense vandKredit:University of Bath En forsker fra University of Bath går forrest i at skabe et nyt, mere effektiv måde for vandindustrien til sikkert at fjerne mikropollutanter fra vand uden at øge deres C
Nye nanoporøse metalskum bruger sollys til at rense vandKredit:University of Bath En forsker fra University of Bath går forrest i at skabe et nyt, mere effektiv måde for vandindustrien til sikkert at fjerne mikropollutanter fra vand uden at øge deres C -
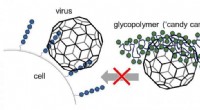 Kunstige slikstokke til at blokere viraDe kunstigt fremstillede glycomimetika (grønne) binder sig til viras bindingssteder, som vira normalt bruger til at binde til sukkerarter (blå) på celleoverfladen. Kredit:L. Hartmann, M. Schelhaas
Kunstige slikstokke til at blokere viraDe kunstigt fremstillede glycomimetika (grønne) binder sig til viras bindingssteder, som vira normalt bruger til at binde til sukkerarter (blå) på celleoverfladen. Kredit:L. Hartmann, M. Schelhaas -
 En billig organisk dampgenerator til at rense vandVarmen fra solen fordamper vandet, mens salt og andre materialer forbliver tilbage. Kredit:Thor Balkhed Det er blevet anslået, at en fjerdedel af verdens børn i 2040 vil bo i regioner, hvor der ma
En billig organisk dampgenerator til at rense vandVarmen fra solen fordamper vandet, mens salt og andre materialer forbliver tilbage. Kredit:Thor Balkhed Det er blevet anslået, at en fjerdedel af verdens børn i 2040 vil bo i regioner, hvor der ma
- Fysikere løser det mangeårige mysterium om strukturløs overgang
- Ny type metasurface tillader hidtil uset laserkontrol
- Forskerteam bøjer individuelle tetrapod -nanostrukturer
- Ekstremt vejr kan bare tilskynde os til at tage os sammen om den globale opvarmning
- Livet efter kul:Nedgangen og opblomstringen af kullandet i West Virginia
- 2019 subsidier til fossile brændstoffer næsten 500 mia. USD:OECD/IEA


