En biobank af reversible mutante embryonale stamceller
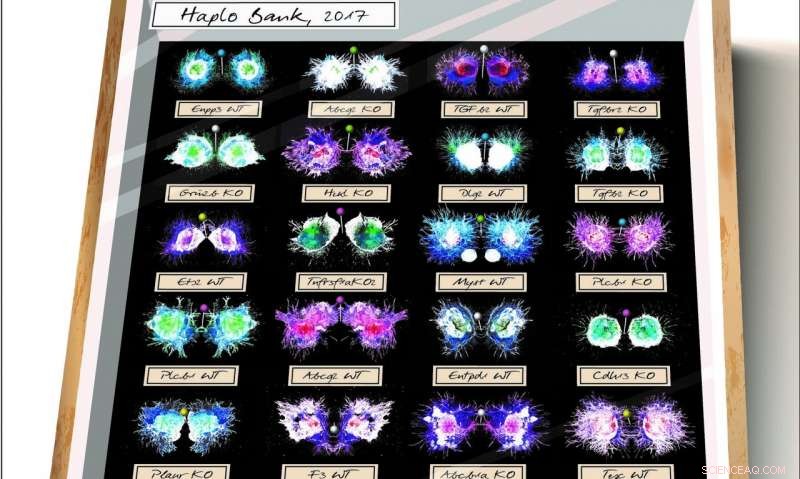
Haplobank indeholder over 100, 000 muterede, betingede mus embryonale stamcellelinjer, målrettet mod omkring 70% af det proteinkodende genom. Kredit:IzabellaKaminski
Videnskabsmand ved IMBA udviklede en biobank med revertible, mutante embryonale stamceller, udgivet i det aktuelle nummer af Natur . Denne cellebank - kaldet Haplobank - indeholder over 100, 000 muterede, betingede mus embryonale stamcellelinjer, målrettet mod omkring 70 procent af det proteinkodende genom.
Genetiske skærme har revolutioneret vores forståelse af biologiske processer og sygdomsmekanismer. Nylige tekniske fremskridt har udvidet de tilgængelige metoder til afbrydelse af genfunktion i en cellepopulation inden screening, fra kemisk og indsættende mutagenese til RNA -interferens, og, seneste, CRISPR-medieret genomredigering. Imidlertid, RNA-interferens og CRISPR-medieret genmålretning lider ofte af dårlig effektivitet og off-target effekter. Ud over, de fleste mutagenesetilgange er ikke reversible - hvilket gør det vanskeligt nøje at kontrollere de hyppige genetiske og epigenetiske forskelle mellem tilsyneladende identiske celler. Disse spørgsmål kan forvirre reproducerbarheden, fortolkning og generel succes af genetiske skærme.
Store bekymringer om videnskabelig reproducerbarhed og stringens er dukket op i de seneste år. Amgen og Bayer, samt reproducerbarhedsinitiativet, har været ude af stand til at replikere mange højt profilerede kræftundersøgelser. Ja, det er ikke ualmindeligt at opnå forskellige resultater fra forsøg med den samme cellelinje i to forskellige laboratorier. Disse uoverensstemmelser kan opstå af forskellige årsager. Uanset, ureproducerbare resultater spilder penge, skade videnskabens og forskernes troværdighed, og forsinke eller fortryde fremskridt, herunder udvikling af effektive terapier.
For at overvinde disse problemer, Penninger -laboratoriet ved IMBA udviklede en biobank med revertible, mutante embryonale stamceller. Denne cellebank - kaldet Haplobank - indeholder over 100, 000 muterede, betingede mus embryonale stamcellelinjer, målrettet mod omkring 70 procent af det proteinkodende genom (næsten 17, 000 gener). "Haplobank er tilgængelig for alle forskere, og repræsenterer det hidtil største bibliotek af hemizyogene mutante embryonale stamcellelinjer til dato. Ressourcen overvinder problemer, der opstår som følge af klonal variabilitet, fordi mutationer kan repareres i enkeltceller og i hele genomskala, "forklarer Ulrich Elling, første og tilsvarende forfatter til den aktuelle publikation i Natur .

Første forfattere Ulrich Elling og Reiner Wimmer. Kredit:PeterDuchek
Vært-patogen-interaktioner og opdagelse af lægemidler
Som et princip-bevis, forfatterne udførte en genetisk screening for at afdække faktorer, der kræves for infektion med rhinovirus - årsagen til forkølelse. De opdagede, at rhinovirus kræver en tidligere ukendt værtscellefaktor, phospholipase A2G16 (PLA2G16), at dræbe celler. Yderligere, de viste, at et specifikt domæne for PLA2G16 er påkrævet for infektion og kan være et attraktivt lægemiddelmål. Interessant nok, PLA2G16 viste sig også for nylig at være nødvendig for vellykket infektion med relaterede vira, herunder poliovirus.
Nye gener til udvikling af blodkar
I en anden proof-of-princip skærm, forfatterne udnyttede det pluripotente potentiale af embryonale stamceller ved at differentiere dem til blodkarorganoider. Dannelse af blodkar (angiogenese) er afgørende for udvikling og vedligeholdelse af væv, såvel som for sygdomme som kræft. Forfatterne screenede kandidatangiogenesegener, der var repræsenteret i Haplobank, og opdagede flere nye faktorer, der påvirker blodkarvækst i organoider. Vigtigere, de observerede en stærk variation mellem uafhængige kloner, fremhæver fordelen ved reparerbar mutagenese til sammenligning af mutanter med deres genetisk reparerede søsterkloner.
"Haplobank kan bruges til skærme til at skabe helt nye indsigter i biologi og sundhed. Det er vigtigt - fordi gen knockouts kan repareres i vores embryonale stamkloner - muliggør denne ressource også velkontrolleret, robuste og reproducerbare valideringsforsøg. Vi føler, at dette er et kritisk punkt og bidrag, givet den nuværende indsats for at forbedre stringensen af videnskabelig forskning. "siger Josef Penninger, IMBA -direktør og sidste forfatter.
 Varme artikler
Varme artikler
-
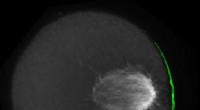 Hvordan kromosomer snyder for chancen for at komme ind i et ægSignaler fra den polariserede cellecortex (i grøn) i museoocytter regulerer mikrotubulus tyrosination (hvid) for at generere spindel-asymmetri i meiose I. Denne asymmetri kan udnyttes af egoistiske ge
Hvordan kromosomer snyder for chancen for at komme ind i et ægSignaler fra den polariserede cellecortex (i grøn) i museoocytter regulerer mikrotubulus tyrosination (hvid) for at generere spindel-asymmetri i meiose I. Denne asymmetri kan udnyttes af egoistiske ge -
 Mennesker overlistede ikke neandertalere,Vi overgav dem bare Neanderthal udryddelse kan meget vel have været en funktion af befolkningens dynamik, ikke mindreværd. Iain Masterton/Getty Images/Canopy Vi moderne mennesker føler os tem
Mennesker overlistede ikke neandertalere,Vi overgav dem bare Neanderthal udryddelse kan meget vel have været en funktion af befolkningens dynamik, ikke mindreværd. Iain Masterton/Getty Images/Canopy Vi moderne mennesker føler os tem -
 Overvågning af mikrober for at holde Marsonauter sundeKredit:CC0 Public Domain For at garantere et sikkert miljø for astronauter på langvarige rummissioner, såsom en rejse til Mars, det er vigtigt at overvåge, hvordan mikroorganismer såsom bakterier
Overvågning af mikrober for at holde Marsonauter sundeKredit:CC0 Public Domain For at garantere et sikkert miljø for astronauter på langvarige rummissioner, såsom en rejse til Mars, det er vigtigt at overvåge, hvordan mikroorganismer såsom bakterier -
 Designerproteiner, der pakker genetisk materiale, kan hjælpe med at levere genterapiLevering af genetisk materiale er en central udfordring i genterapi. Kredit:Kstudio, CC BY Hvis du nogensinde har købt en ny iPhone, du har oplevet god emballage. Den måde låget langsomt adskille
Designerproteiner, der pakker genetisk materiale, kan hjælpe med at levere genterapiLevering af genetisk materiale er en central udfordring i genterapi. Kredit:Kstudio, CC BY Hvis du nogensinde har købt en ny iPhone, du har oplevet god emballage. Den måde låget langsomt adskille
- Cybersikkerhedseksperter siger, at enhedsproducenter har pligt til at holde brugerne sikre mod hacki…
- MXenes tour de force
- MRI-scanning hjælper med næste generations batteridesign
- Det globale kapløb om grundvand accelererer for at brødføde landbrugets voksende behov
- Hatchet enzym, muliggør sygdom og sundhed, eksponeret af neutronstråler
- Australiens bushfire -krise slukker turister


