At få myg til at destruere sig selv

CRISPR/Cas9-medieret forstyrrelse af gener forbundet med øjenpigment fik øjenfarven til at ændre sig fra sort til hvid. Kredit:Michelle Bui, UC Riverside.
Forskere ved University of California, Riverside har udviklet transgene myg, der stabilt udtrykker Cas9-enzymet i deres kimlinje. Tilføjelsen af Cas9 vil muliggøre brugen af CRISPR-genredigeringsværktøjet til at effektivisere, målrettede ændringer af myggenes DNA.
Som proof of concept, forskerne brugte systemet til at forstyrre neglebånd, vinge, og øjenudvikling, producerer helt gul, treøjede og vingeløse myg. Deres langsigtede mål er at bruge Cas9-udtrykkende myg sammen med en anden teknologi - kaldet gendrev - til at indsætte og sprede gener, der undertrykker insekterne og samtidig undgå den resistens, som evolutionen typisk vil favorisere. Aedes aegypti er hovedbærere af dengue, chikungunya, gul feber, og zika-virus, og bliver hurtigt resistente over for almindeligt anvendte pesticider.
Udgivet i dag i Proceedings of the National Academy of Sciences (PNAS) , undersøgelsen blev ledet af Omar Akbari, en assisterende professor i entomologi i UCR's College of Natural and Agricultural Sciences og medlem af universitetets Institut for Integrativ Genome Biologi.
Tidligere bestræbelser på at bruge genomredigering til at forhindre myg i at sprede patogener er blevet hæmmet af lave mutationshastigheder, dårlig overlevelse af redigerede myg, og ineffektiv overførsel af forstyrrede gener til afkom. Akbari og kolleger udviklede transgene myg, der stabilt udtrykker et bakterielt Cas9-enzym i kimlinien, muliggør højeffektiv genomredigering ved hjælp af CRISPR-systemet. CRISPR fungerer som en molekylær saks, udskæring og udskiftning af specifikke DNA -sekvenser baseret på en ribonukleinsyre (RNA) guide. I avisen, holdet brugte systemet til at forstyrre gener, der styrer synet, flugt og fodring, resulterer i myg med et ekstra øje, misdannede vinger, og defekter i øjen- og neglebåndsfarve, blandt andre ændringer.

CRISPR/Cas9-medieret forstyrrelse af gener forbundet med kutikula-pigment fik myg til at blive fra sort til gul, og forstyrrelse af gener forbundet med øjenpigment fik øjenfarven til at ændre sig fra sort til hvid. Kredit:UC Riverside.
Akbari sagde, at disse stammer repræsenterer det første skridt mod at bruge gendrevsystemer til at kontrollere myggepopulationer og reducere de sygdomme, de spreder.
"Disse Cas9-stammer kan bruges til at udvikle split-gen-drev, som er en form for gen-drev, hvorved Cas9 og guide-RNA'erne indsættes på separate genomiske loci og er afhængige af hinanden for spredning. Dette er den sikreste måde at udvikle sig på. og testgener driver i laboratoriet for at sikre, at der ikke spredes i naturen, "Sagde Akbari.
Gendrift øger i høj grad chancerne for, at et gen eller et sæt gener vil blive videregivet til afkom - fra 50 procent til 99 procent. Dette tal kan potentielt stige til 100 procent, når et målgen er forstyrret på flere steder, en teknik kaldet multiplexing, der for nylig er matematisk modelleret af Akbari og kolleger på UC Berkley.
Gendrift kan bruges til at påvirke genetisk arv til fordel for hurtig spredning, selvdestruktive gener – såsom dem, der forstyrrer fertiliteten – og kunne være en miljøvenlig og omkostningseffektiv måde at undertrykke populationer af sygdomsspredende insekter.
"Næste skridt bør tages for at identificere de regulatoriske sekvenser, der kan bruges til at udtrykke guide-RNA'erne fra genomet, og når først disse sekvenser er identificeret, bør udviklingen af gendrev i arten være nøglefærdige, " sagde Akbari.
Titlen på papiret er "Germline Cas9 Expression Yields Highly Efficient Genome Engineering in a Major Worldwide Disease Vector, Aedes Aegypti."
 Varme artikler
Varme artikler
-
 Venstrehåndsfisk og asymmetriske hjernerCichlider af Perissodus microlepis-arten endemisk til Tanganyika-søen i Afrika. Kredit:Universitetet i Konstanz Til mennesker, at være højrehåndet eller venstrehåndet spiller en vigtig rolle. De f
Venstrehåndsfisk og asymmetriske hjernerCichlider af Perissodus microlepis-arten endemisk til Tanganyika-søen i Afrika. Kredit:Universitetet i Konstanz Til mennesker, at være højrehåndet eller venstrehåndet spiller en vigtig rolle. De f -
 Hvad gør Acetonalkohol til en gramplet?Gram-pletten er en differentieret farvningsprocedure, der viser, hvilke bakterier der er Gram-positive eller Gram-negative, baseret på deres pletfarve. Acetonalkohol er et reagens, der anvendes i d
Hvad gør Acetonalkohol til en gramplet?Gram-pletten er en differentieret farvningsprocedure, der viser, hvilke bakterier der er Gram-positive eller Gram-negative, baseret på deres pletfarve. Acetonalkohol er et reagens, der anvendes i d -
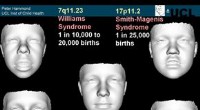 DysmorfologiBillede høflighed UCL Institute of Child Health Forældre, der har mistanke om, at deres barn kan have en genetisk lidelse, har et nyt værktøj i deres læges diagnostiske arsenal. En britisk læge har f
DysmorfologiBillede høflighed UCL Institute of Child Health Forældre, der har mistanke om, at deres barn kan have en genetisk lidelse, har et nyt værktøj i deres læges diagnostiske arsenal. En britisk læge har f -
 Tankeeksperiment:Hvad er vores transhumane vej ud over jorden?Hvad kan en interplanetarisk menneskelig race udvikle sig til at være? David Ryle/Getty Images Menneskeheden eksisterer på et nysgerrigt sted lige nu, hængende mellem tidligere sci-fi-drømme om menne
Tankeeksperiment:Hvad er vores transhumane vej ud over jorden?Hvad kan en interplanetarisk menneskelig race udvikle sig til at være? David Ryle/Getty Images Menneskeheden eksisterer på et nysgerrigt sted lige nu, hængende mellem tidligere sci-fi-drømme om menne
- Forskere skærper ind på størrelse og miljøpåvirkning af kvanteprikkerne, der bruges i hybridsol…
- Grækenland i sorg, da flere stadig er savnet efter dødelig oversvømmelse
- Spektral tilsløring kunne gøre objekter usynlige under realistiske forhold
- Massivt behov for dyrkning af træer på gårde
- To miljøfaktorer, der påvirker transpiration
- Denne luftfugtighedsfordøler indånder atmosfærisk vand og udånder energi


