Cellevagten, der neutraliserer hepatitis B
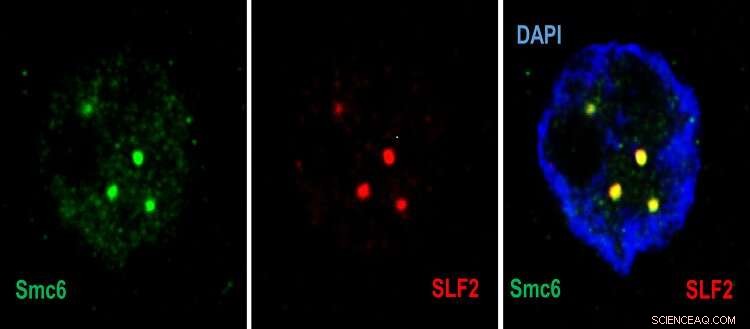
Konfokale mikroskopibilleder, der viser i cellekernen (blå), rekrutteringen af Smc5/6 (grøn) af SLF2 (rød) til PML-kroppe. Kredit:© UNIGE – Laboratory of Professor Michel Strubin – Regulering af hepatitis B-virus genekspression – Institut for Mikrobiologi og Molekylær Medicin.
Hepatitis B-virus (HBV) er ansvarlig for en af de mest alvorlige og almindelige infektionssygdomme. Overført gennem biologiske væsker angriber det levercellerne. Den kroniske form af sygdommen kan føre til alvorlige komplikationer, herunder skrumpelever og leverkræft. Der findes ingen effektiv behandling for den kroniske form af sygdommen, som kun kan forebygges ved vaccination. Efter at have identificeret et nøgleproteinkompleks, der er aktivt, når vores krop er inficeret med virussen, har et hold fra Universitetet i Genève (UNIGE) dechifreret den præcise funktion af denne beskyttelsesmekanisme, hvilket åbner vejen for nye terapeutiske mål. Disse resultater kan læses i tidsskriftet Nature Structural &Molecular Biology .
Hepatitis B er den mest almindelige form for hepatitis. Det er en virussygdom forårsaget af hepatitis B-virus. Det er hovedsageligt seksuelt overført eller overføres gennem blod. Det er op til 100 gange mere smitsomt end HIV. Ved at inficere levercellerne forårsager denne virus en forbigående betændelse i dette organ, der også kan udvikle sig til en kronisk infektion. Dette kan derefter føre til alvorlige patologier, såsom skrumpelever eller leverkræft. Det anslås, at næsten 1 million mennesker dør hvert år af denne sygdom på verdensplan. Der er ingen endelig behandling for kronisk hepatitis B. Den eneste måde at forhindre det på er at blive vaccineret, før sygdommen viser sig.
I 2016 afslørede et UNIGE-hold ledet af Michel Strubin, en lektor i Institut for Mikrobiologi og Molekylær Medicin og i Geneve Center for Inflammation Research ved UNIGE Fakultet for Medicin, en mekanisme, der er afgørende for at forstå denne sygdom:når vores immunsystemet forsvarer sig mod det, et kompleks – et indbyrdes afhængigt sæt – af seks proteiner kaldet SMC5/6, der er til stede i vores celler, detekterer det virale DNA og blokerer det. Virussen slår derefter tilbage og producerer et specifikt protein, X-proteinet. Dette protein kommer ind i cellen og nedbryder SMC5/6, som ikke længere er i stand til at spille sin vagtpostrolle.
En tretrinsmekanisme
Før denne opdagelse var den antivirale funktion af SMC5/6 ukendt. Det blev kun identificeret som et nøglekompleks til den strukturelle vedligeholdelse af vores kromosomer. I dag har Michel Strubins team fået et nyt gennembrud. I en nylig undersøgelse, udført i samarbejde med det amerikanske medicinalfirma Gilead Sciences, identificerede UNIGE-forskerne de tre trin og de specifikke proteiner, der kræves for at SMC5/6 kan spille sin antivirale rolle.
"I det første trin opdager et protein af SMC5/6-komplekset virusets DNA og fanger det," forklarer Fabien Abdul, en senior forsknings- og undervisningsassistent ved Institut for Mikrobiologi og Molekylær Medicin ved UNIGE Fakultet for Medicin og første gang forfatter til undersøgelsen. "Så tager et andet protein af komplekset - SLF2 - virusets fangede DNA ind i et underrum af kernen i den angrebne celle, kaldet PML-legemet. Et tredje protein - Nse2 - kommer derefter i spil og hæmmer virus' kromosom."
Da SMC er en stor familie af proteinkomplekser, ønskede forskerne også at vide, om andre medlemmer af denne familie var i stand til at binde sig til hepatitis B viralt DNA. "Vi opdagede, at denne kompetence var unik for SMC5/6," siger Fabien Abdul.
Mod nye terapeutiske mål
For at opnå disse resultater arbejdede forskerholdet på in vitro cellekulturer. "Vi brugte molekylærbiologiske teknikker og mere specifikt genetiske sakse kaldet CRISPR-Cas9. Dette værktøj gjorde det muligt for os at klippe DNA-strengene i cellerne og dermed slette eller modificere genet, der koder for hvert protein, der udgør SMC5/6-komplekset. Takket være denne teknik , var vi i stand til at få det ene eller det andet af proteinerne til at forsvinde og dermed forstå deres respektive funktioner i komplekset," forklarer Michel Strubin, undersøgelsens sidste forfatter. Baseret på disse observationer kunne de tre trin af den antivirale mekanisme etableres.
Denne opdagelse giver en bedre forståelse af, hvordan komplekset fungerer under dets antivirale virkning. Det kunne således bane vejen for identifikation af nye terapeutiske mål til bekæmpelse af hepatitis B-virus. "Næste fase af forskningen vil bestå i bedre at dechifrere mekanismen for inhibering af virussen i cellekernens underkompartment," angiver Aurélie Diman, en postdoc-forsker i Michel Strubins laboratorium. Der skal også arbejdes med X-proteinet, hvis rolle blev identificeret af UNIGE-forskerne i 2016, for bedre at forstå hepatitis B's modangrebsmekanisme mod den antivirale aktivitet af den cellulære SMC5/6. + Udforsk yderligere
Modangreb af hepatitis B-virus
 Varme artikler
Varme artikler
-
 Støjforurening skader dyr, og vi ved ikke engang hvor megetHvis du ikke kan lide støj, så forestil dig, hvordan kæledyr og andre dyr har det med det. Kredit:Aleksey Boyko/Shutterstock Fra byggeprojekter til travle veje, fly og jernbaner, menneskelig støj e
Støjforurening skader dyr, og vi ved ikke engang hvor megetHvis du ikke kan lide støj, så forestil dig, hvordan kæledyr og andre dyr har det med det. Kredit:Aleksey Boyko/Shutterstock Fra byggeprojekter til travle veje, fly og jernbaner, menneskelig støj e -
 RIP Jeremy den venstrehavede havesneglKredit:University of Nottingham En en ud af en million mutant havesnegl, der opnåede international berygtelse efter at en offentlig appel blev lanceret for at hjælpe ham med at finde en ægtefælle,
RIP Jeremy den venstrehavede havesneglKredit:University of Nottingham En en ud af en million mutant havesnegl, der opnåede international berygtelse efter at en offentlig appel blev lanceret for at hjælpe ham med at finde en ægtefælle, -
 Hvad er fysiske egenskaber, der er overgivet fra forældre?DNAet i cellerne indeholder den genetiske information for hvert individ, inklusive de fysiske træk, som vi forbinder med, hvordan nogen ser ud, såsom hårfarve, øjenfarve, fregner og huler . Børn arver
Hvad er fysiske egenskaber, der er overgivet fra forældre?DNAet i cellerne indeholder den genetiske information for hvert individ, inklusive de fysiske træk, som vi forbinder med, hvordan nogen ser ud, såsom hårfarve, øjenfarve, fregner og huler . Børn arver -
 Landbrugsparasit tager kontrol over værtsplantens generDodder, en parasitplante, knyttet til en værtsplante, hvorfra den får vand og næringsstoffer. Parasitten indsætter mikroRNAer i værten, der kan dæmpe ekspressionen af værtsgener. Dette er det første
Landbrugsparasit tager kontrol over værtsplantens generDodder, en parasitplante, knyttet til en værtsplante, hvorfra den får vand og næringsstoffer. Parasitten indsætter mikroRNAer i værten, der kan dæmpe ekspressionen af værtsgener. Dette er det første
- Gentagne udstrømninger af varm vind fundet tæt på sort hul
- Kapløb for at redde indonesisk krokodille, der er ramt af dækhalskæde
- Billede:Hubbles -skive af Skytten
- Undersøgelse viser, at homoseksuelle og biseksuelle unge er mere tilbøjelige til at opgive kirkega…
- Grundlæggende om fiskeopdræt
- In vivo billeddannelse af den menneskelige hornhinde ved høj hastighed og høj opløsning


