Hvordan et smalspektret antibiotikum sigter mod C. difficile
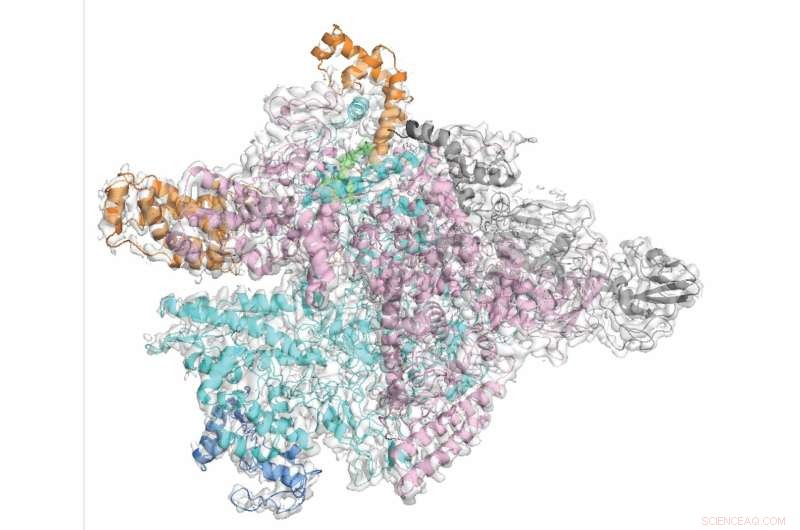
Forskerne demonstrerede på molekylært niveau, hvordan fidaxomicin selektivt retter sig mod C. diff, mens de skåner de uskyldige bakterielle tilskuere. Kredit:Rockefeller University
De fleste antibiotika er tveæggede sværd. Udover at dræbe det patogen, de er ordineret til, decimerer de også gavnlige bakterier og ændrer sammensætningen af tarmmikrobiomet. Som følge heraf bliver patienterne mere tilbøjelige til at blive smittet igen, og lægemiddelresistente stammer er mere tilbøjelige til at dukke op.
Svaret på dette problem kan være smalspektrede antibiotika, der kun dræber en eller nogle få arter af bakterier, hvilket minimerer risikoen for sideskader. I en nylig undersøgelse kiggede Rockefeller-forskere nøje på et sådant antibiotikum, fidaxomicin, der bruges til at behandle Clostridium difficile eller C. diff, en af de mest almindelige sundhedsrelaterede infektioner. Forskerne demonstrerede på molekylært niveau, hvordan fidaxomicin selektivt retter sig mod C. diff, mens de skåner de uskyldige bakterielle tilskuere.
Resultaterne, detaljeret i Nature , kan hjælpe forskere i kapløbet om at udvikle nye smalspektrede antibiotika mod andre patogener.
"Jeg ønsker, at folk, videnskabsmænd og læger tænker anderledes om antibiotika," siger Elizabeth Campbell, en forskningslektor ved Rockefeller. "Da vores mikrobiom er afgørende for sundheden, har smalspektrede tilgange en vigtig rolle at spille i, hvordan vi behandler bakterielle infektioner i fremtiden."
Gadematisk selektiv
C. diff er en toksinproducerende bakterie, der kan betænde tyktarmen og forårsage alvorlig diarré. Det inficerer omkring en halv million mennesker i USA, for det meste på hospitaler, og omkring én ud af 11 af dem over 65 år, der dør inden for en måned.
I årevis har læger brugt bredspektrede antibiotika til behandling af C. diff. Fidaxomicin er et relativt nyt alternativ, som fik FDA-godkendelse i 2011.
Ligesom flere andre antibiotika, herunder tuberkuloselægemidlet rifampicin, er fidaxomicin rettet mod et enzym kaldet RNA-polymerase (RNAP), som bakterien bruger til at transskribere sin DNA-kode til RNA. For at forstå præcis, hvorfor fidaxomicin selektivt hæmmer RNAP i C. diff og ikke i de fleste andre bakterier, gik Campbell sammen med biokemiker Robert Landick fra University of Wisconsin-Madison for at visualisere C. diff RNAP ved hjælp af kryo-elektronmikroskopi, en kraftfuld billedbehandlingsteknik, der kan afsløre 3D-formen af molekyler og fange lægemiddelmolekylet og dets mål i aktion. "Selvom den overordnede arkitektur af RNAP i forskellige bakterier er ens, er der stadig betydelige forskelle," siger Campbell.
Spionerer på RNAP
En stor udfordring var dog først at producere store mængder C. diff, en anaerob kim, der ikke vokser i nærvær af ilt. Studiets første forfatter, Xinyun Cao, fra Landick Lab, brugte to år på at udvikle et system til lettere at producere C. diff RNAP ved hjælp af E. Coli, en letvoksende bakterie, der ofte bruges i laboratoriet.
Ved at bruge dette materiale genererede medførsteforfatter Hande Boyaci, en postdoc på Campbells team, billeder af C. diff RNAP låst med fidaxomicin ved næsten atomær opløsning. Indkilet i et hængsel mellem to underenheder af RNAP åbner fidaxomicin-syltetøj enzymets tang og forhindrer det i at gribe fast i genetisk materiale og starte transkriptionsprocessen.
Ved en nøje undersøgelse af kontaktpunkterne mellem RNAP og fidaxomicin identificerede forskerne én aminosyre på RNAP, der binder til fidaxomicin, men som er fraværende i hovedgrupperne af tarmmikrober, der spares af fidaxomicin. En genetisk ændret version af C. diff, der manglede denne aminosyre, var uforstyrret af fidaxomicin, ligesom andre kommensale bakterier i tarmen. Omvendt blev bakterier, der fik det tilføjet til deres RNAP, følsomme over for fidaxomicin.
Resultaterne tyder på, at denne ene aminosyre blandt de 4.000 aminosyrer i denne robuste og essentielle transkriptionsmaskine er dens akilleshæl, der er ansvarlig for at dræbe bakterierne med fidaxomicin.
Den tilgang, der bruges i denne undersøgelse, foreslår en køreplan for at udvikle nye og sikrere antibiotika, siger forskerne. Ved yderligere at belyse RNAP-strukturen af forskellige bakterier, kan forskere designe antibiotika, der retter sig mod hvert patogen mere selektivt og effektivt.
 Varme artikler
Varme artikler
-
 Din hjerne på: eksamen StressDu har studeret hele ugen, du kender materialet som bagsiden af din hånd, men dit hjerte banker stadig, når du går ind i eksamenslokalet, og dit sind bliver tomt, når du ser på papiret. Hvis det nog
Din hjerne på: eksamen StressDu har studeret hele ugen, du kender materialet som bagsiden af din hånd, men dit hjerte banker stadig, når du går ind i eksamenslokalet, og dit sind bliver tomt, når du ser på papiret. Hvis det nog -
 Industrielle mikroalger til fremstilling af sund biologisk olieEn mekanistisk model af NoDGAT2s-medieret MCT-syntese i N. oceanica. Kredit:Liu Yang De genetiske talenter af en marin mikroalge er nu låst op for at producere mellemkædede triacylglyceroler, som e
Industrielle mikroalger til fremstilling af sund biologisk olieEn mekanistisk model af NoDGAT2s-medieret MCT-syntese i N. oceanica. Kredit:Liu Yang De genetiske talenter af en marin mikroalge er nu låst op for at producere mellemkædede triacylglyceroler, som e -
 Tusinder af pingvinkyllinger sulter i AntarktisMassesult har udslettet tusinder af Adelie pingvinkyllinger i Antarktis, da usædvanlig tyk havis tvang deres forældre til at fodre yderligere efter mad Massesult har udslettet tusindvis af pingvin
Tusinder af pingvinkyllinger sulter i AntarktisMassesult har udslettet tusinder af Adelie pingvinkyllinger i Antarktis, da usædvanlig tyk havis tvang deres forældre til at fodre yderligere efter mad Massesult har udslettet tusindvis af pingvin -
 Spanien melder om tilfælde af kogalskabKoen, der viste sig at have bovin spongiform encephalopati (BSE) i provinsen Salamanca, blev ødelagt Et tilfælde af gal ko -sygdom er blevet opdaget i det nordvestlige Spanien, sagde den Paris-bas
Spanien melder om tilfælde af kogalskabKoen, der viste sig at have bovin spongiform encephalopati (BSE) i provinsen Salamanca, blev ødelagt Et tilfælde af gal ko -sygdom er blevet opdaget i det nordvestlige Spanien, sagde den Paris-bas
- Kenya forbyder engangsplast i beskyttede områder
- Unikt sværd kaster nyt lys på vikingerejser over Nordsøen
- Rumskrot harpuneret som hval i kredsløbsoprydningstest
- Et skridt på vejen mod bedre behandlinger mod vira
- Størstedelen af amerikanerne mener, at det er vigtigt, at USA forbliver en global leder inden for…
- Antenne Tower Types


