GoT-ChA:Nyt værktøj afslører, hvordan genmutationer påvirker celler
Et team ledet af forskere ved Weill Cornell Medicine og New York Genome Center har udviklet en avanceret metode til at afsløre, hvordan genmutationer forstyrrer den normale pakning af DNA. Disse strukturelle ændringer, som ændrer mønstre af genaktivitet i en celle, er kendt som epigenetiske ændringer og kan føre til malignitet.
Den nye metode, beskrevet i et papir offentliggjort i Nature , tilbyder biologer et kraftfuldt værktøj, der kan anvendes i mange undersøgelsesområder, fra grundlæggende cellebiologi til studiet af, hvordan kræftformer opstår. Forskerne demonstrerede den nye metode ved at bruge den til at belyse, hvordan en almindelig genmutation udøver sin virkning på to sjældne blodkræftformer.
"Denne nye teknik bør tillade brede fremtidige udforskninger af sammenhængen mellem mutationer og epigenetiske ændringer i forbindelse med kræft og relaterede tilstande," siger seniorforfatter Dr. Dan Landau, professor i medicin i afdelingen for hæmatologi og medicinsk onkologi ved Weill. Cornell Medicine og et kernefakultetsmedlem ved New York Genome Center.
Undersøgelsen blev ledet af Dr. Franco Izzo, en postdoc-forsker i Landau Lab under undersøgelsen, nu adjunkt ved Icahn School of Medicine ved Mount Sinai.
Den nye præstation er den seneste i rækken af enkeltcellede profileringsinnovationer fra Landaus forskningsgruppe. Sådanne metoder, også kaldet "enkeltcellede multi-omics"-metoder, gør det muligt for forskere at karakterisere DNA-mutationer, genaktivitetsmønstre, celleoverfladeproteiner og andre lag af information - alt sammen i en individuel celle ved at bruge automatisering til at behandle mange tusinde celler ad gangen.
I modsætning hertil bruges ældre metoder på bulkprøver, som typisk indeholder blandinger af forskellige celletyper såvel som både muterede og ikke-muterede celler – hvilket i høj grad begrænser enhver analyse.
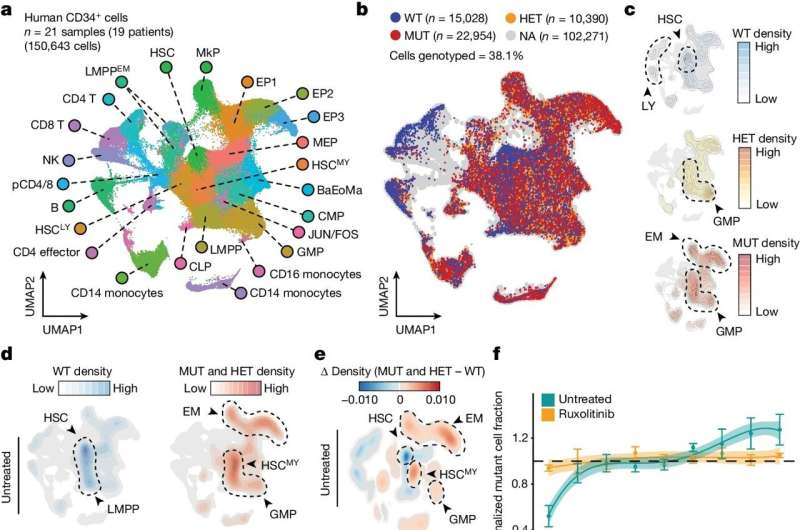
I dette tilfælde udviklede holdet en mere følsom og nøjagtig enkeltcellemetode til påvisning af DNA-mutationer af interesse. De kombinerede derefter dette med en ny teknik til at kortlægge en celles "kromatintilgængelighed" - i det væsentlige de steder, hvor DNA er relativt åbent og tilgængeligt for gentranskription - som et bredt billede af cellens epigenetiske tilstand.
Forskerne kaldte disse parrede teknikker "Genotyping af målrettede loci med enkeltcellet kromatintilgængelighed" eller "GoT-ChA" og viste, at de kunne integrere GoT-ChA med enkeltcellemetoder til profilering af andre informationslag såsom RNA'er og celle- overfladeproteiner.
Forskerne demonstrerede styrken af deres nye værktøjssæt ved at bruge det til at studere blodceller fra patienter med to sjældne blodkræftformer, polycythemia vera og myelofibrose. Disse kræftformer er normalt drevet af en specifik mutation i et gen kaldet JAK2 - en mutation, der har været impliceret i andre tilstande og også findes hos mange tilsyneladende raske mennesker.
Begge kræftformer har også forstyrrelser i den normale blodcellemodningsproces, hvilket indebærer, at JAK2-mutationen inducerer betydelige epigenetiske ændringer - men begrænsningerne af ældre metoder betød, at disse epigenetiske ændringer og andre nedstrømseffekter af mutationen ikke var godt forstået. Med GoT-ChA var forskerne i stand til at katalogisere disse effekter meget detaljeret.
"Man troede, at ved myelofibrose, for eksempel, er knoglemarvsbetændelse drevet af marvs mikromiljø, men vi opdagede, at inflammatoriske ændringer i blodstamceller direkte skyldes JAK2-mutationen og også afhænger af celletypen," sagde Landau, der er også medlem af Sandra og Edward Meyer Cancer Center og Englander Institute of Precision Medicine ved Weill Cornell Medicine.
Resultaterne tyder på, at potente nye JAK2-hæmmere, som i øjeblikket er under udvikling, kan være nyttige til behandling af myelofibrosepatienter, sagde han.
Landau bemærkede, at GoT-ChA generelt burde være nyttig til at studere tilstande, hvor DNA-mutationer - som kan opstå gennem livet af forskellige årsager - kun er til stede i et mindretal af celler i et organ og derfor er svære eller umulige at studere med traditionelle , præ-enkeltcelle teknikker.
Studiets medførste forfattere, udover Izzo, var M.D.-Ph.D. studerende Robert Myers, postdoc-stipendiat Saravanan Ganesan og doktorgradskandidat Levan Mekerishvili, alle fra Landau Laboratory.
Flere oplysninger: Franco Izzo et al., Kortlægning af genotyper til kromatintilgængelighedsprofiler i enkeltceller, Nature (2024). DOI:10.1038/s41586-024-07388-y
Journaloplysninger: Natur
Leveret af Cornell University
 Varme artikler
Varme artikler
-
 Kan vi bringe neandertalerne tilbage?Et folk fra en fjern fortid. Altmodern/Getty Images Neanderthalere og mennesker sameksisterede i tusinder af år, men forholdet mellem de to menneskelige arter var altid lidt dysfunktionelt. Teorier v
Kan vi bringe neandertalerne tilbage?Et folk fra en fjern fortid. Altmodern/Getty Images Neanderthalere og mennesker sameksisterede i tusinder af år, men forholdet mellem de to menneskelige arter var altid lidt dysfunktionelt. Teorier v -
 Er regenerativt landbrug et øko-wake-up call?Kredit:Pixabay/FelixMittermeier Kunne regenerativt landbrug være fremtiden for WA fødevareproduktion? Næste gang du åbner dit spisekammer eller køleskab, skal du vælge fem madvarer. Ved du, hvor d
Er regenerativt landbrug et øko-wake-up call?Kredit:Pixabay/FelixMittermeier Kunne regenerativt landbrug være fremtiden for WA fødevareproduktion? Næste gang du åbner dit spisekammer eller køleskab, skal du vælge fem madvarer. Ved du, hvor d -
 Hvordan dækafgrøder kan beskytte Chesapeake BayDækafgrøder plantet med kun to ugers mellemrum i september viser betydelige forskelle i biomasse i slutningen af efterårets vækstsæson. En nylig undersøgelse viste, at tidligere plantning af dækafgr
Hvordan dækafgrøder kan beskytte Chesapeake BayDækafgrøder plantet med kun to ugers mellemrum i september viser betydelige forskelle i biomasse i slutningen af efterårets vækstsæson. En nylig undersøgelse viste, at tidligere plantning af dækafgr -
 Virus omkobler værtscellulært maskineri for at maksimere viral produktionet skema af CHIKV RNA-genom. b Transkriptomanalyser af cytosol (Cyt) og ER-kompartmenter i CHIKV-inficerede celler. Gener blev plottet i overensstemmelse med deres log2-fold ændringer i CHIKV-inficere
Virus omkobler værtscellulært maskineri for at maksimere viral produktionet skema af CHIKV RNA-genom. b Transkriptomanalyser af cytosol (Cyt) og ER-kompartmenter i CHIKV-inficerede celler. Gener blev plottet i overensstemmelse med deres log2-fold ændringer i CHIKV-inficere
- Kan det arkæologiske felt give spaden videre til lokalbefolkningen for at forvalte kulturarven?
- Hvad sker der med planter, hvis de ikke har sol?
- Gensyn med kvanteeffekter i MEMS
- Kan vi skabe en rigtig Jurassic Park?
- Giftige metaller kan påvirke elevernes sundhed, siger videnskabsmænd
- Fotonik:Graphen øger lysdetektorer på chip


