Tager biddet af slangegift

Mere effektive behandlinger for slangebid, som hvert år rammer millioner af mennesker verden over, er ved at dukke op fra EU-forskning.
I november 2023 udsendte politiet i den sydhollandske by Tilburg en alarm om en "ekstremt giftig" slange, der var to meter lang og var undsluppet fra sine afgrænsninger.
Den grønne mamba blev til sidst fundet bag en gipsvæg i ejerens hus, hvilket lettede offentlighedens bekymring og afsluttede det, der havde været en national nyhed.
Millioner af bid
Hændelsen gav byboere i Europa en sjælden eksponering for en trussel, som mange millioner mennesker andre steder møder regelmæssigt.
Hvert år bliver omkring 5,4 millioner mennesker globalt – ofte i verdens fattigste samfund – bidt af giftslanger, og lande som Bangladesh, Burkina Faso, Indien og Nigeria anslås at have et stort antal tilfælde.
Globalt forårsager disse bid mellem 81.000 og 138.000 dødsfald og omkring 400.000 permanente kvæstelser inklusive amputationer som følge af alvorlig vævsskade. Forgiftning af slangebid anses for at være en overset tropisk sygdom af Verdenssundhedsorganisationen og er mere dødelig end alle andre WHO-anerkendte oversete tropiske sygdomme.
Professor Nicholas Casewell søger at reducere disse tal som en del af et forskningsprojekt, der modtog EU-midler til at forbedre slangebidsbehandlinger, som næsten ikke har ændret sig i de sidste 100 år.
"Hvis du får det rigtige antigift hurtigt nok, så kan de være effektive - de er livreddende behandlinger," sagde Casewell, ekspert i slangebid ved Liverpool School of Tropical Medicine i Storbritannien. "Men de har så mange mangler forbundet med dem."
Antigifte fremstilles i dag ved at indsprøjte heste eller får med lave doser gift, så dyrene udvikler antistoffer mod det. Blodserum, der indeholder disse antistoffer, opsamles derefter fra værtsdyrene for at blive brugt som antigift - en proces, som først blev demonstreret af en fransk læge ved navn Albert Calmette i 1890'erne.
Antigifte er dyre, viser sig ofte at være ineffektive og skal opbevares på køl. De kan også forårsage alvorlige bivirkninger såsom udslæt, ledsmerter, feber og hævelse af lymfeknuder.
Desuden er store medicinalvirksomheder holdt op med at producere antigifte, fordi de ikke anses for at være økonomisk levedygtige. Det øger behovet for nye behandlinger.
Ny nanopartikel
Projektet, som Casewell er involveret i, samler forskningsinstitutter og universiteter fra Belgien, Frankrig, Portugal og Storbritannien. Kaldet ADDovenom og løber i fire et halvt år indtil marts 2025.
Forskerne har henvendt sig til en ny syntetisk nanopartikel for at udvikle mere effektive behandlinger for slangebid. Viruslignende er det kendt som en ADDomer.
ADDomerer samler sig selv, fordi de består af mange kopier af det samme protein. Disse proteiner kan modificeres på en måde, der gør dem i stand til at gribe og neutralisere specifikke mål.
I tilfælde af ADDovenom er disse mål toksinerne i slangegift.
hugorme og mambaer
Projektet fokuserer på de savskællede hugorme og mambaer i Afrika. De forårsager en betydelig medicinsk byrde blandt slanger i regionen syd for Sahara.
Savskællede hugorme signalerer, når de føler sig truede og kan bide ved at rulle sig sammen til en kringleform og gnide deres skæl sammen – en handling, der skaber en sydende lyd.
Mambaer, som er nært beslægtet med kobraer, søger at skræmme angribere af ved at rejse sig og hvæse.
Giften fra disse to typer slanger har meget forskellige virkninger. Hos savskællede hugorme forårsager det indre blødninger, mens det hos mambas udløser lammelser.
Under ADDovenom har proteomikeksperter ved University of Liege i Belgien analyseret giften fra disse slanger høstet på herpetarium på Liverpool School of Tropical Medicine, som huser den største samling af giftslanger i Storbritannien og er en af de mest forskelligartede i Europa.
Gifte er en blanding af forskellige komponenter. Projektets mål er at identificere og neutralisere de farligste giftstoffer i savskællede hugorme og mambaer.
"Vi kender nu sammensætningen af disse gifte, og vi kan udvinde de mest rigelige og mest patogene toksiner," sagde professor Christiane Berger-Schaffitzel, en biokemiker ved det britiske-baserede universitet i Bristol, som driver projektet. "Dette er vores mål."
Mere effektiv, overkommelig
Nuværende antigifte virker på alt andet end en målrettet måde.
Højst er det kun omkring en tredjedel af anti-gift-antistoffer, der er rettet mod slangegift. Resten er antistoffer, som dyrene, hvorfra antigiften blev skabt, havde cirkuleret i deres kroppe for at bekæmpe andre patogener.
Dette, kombineret med det faktum, at antistofferne stammer fra dyr, er grunden til, at antigifte kan gøre folk syge. Patienter udvikler en tilstand kendt som serumsyge, som er en allergisk reaktion på disse yderligere og unødvendige komponenter i dyreserumet.
"Her forsøger vi at gøre tingene på en meget mere rationel, informeret måde," sagde Casewell.
Forskerne håber, at deres planlagte behandlinger ud over at være mere effektive vil være sikrere.
Og fordi ADDomers forbliver stabile ved høje temperaturer, behøver behandlingerne ikke at blive nedkølet, hvilket gør dem mere tilgængelige for fjerntliggende landdistrikter i troperne.
Selvom projektet afsluttes om mindre end et år, gør forskningen det ikke.
Ud over at videreudvikle ADDomer nanopartikler til forskellige toksiner, vil forskerne undersøge, hvordan disse produkter kan fremstilles i skala for at holde dem overkommelige.
"Omkostningerne er virkelig vigtige, fordi vi taler om udviklingslande og landdistrikter," sagde Berger-Schaffitzel. "Folk har helt sikkert problemer med at få råd til behandling."
Hvornår ADDomer-baserede behandlinger bliver tilgængelige, afhænger af forhold såsom den beskyttelse, de giver mus mod toksinerne og hugormegiften. For en livreddende behandling er målet en bred reaktivitet på tværs af gifte fra forskellige hugorme.
Laboratoriefremstillede antistoffer
ADDomers er ikke det eneste håb for at udvikle nye måder at tackle slangebid på.
Andre EU-finansierede forskere forsøger at gøre det med humane monoklonale antistoffer. Disse er laboratorieproducerede kloner af menneskekroppens utallige antistoffer.
"Vi har antistoffer i vores blod, men det er en blanding af millioner af forskellige antistoffer," siger Andreas Hougaard Laustsen-Kiel, professor i antistofteknologier ved Danmarks Tekniske Universitet. "En monoklonal er bare et af disse mange, mange antistoffer."
Konstruerede monoklonale antistoffer bruges allerede inden for flere områder af medicinen, hovedsageligt som målrettede terapier for cancer og som behandlinger for autoimmune sygdomme, herunder leddegigt.
Laustsen-Kiel og kolleger udvikler antistoffer, der neutraliserer flere relaterede toksiner i slangegifte.
"Det er relativt ligetil at finde et monoklonalt antistof, der bare binder et mål," sagde han. "Det sværeste er at finde et monoklonalt antistof, der binder flere forskellige mål."
Deres projekt, MABSTER, skal afsluttes i december 2024 efter fem år.
Som med ADDovenom har forskerne fokuseret på slangetoksiner, der forårsager en betydelig medicinsk byrde.
MABSTER har udviklet og testet på mus en blanding af antistoffer, der kan neutralisere koralslangegifte, en familie af farvestrålende, meget giftige slanger, der lever i Amerika.
Holdet er også tæt på at færdiggøre en blanding til behandling af bid fra afrikanske kobraer og mambaer, ifølge Laustsen-Kiel.
Færre bivirkninger
Ud over at konstruere antistofferne til at målrette mod specifikke toksiner, forsøger holdet at sikre, at antistofferne overlever længere i kroppen for at bekæmpe nye toksiner igen.
Normalt, efter at et antistof har bundet sig til sit mål, kendt som et antigen - i dette tilfælde et gifttoksin - neutraliserer det antigenet og signalerer det til ødelæggelse. I denne proces forbliver antistoffet optaget af antigenet, indtil begge er ødelagt.
Ved at konstruere de monoklonale antistoffer til at være følsomme over for deres mikromiljø, er det muligt at programmere dem, så de frigiver antigenet under cellulær genbrug af antistof-antigen-komplekset, ifølge Laustsen-Kiel.
Dette efterlader antistoffet intakt og frit til at binde flere toksiner.
Genanvendelse af antistoffer på denne måde kunne gøre det muligt at anvende lavere doser af behandling, hvilket øger effektiviteten og potentielt reducerer bivirkninger.
Laustsen-Kiel gentog Berger-Schaffitzel ved at understrege vigtigheden af overkommelige priser, når det kommer til sådanne behandlinger.
"Det næste store forskningsspørgsmål er, hvordan man fremstiller disse ting billigt," sagde han.
Flere oplysninger:
- ADDovenom
- MABSTER
Leveret af Horizon:The EU Research &Innovation Magazine
 Varme artikler
Varme artikler
-
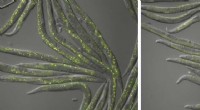 Forskere opdager ny vej til håndtering af stressEn sammenlægning, eller klumper, af proteiner er fremhævet gennem fluorescerende gule prikker i en kontrolgruppe (venstre) og i en pals-22-genstamme (højre), hvor næsten ingen proteinaggregering er sy
Forskere opdager ny vej til håndtering af stressEn sammenlægning, eller klumper, af proteiner er fremhævet gennem fluorescerende gule prikker i en kontrolgruppe (venstre) og i en pals-22-genstamme (højre), hvor næsten ingen proteinaggregering er sy -
 Probiotisk kombination forbedrer østerslarvernes overlevelse drastiskKredit:Oregon State University Overlevelsesraten for østerslarver blev væsentligt øget ved at behandle dem med specifikke kombinationer af probiotika, fandt forskere fra Oregon State University i e
Probiotisk kombination forbedrer østerslarvernes overlevelse drastiskKredit:Oregon State University Overlevelsesraten for østerslarver blev væsentligt øget ved at behandle dem med specifikke kombinationer af probiotika, fandt forskere fra Oregon State University i e -
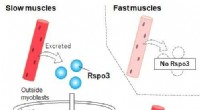 Hvordan langsomme muskelfibre overbeviser deres naboer om at slutte sig til demRspo3 udskilles fra langsomme type I fibre (ikke fra hurtige fibre), hvilket fremmer ophobningen af beta-catenin inde i myoblaster. Dette fører til den øgede produktion af MyHC I og den endelige dif
Hvordan langsomme muskelfibre overbeviser deres naboer om at slutte sig til demRspo3 udskilles fra langsomme type I fibre (ikke fra hurtige fibre), hvilket fremmer ophobningen af beta-catenin inde i myoblaster. Dette fører til den øgede produktion af MyHC I og den endelige dif -
 Irakiske dyreelskere går online for at hjælpe med at redde Bagdads vildfarneHjemløse dyr udsættes typisk for grusomhed eller endda udryddelse på gaderne i byen, men nu søger nogle dyreelskere at bruge sociale medier til at ændre holdninger og finde kærlige ejere til de firben
Irakiske dyreelskere går online for at hjælpe med at redde Bagdads vildfarneHjemløse dyr udsættes typisk for grusomhed eller endda udryddelse på gaderne i byen, men nu søger nogle dyreelskere at bruge sociale medier til at ændre holdninger og finde kærlige ejere til de firben
- Inkjet-printet flydende metal kunne bringe bærbar teknologi, blød robotik
- Merkur kunne være den perfekte destination for et solsejl
- Koffein giver spor til ultra-forbigående migration med positive ladninger
- Havcirkulationen vil sandsynligvis være skyld i sværhedsgraden af rødvandet i 2018
- Brug af mikrobølger til lavprisproduktion af alkalimetalliske fosfat-nanokompositter til brug i nat…
- Ny undersøgelse afslører, hvorfor kvinder tager sexede selfies


