Blokering af bortskaffelse af cellulært affald:Forskere viser, hvordan proteinaggregater forstyrrer cellens molekylære balance
Proteinaggregater, også kendt som proteinklumper, er unormale klynger af fejlfoldede proteiner, der akkumuleres inde i celler. Disse aggregater kan interferere med forskellige cellulære processer, herunder den afgørende funktion at fjerne cellulært affald.
Undersøgelsen, udført af forskere ved University of California, San Francisco (UCSF), fokuserede på et specifikt proteinaggregat kaldet p62-kroppe. P62-legemer findes i celler i hele kroppen, men er særligt rigelige i nerveceller (neuroner).
Ved hjælp af avancerede billeddannelsesteknikker observerede forskerne, at p62-kroppe akkumuleres omkring strukturer kaldet lysosomer, som er ansvarlige for at nedbryde og genbruge cellulært affald. Normalt opsluger og fordøjer lysosomer p62-kroppe, men når aggregaterne bliver for mange, kan de overvælde lysosomernes kapacitet, hvilket fører til en trafikprop af cellulært affald.
Forskerne fandt ud af, at opbygningen af p62-legemer forringer lysosomernes evne til at smelte sammen med andre vesikler i cellen, hvilket forhindrer dem i effektivt at levere deres last til nedbrydning. Denne forstyrrelse i affaldsbortskaffelsessystemet forårsager en ophobning af giftige stoffer i cellen, hvilket bidrager til cellulær dysfunktion og potentielt neurodegeneration.
Interessant nok opdagede forskerne også, at p62-kroppe kan fange andre proteiner, der er involveret i cellulær affaldsrensning, såsom ubiquitin og autophagy-receptorer, hvilket yderligere hindrer cellens evne til at fjerne affald. Denne kaskade af begivenheder forværrer blokaden i cellulært affaldsbortskaffelse, og fortsætter en ond cirkel af cellulær skade.
Undersøgelsen giver ny indsigt i de mekanismer, hvorved proteinaggregater forstyrrer cellulær affaldsbortskaffelse, hvilket potentielt kan bidrage til udviklingen af neurodegenerative sygdomme. Ved at forstå disse mekanismer kan forskere udforske nye terapeutiske strategier, der sigter mod at rense proteinaggregater, genoprette cellulære affaldsbortskaffelsesveje og bremse sygdomsprogression.
 Varme artikler
Varme artikler
-
 Hvordan træffer en slimform en beslutning uden hjerne?Physarum polycephalum slimforme kan lagre hukommelsen fra tidligere fodringsbegivenheder i et netværk af elastiske rør, informere retningen for fremtidige migration. Wikimedia Commons (CC By-SA 3.0)
Hvordan træffer en slimform en beslutning uden hjerne?Physarum polycephalum slimforme kan lagre hukommelsen fra tidligere fodringsbegivenheder i et netværk af elastiske rør, informere retningen for fremtidige migration. Wikimedia Commons (CC By-SA 3.0) -
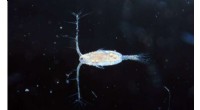 Eksperimentel evolution:Marine copepoder kan genetisk tilpasse sig skiftende havforholdCopepod forstørret. De små krebsdyr kan tilpasse sig skiftende miljøfaktorer - så længe ikke for mange stressfaktorer kommer sammen. Kredit:Alexandra Hahn/GEOMAR Copepoder er blandt de vigtigste or
Eksperimentel evolution:Marine copepoder kan genetisk tilpasse sig skiftende havforholdCopepod forstørret. De små krebsdyr kan tilpasse sig skiftende miljøfaktorer - så længe ikke for mange stressfaktorer kommer sammen. Kredit:Alexandra Hahn/GEOMAR Copepoder er blandt de vigtigste or -
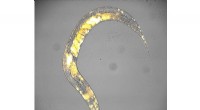 Mødres alder påvirker genetisk lighed mellem tvillingerCaenorhabditis elegans orm med fluorescerende æggeblomme og embryoner indeni. Kredit:Lola Davey, Marcos Francisco Perez, CRG Påvirker en mors alder træk og egenskaber ved hendes afkom, og hvor? Et
Mødres alder påvirker genetisk lighed mellem tvillingerCaenorhabditis elegans orm med fluorescerende æggeblomme og embryoner indeni. Kredit:Lola Davey, Marcos Francisco Perez, CRG Påvirker en mors alder træk og egenskaber ved hendes afkom, og hvor? Et -
 Du behøver ikke at være en sød koala for at være en Instagram-influencer. Giv firben og insekter…Mængden af engagementsindlæg med hver gruppe af dyr (taxon) modtaget. Kategorier, der ikke deler bogstaver, er væsentligt forskellige fra hinanden, f.eks. pattedyr (b) modtog større engagement end h
Du behøver ikke at være en sød koala for at være en Instagram-influencer. Giv firben og insekter…Mængden af engagementsindlæg med hver gruppe af dyr (taxon) modtaget. Kategorier, der ikke deler bogstaver, er væsentligt forskellige fra hinanden, f.eks. pattedyr (b) modtog større engagement end h
- III-V halvleder fotoniske integrerede kredsløb går kvante
- Comet U1 NEOWISE—en mulig kikkertkomet?
- Forskere studerer tarm-til-CNS translokation af sølv nanomaterialer
- Thailandske lovgivere godkender kontroversiel cybersikkerhedslov
- For meget uønsket mad fremstillet af en teenager Blind
- Unge arbejdere lider længere under recessioner


