Frysfrakturering:Låser op for cellemembranarkitektur og proteinfunktion
SolStock/E+/GettyImages
Cellemembraner er sammensat af phospholipid-dobbeltlag med indlejrede proteiner, der medierer essentielle cellulære funktioner. Traditionel lysmikroskopi kan ikke opløse individuelle membranproteiner. Frysefraktur, kombineret med elektronmikroskopi, giver os mulighed for at opdele frosne membraner langs deres dobbeltlag, hvilket blotlægger proteinfordelingen i lipidmatrixen. Ved at integrere yderligere mærkningsteknikker kan forskerne kortlægge specifikke proteiner såvel som bakterielle og virale komponenter med sub-nanometer-præcision.
Grundlæggende trin i frysebrud
1. Frys hurtigt celler eller væv i flydende nitrogen for at immobilisere strukturer.
2. Brug en mikrotom til at bryde den frosne prøve; membranen spalter mellem de to fosfolipidblade, hvor hydrofobe interaktioner er svagest.
3. Udfør fryseætsning i højvakuum for at fjerne iskrystaller og bevare fine detaljer.
4. Skygge brudfladen med en tynd film af kulstof og platin for at skabe en stabil replika, der følger membrantopologien.
5. Fordøj resterende organisk materiale med syre, og efterlad en platinskal, der repræsenterer den blottede membranoverflade.
6. Undersøg replikaen ved transmissionselektronmikroskopi (TEM) til strukturel analyse.
Frys ætsning
Fryseætsning fjerner iskrystaller, der ellers ville skjule membrandetaljer. Vakuumtørringsprocessen bevarer den oprindelige arkitektur og muliggør observation af dynamiske membranaktiviteter, intracellulære organeller og virale samlinger.
Elektronmikroskopi
Transmissionselektronmikroskopi tilbyder op til 1 million gange forstørrelse og opløsninger ned til 3nm, hvilket gør det til den foretrukne modalitet til replikaer med frysebrud. Scanning elektronmikroskopi (SEM) er mindre almindeligt anvendt i denne sammenhæng, men kan give overfladetopologi af større prøver.
Afsløring af cellemembranstruktur
Siden introduktionen for over fem årtier siden har frysefraktur-TEM været medvirkende til at bekræfte lipid-dobbeltlagsmodellen af plasmamembranen og belyse det rumlige arrangement af integrale, perifere og lipid-forankrede proteiner. Teknikken afslører, om proteiner er "flydere", der driver inden for dobbeltlaget eller "ankre", der spænder over begge foldere, og det kan detektere proteinaggregering eller klyngedannelse. Når de kombineres med immunogold-mærkning – antistoffer mærket med elektrontætte partikler – kan forskere identificere specifikke proteiner og udlede deres funktionelle roller.
 Varme artikler
Varme artikler
-
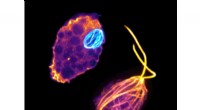 Hvad hjerneædende amøber kan fortælle os om mangfoldigheden af liv på jorden og evolutionær h…Naegleria gruberi-celler bruger et sæt tubuliner til at bygge en mitotisk spindel (cyan, venstre), og et andet sæt tubuliner (orange, højre) til at omdanne til en flagellatcelletype. Kredit:Katrina Ve
Hvad hjerneædende amøber kan fortælle os om mangfoldigheden af liv på jorden og evolutionær h…Naegleria gruberi-celler bruger et sæt tubuliner til at bygge en mitotisk spindel (cyan, venstre), og et andet sæt tubuliner (orange, højre) til at omdanne til en flagellatcelletype. Kredit:Katrina Ve -
 Forskere opdager ny produktionsvej for plante-SOS-signalerKredit:University of Hohenheim / Andreas Schaller Når skadelige insekter angriber en plante, det forsvarer sig. Det danner beskyttende stoffer, der er giftige for insekterne. Dette forsvarssvar ak
Forskere opdager ny produktionsvej for plante-SOS-signalerKredit:University of Hohenheim / Andreas Schaller Når skadelige insekter angriber en plante, det forsvarer sig. Det danner beskyttende stoffer, der er giftige for insekterne. Dette forsvarssvar ak -
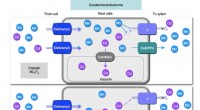 Hold giftig cadmium ude af ris på den genetiske mådeI Pokkali optager rødderne på grund af duplikeret OsNramp5 mere Mn og Cd i rodcellerne sammenlignet med andre risvarianter (for eksempel Koshihikari). Det meste Cd optaget gennem OsNramp5 sekvestreres
Hold giftig cadmium ude af ris på den genetiske mådeI Pokkali optager rødderne på grund af duplikeret OsNramp5 mere Mn og Cd i rodcellerne sammenlignet med andre risvarianter (for eksempel Koshihikari). Det meste Cd optaget gennem OsNramp5 sekvestreres -
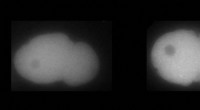 Hvordan fysik og biologi arbejder sammen for at udforske livets mekanismerTil venstre, MEX-5 protein. Til højre, PLK-1 protein i C. elegans embryoner. Hvid viser den højere eller lavere tilstedeværelse af proteinerne. Kredit:UNIGE / Laboratoire Monica Gotta Hver af vores
Hvordan fysik og biologi arbejder sammen for at udforske livets mekanismerTil venstre, MEX-5 protein. Til højre, PLK-1 protein i C. elegans embryoner. Hvid viser den højere eller lavere tilstedeværelse af proteinerne. Kredit:UNIGE / Laboratoire Monica Gotta Hver af vores
- Hvorfor er Europa så sårbart over for hedebølger
- Bundet til Mars - nedtælling til første interplanetariske lancering fra Californien
- Hvad tager planeter ind, og hvad de afgiver?
- Hvordan forestilte Dalton atomet?
- Nyt kamera uden linse skaber 3D-billeder fra en enkelt eksponering
- Hvad er definitionen for kromosomer?


