Rødt fosfor:egenskaber, produktion og anvendelser
By Joan Reinbold
Opdateret 24. marts 2022
Oversigt
Rødt fosfor er den næstmest almindelige allotrope af fosfor, kendt for sit mørkerøde udseende og lave toksicitet. I modsætning til sin hvide pendant er den ikke-phosphorescerende og udviser moderat kemisk reaktivitet.
Atomstruktur
Molekylet består af tetraedrisk bundne fosforatomer, der kæder sammen og danner en netværksstruktur, der er ansvarlig for dets stabilitet og karakteristiske farve.
Produktionsmetoder
Kommercielt produceres rødt fosfor ved at opvarme hvidt fosfor i forseglede beholdere eller ved at udsætte det for sollys, begge processer omdanner den meget reaktive hvide form til den sikrere røde allotrope.
Historisk baggrund
Processen blev opdaget i 1845 af den østrigske kemiker Anton von Schrötter og involverede opvarmning af hvidt fosfor i en nitrogenfyldt kolbe til ca. 482°F (250°C) i flere timer.
Nøgleapplikationer
- Halvlederfremstilling
- Pyroteknik og sikkerhedskampe
- Gødning og pesticider
- Røgbomber og brand-granater
- Organiske syntesereagenser
- Visse flammehæmmende formuleringer
- Produktion af elektroluminescerende belægning
Bemærkning om sikkerhed og lovgivning
Mens rødt fosfor er relativt sikkert til industriel brug, kan det misbruges i ulovlig narkotikaproduktion. Ved fremstilling af metamfetamin reagerer det med jod og danner jodhydridsyre, hvilket understreger vigtigheden af korrekt håndtering og regulering.
For detaljerede sikkerhedsretningslinjer, se NIOSH Pocket Guide to Chemical Hazards .
 Varme artikler
Varme artikler
-
 Mikroalger renser vand og producerer værdifulde forbindelserAlgerne optræder i grupper på to eller fire. Kredit:Lorenzo Ferro Kemikere ved Umeå Universitet i MicroBioRefine-konsortiet viser, at nordiske mikroalger, der får lov til at vokse i saltvand, både
Mikroalger renser vand og producerer værdifulde forbindelserAlgerne optræder i grupper på to eller fire. Kredit:Lorenzo Ferro Kemikere ved Umeå Universitet i MicroBioRefine-konsortiet viser, at nordiske mikroalger, der får lov til at vokse i saltvand, både -
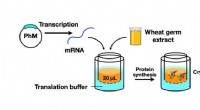 Ny cellefri proteinkrystalliseringsmetode til fremme af strukturbiologiSkematisk illustration af CFPC-proces ved anvendelse af et hvedekimproteinsyntesesæt til at syntetisere polyhedrinmonomer (PhM), som blev yderligere krystalliseret til polyederkrystaller i nanostørrel
Ny cellefri proteinkrystalliseringsmetode til fremme af strukturbiologiSkematisk illustration af CFPC-proces ved anvendelse af et hvedekimproteinsyntesesæt til at syntetisere polyhedrinmonomer (PhM), som blev yderligere krystalliseret til polyederkrystaller i nanostørrel -
 Beskyttelse af naturen:Professor hjælper med at minimere rekreative forstyrrelser for dyrelivetEksempler på billeder af fugle og pattedyr, der ofte søges af besøgende til parker og andre vilde områder:(a) spidshorn, (b) stablet spætte, c) storhornsfår, og (d) vermillion fluesnapper. Kredit:Kevi
Beskyttelse af naturen:Professor hjælper med at minimere rekreative forstyrrelser for dyrelivetEksempler på billeder af fugle og pattedyr, der ofte søges af besøgende til parker og andre vilde områder:(a) spidshorn, (b) stablet spætte, c) storhornsfår, og (d) vermillion fluesnapper. Kredit:Kevi -
 Menneskelige rester fundet i stor australsk krokodilleSaltvandskrokodiller, som kan blive op til syv meter lang og veje mere end et ton, er et fællestræk i Australiens tropiske nord og dræber i gennemsnit to mennesker om året Menneskelige rester blev
Menneskelige rester fundet i stor australsk krokodilleSaltvandskrokodiller, som kan blive op til syv meter lang og veje mere end et ton, er et fællestræk i Australiens tropiske nord og dræber i gennemsnit to mennesker om året Menneskelige rester blev
- Hvilken energitransformation opstår, når en baseløber glider sikkert til tredje base?
- Perovskite solceller:Mulige aspekter af høj effektivitet afdækket
- Mere forener os end adskiller os siger forskere
- Hvilke ting i en cellevæg handler med cellulær bevægelse?
- Hvem opdagede de grundlæggende love for genetik?
- Den proces, der er ansvarlig for at overføre materiale nedhældning under påvirkning af tyngdekraf…


