Sådan laver du et batteri med koks og eddike
Batterier konverterer kemisk energi til elektrisk energi, og det tager ikke meget ressourcer til at skabe en - du kan lave et arbejdsbatteri med en citron. Du får måske ikke meget strøm fra en citron, men princippet om elproduktion er det samme som for batteriet i en bil. Det er let at lære om dette princip, når du kan lave enkle batterier hjemme ved hjælp af to usandsynlige ingredienser: koks og eddike.
Sådan fungerer et batteri
En elektrokemisk celle, som er den enkleste type batteri, har tre komponenter: en anode, en katode og en elektrolyt. Anoden og katoden er to forskellige typer af metal, hvoraf den ene taber elektroner lettere end den anden. Hvis de to metaller rørte hinanden, ville elektroner flyde, men for langsomt for at skabe en betydelig strøm. Når katoden og anoden er nedsænket i en elektrolyt, som normalt er en syre, skaber kemiske reaktioner modsatte ladninger på dem, men elektrolytten forhindrer ladningen i at strømme. De kan flyde, hvis du forbinder katoden og anoden med en ledning. Desuden holder løbende reaktioner mellem metaller og elektrolyt batteriet "ladet".
Lav et koksbatteri
Du kan bruge enhver sodavand, der indeholder fosforsyre til at lave en voltaic celle og cola er et godt eksempel (kost eller regelmæssig er fint, det er kun den syre der betyder noget). Aluminium fra en cola kan også lave en god katode, som er den negative terminal. Brug stykker til at skære en strimmel fra dåsen og sandpapiret for at male malingen af. Du har brug for en stribe af kobber til anoden eller en positiv terminal - dette kan du normalt finde i hardwareforretningen. Hæld koks i et glas, sænk striperne og rør strimlerne ved hjælp af sonderne til et voltmeter. Du skal få en læsning på ca. 3/4 volt.
Lav et eddike batteri
Eddike gør også en god elektrolyt, fordi den indeholder eddikesyre. Du kan bruge kobber til anoden, men zink gør en bedre katode end aluminium; Hvis du ikke har en zinkstrimmel, skal du bruge en galvaniseret søm, som er belagt med zink. Du skal komme tæt på en volt fra denne celle. Hvis du vil have strøm til en LED, skal du til at binde to af disse celler i serie for at fordoble spændingen. For at gøre dette skal du forbinde pæren til ledninger, der er forbundet med anoden til et batteri og en katode på den anden og bruge en tredje ledning til at forbinde det andet par elektroder til hinanden.
Observering af en eddikecelle
Da eddike er klart, kan du observere interessante virkninger på elektroderne i en eddike-celle. Hvis du forbinder to af disse celler i serie og bruger dem til at tænde en LED, og du forlader LED'en hele natten, vil du finde et lag af sorte aflejringer på zinkelektroden om morgenen. Det skyldes kobberatomer, som kombinerer med hydrogenioner i elektrolytten og samler på zinkoverfladen. Du bør også se bobler af hydrogengasform på kobberstrimlen, da hydrogenioner fra syren kombineres med elektroner for at danne hydrogenatomer, og atomer parrer op til dannelse af hydrogenmolekyler.
Sidste artikelLodde- og desolderingsteknikker
Næste artikelSådan beregnes Millivolts fra Microsiemens
 Varme artikler
Varme artikler
-
 Hvordan beregnes Wattage?Måleenheden for elektrisk strøm er watt. Wattage repræsenterer mængden af arbejdet eller elforbruget pr. Tidsenhed. Én watt er defineret som en joule per sekund. Wattage er produktet af spænding og
Hvordan beregnes Wattage?Måleenheden for elektrisk strøm er watt. Wattage repræsenterer mængden af arbejdet eller elforbruget pr. Tidsenhed. Én watt er defineret som en joule per sekund. Wattage er produktet af spænding og -
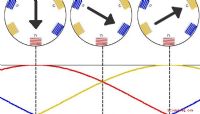 Dele af induktionsmotorerEn induktionsmotor er en type elektrisk motor, der omdanner elektrisk strøm til roterende bevægelse. En induktionsmotor anvender princippet om elektromagnetisk induktion for at få rotoren til at dreje
Dele af induktionsmotorerEn induktionsmotor er en type elektrisk motor, der omdanner elektrisk strøm til roterende bevægelse. En induktionsmotor anvender princippet om elektromagnetisk induktion for at få rotoren til at dreje -
 Sådan bestemmes de positive og negative sider af en magnetJordens poler skaber et magnetfelt, der omgiver planeten. Magneter har deres egne poler, der peger mod jordens poler. Ved hjælp af jordens magnetfelt kan du bestemme de positive og negative sider af e
Sådan bestemmes de positive og negative sider af en magnetJordens poler skaber et magnetfelt, der omgiver planeten. Magneter har deres egne poler, der peger mod jordens poler. Ved hjælp af jordens magnetfelt kan du bestemme de positive og negative sider af e -
 Sådan laver du en robotarmNår du overvejer hvordan den menneskelige arm rent faktisk virker, er robotarmen næsten simpel ved sammenligning. Begge systemer anvender en ramme, som måske eller ikke er bevægelig. Den ene er kemisk
Sådan laver du en robotarmNår du overvejer hvordan den menneskelige arm rent faktisk virker, er robotarmen næsten simpel ved sammenligning. Begge systemer anvender en ramme, som måske eller ikke er bevægelig. Den ene er kemisk


