Hvorfor hurtig opladning reducerer kapaciteten af et bilbatteri

Kredit:CC0 Public Domain
Når lithium-ioner tvinges hurtigt gennem et batteri, kan de sætte sig fast og blive til lithiummetal, der ikke længere er i stand til at bevæge sig gennem batteriet.
Forestil dig at kunne tanke din elbil, mens du stopper for en hurtig snack eller fylder din telefon op, mens du børster tænder.
"Hurtig opladning er en slags den hellige gral. Det er, hvad alle, der ejer en lithium-ion-batteribaseret enhed, ønsker at kunne gøre," siger senioringeniør David Wragg fra Center for Materials Science and Nanotechnology ved Universitetet i Oslo.
Inde i batteriet er der dog en masse kompliceret kemi, der kan være følsom over for, hvor hurtigt det oplades. Ting kan gå galt.
"Kapacitetstab er det mest kritiske," siger Wragg til Titan.uio.no.
"Det er muligt at lave batterier med meget høj kapacitet, som måske giver dig mulighed for at køre din elbil 1000 km, men efter du har opladet og afladet den et par gange, ville du miste omkring halvdelen af den kapacitet og rækkevidde.
Alle genopladelige batterier forringes med tiden, men denne negative effekt er ekstra stærk, når batteriet udsættes for hurtig opladning. Wragg er en af forskerne bag en undersøgelse, der viser hvorfor.
De har kunnet se, at lithium-ionerne, som er så vigtige for et batteris kapacitet, bliver omdannet til rent lithiummetal og ikke længere er anvendelige. Og vigtigst af alt:denne effekt forstærkes kraftigt af hurtig opladning.
Batteriet er som en gyngestol
På den ene side af batteriet er anoden, og på den anden side er katoden. Begge disse elektroder kan lagre elektroner og ioner. Mellem dem er en separator og en flydende elektrolyt, der hjælper ionerne fra den ene side til den anden.
Ioner og elektroner bevæger sig fra den ene side af batteriet til den anden, når du bruger strømmen, der er lagret der, og tilbage igen, når du genoplader det.
"De kalder dette gyngestolsmekanismen, hvor du vipper jernene og elektronerne fra den ene side til den anden."
"Når de er friske, og de fungerer perfekt, kan batterier lagre en vis mængde ioner, og det er systemets samlede kapacitet," siger Wragg.
Når ionerne, som før bevægede sig frem og tilbage, bliver til metal, er de ikke længere i stand til at bevæge sig gennem batteriet. Ionerne er ladede og kan lokkes frem og tilbage. Metalatomerne er neutrale og kan ikke fristes i nogen retning.
"Når lithium er omdannet til metal, er det ikke rigtig tilgængeligt for den elektrokemiske reaktion længere. Denne kapacitet er fuldstændig tabt," siger Wragg.
Dette sker i alle genopladelige lithium-ion-batterier, når du har opladet dem mange nok gange. Men hvorfor bliver det værre, når du oplader hurtigt?
Flaskehalse under hurtig opladning
Under hurtig opladning bevæger det samme antal ioner sig gennem systemet, men meget hurtigere. Alle ioner skal finde deres plads i anoden på meget kortere tid.
"Når du oplader ved dobbelt hastighed, skal du flytte den samme mængde ioner og elektroner på den halve tid," siger Wragg.
Hvis du oplader fire eller seks gange så hurtigt, bliver det naturligvis endnu sværere.
"Det er svært, fordi der er visse grænser for den kemi, der foregår, når du prøver at sætte lithiumioner i et fast elektrodemateriale virkelig hurtigt," siger Wragg.
Anoderne, som modtager ioner under opladningen, er lavet af grafit, som er dannet af tynde lag kulstof. Anoden består af flere millioner sådanne lag.
"Tom grafit er som et spil kort, og lithium-ionerne er som små kugler, der bliver skubbet ind i mellemrummene mellem kortene. Problemet er, at du kan få flaskehalse, når du forsøger at skubbe lithium-ionerne mellem lagene i grafitten.
"Du bliver ved med at skubbe ioner ind, men medmindre de ioner, der allerede er mellem lagene, kan skubbe dybere ind i stakken, er der ikke plads til nye ioner at komme ind i. Når du oplader batteriet rigtig hurtigt, spredes lithiumet ikke gennem det hele. grafitelektrode overhovedet. Den sætter sig bare fast tæt på elektrolytten, hvor anoden og katoden er adskilt."
Det er især her, i disse flaskehalse, at de ladede ioner bliver til neutrale atomer og ophobes i bittesmå metalklumper. Ionerne bevæger sig ikke længere, samtidig med at der tilføres energi. Denne overskydende energi kan være det, der ændrer en ion til et neutralt og stabilt atom.
"Det kaldes lithiumplettering. Det er, når lithiumioner i stedet for at forblive i ionformen bliver til lithiummetal. Dette har været kendt i ret lang tid, men det er ikke rigtig blevet observeret i et fungerende batteri før," Wragg siger.
Dette har Wragg og hans kolleger dog formået at gøre. Ved hjælp af røntgenstråler scannede de batterier hvert 25. millisekund, igen og igen, mens de hurtigt opladede med forskellige hastigheder. Dette gav dem enorme mængder data om, hvad der sker helt ned på atomniveau.
"Vi kunne faktisk se lithiumbelægningen bygge op. Under hurtig opladning kunne vi se mængden af lithium stige virkelig hurtigt. Vores teori er, at det har noget at gøre med denne flaskehals af lithium-ioner. Vi ser mange lithium-ioner tæt på separatoren, og det er også her, vi ser lithiumbelægningen," siger Wragg.
"Det mest sandsynlige er, at du får disse lithium-ioner til at bygge op, og de kan bare ikke komme til grafitten længere. De sætter sig fast der, og der er meget varme, meget energi, der bliver lagt i dem, og så bliver de reduceret til lithiummetal."
De så, hvordan grafitlagene tættest på den anden elektrode var meget rige på lithium, mens der dybere nede i den næsten ikke var lithium overhovedet. Det blev værre, jo hurtigere de opladede.
"Jo hurtigere du skubber den, jo hurtigere sker pletteringen," siger Wragg.
Fremtiden:nanorør og grafen?
Undersøgelsen er på ingen måde enden på hurtig opladning. Det betyder bare, at forskerne skal finde nye og bedre løsninger.
"Nøglen ved dette er, at folk, der laver batterier, forsøger at finde ud af, hvordan lithiumtransporten kan forbedres, så når du oplader hurtigt, er der større chance for, at lithium rent faktisk kommer igennem til hele grafitanoden, " siger Wragg.
Forskere over hele verden leder efter nye materialer og metoder, der kan få batterier til at modstå hurtig opladning bedre.
"For eksempel er der rigtig mange, der bruger kulstofnanorør. Kulstofnanorør er det, man får, hvis man tager et af kortene og krøller det rundt til et rør. Det er ligesom en grafit, der er blevet formet til rør frem for lidt flad. "
Wragg og kolleger ved Universitetet i Oslo arbejder med grafen, enkelte plader af grafit, i anoden.
"Grafit har været kendt i hundreder af år. Grafen og kulstof nanorør har været kendt i omkring 30 år, så det tager tid."
Indtil videre er ingen af disse innovationer dukket op i kommercielle batterier.
"Men det vil uden tvivl ske," siger Wragg.
 Varme artikler
Varme artikler
-
 Kunne 5G virkelig jordfly? Hvorfor USA har forsinket udrulningen af teknologien nær lufthavneKredit:Simlinger/Shutterstock Adskillige internationale flyselskaber aflyste for nylig flyvninger til visse amerikanske lufthavne, fordi udbredelsen af 5G mobilkommunikationsteknologi kunne forst
Kunne 5G virkelig jordfly? Hvorfor USA har forsinket udrulningen af teknologien nær lufthavneKredit:Simlinger/Shutterstock Adskillige internationale flyselskaber aflyste for nylig flyvninger til visse amerikanske lufthavne, fordi udbredelsen af 5G mobilkommunikationsteknologi kunne forst -
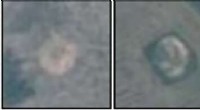 Studiet bruger kunstig intelligens til at vurdere ueksploderede bomber fra VietnamkrigenBombekratere set med satellit. Kredit:Ohio State University Forskere har brugt kunstig intelligens til at opdage bombekratere fra Vietnamkrigstiden i Cambodja fra satellitbilleder - med håbet om,
Studiet bruger kunstig intelligens til at vurdere ueksploderede bomber fra VietnamkrigenBombekratere set med satellit. Kredit:Ohio State University Forskere har brugt kunstig intelligens til at opdage bombekratere fra Vietnamkrigstiden i Cambodja fra satellitbilleder - med håbet om, -
 Fortnite går offline, efter at asteroide sprænger den virtuelle verden i luftenFortnite, som er gratis at spille, har 250 millioner brugere på verdensplan Internetspilfænomenet Fortnite er midlertidigt gået offline, efterlader millioner af afhængige spillere, der spekulerer
Fortnite går offline, efter at asteroide sprænger den virtuelle verden i luftenFortnite, som er gratis at spille, har 250 millioner brugere på verdensplan Internetspilfænomenet Fortnite er midlertidigt gået offline, efterlader millioner af afhængige spillere, der spekulerer -
 LA bliver den første i USA til at installere subway kropsscannereI denne tirsdag, 27. februar, 2018 filfoto ThruVision selvmordsvest-detektionsteknologi afslører en mistænkelig genstand på en mand, til venstre, under en demonstration af Transportation Security Admi
LA bliver den første i USA til at installere subway kropsscannereI denne tirsdag, 27. februar, 2018 filfoto ThruVision selvmordsvest-detektionsteknologi afslører en mistænkelig genstand på en mand, til venstre, under en demonstration af Transportation Security Admi
- Foreslået astrofysikmission for at udføre den første infrarøde spektralundersøgelse af hele him…
- Hvad du behøver at vide om SpaceXs Demo-2-mission
- Der er fundet beviser for jordskælv med lavt skred, der forhindrer udviklingen af store ødelægg…
- Et nyt materiale til regenerativ medicin, der er i stand til at kontrollere celleimmunrespons
- Moodys:AT&T laver en bedømmelsesfejl i deres HBO Max-priser
- Mægtige mus forbliver muskelbundne i rummet, velsignelse for astronauter


