Alkaliske batterier forklaret:nøglekomponenter og hvordan de virker
Af Jack Byrom – Opdateret 24. marts 2022
Beholder
Batteriets ydre skal er et standardiseret stålhus, der sikrer alle indvendige dele. Inde i dette kabinet er katodematerialet støbt mod indervæggen og etablerer den positive terminal.
Katode
Katoden er den elektrode, der tiltrækker elektroner, når kredsløbet er lukket, hvilket tillader strøm at flyde. I alkaliske celler er det en sammensætning af mangandioxid og kulstof (grafit), som er placeret i toppen af batteriet og bliver til +-terminalen.
Separator
Placeret mellem anoden og katoden forhindrer separatoren direkte kontakt, mens den tillader ionbytning. Den tillader kun den elektrokemiske reaktion at fortsætte, når enheden er tændt, og kredsløbet er afsluttet.
Anode
Anoden består af pulveriseret zink. Den monteres sammen med elektrolytten og opsamleren i beholderen, hvorefter batteriet forsegles. Zink tjener som kilden til elektroner.
Elektrolyt
Alkaliske batterier bruger en kaliumhydroxid (KOH) opløsning. Denne elektrolyt bader anoden og letter bevægelsen af ioner og elektroner, hvilket gør det muligt for cellen at generere spænding.
Samler
En messingstift, der er indlejret i midten af anoden, samler strømmen og forbindes til den negative terminal i bunden af batteriet.
 Varme artikler
Varme artikler
-
 To japanske operatører udsætter udgivelsen af Huawei -telefonerTo af Japans førende mobiltelefonudbydere sagde, at de vil udsætte frigivelsen af nye håndsæt lavet af Huawei efter et amerikansk forbud mod amerikanske virksomheder, der sælger teknologi til den ki
To japanske operatører udsætter udgivelsen af Huawei -telefonerTo af Japans førende mobiltelefonudbydere sagde, at de vil udsætte frigivelsen af nye håndsæt lavet af Huawei efter et amerikansk forbud mod amerikanske virksomheder, der sælger teknologi til den ki -
 Boeing søger at forlade krisetilstand, da det rapporterer resultaterUnder lup efter to dødbringende flystyrt, Boeing vil rapportere indtjening i denne uge Under voksende kontrol fra investorer og regulatorer, Den kæmpende amerikanske luft- og rumfartsgigant Boeing
Boeing søger at forlade krisetilstand, da det rapporterer resultaterUnder lup efter to dødbringende flystyrt, Boeing vil rapportere indtjening i denne uge Under voksende kontrol fra investorer og regulatorer, Den kæmpende amerikanske luft- og rumfartsgigant Boeing -
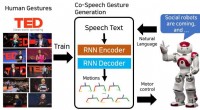 End-to-end læring af generering af co-tale gestus til humanoide robotterDen foreslåede model genererer en sekvens af overkropsstillinger og er trænet på menneskelige gestus fra TED-foredrag. Kredit:Yoon et al. Forskere ved Electronics and Telecommunications Research I
End-to-end læring af generering af co-tale gestus til humanoide robotterDen foreslåede model genererer en sekvens af overkropsstillinger og er trænet på menneskelige gestus fra TED-foredrag. Kredit:Yoon et al. Forskere ved Electronics and Telecommunications Research I -
 Taler om, hvordan vi taler om etik i kunstig intelligensKredit:CC0 Public Domain Hvis du vil forstå, hvordan folk tænker (og føler) om nye teknologier, det er vigtigt at forstå, hvordan medier tænker (og skriver) om nye teknologier. En nylig analyse a
Taler om, hvordan vi taler om etik i kunstig intelligensKredit:CC0 Public Domain Hvis du vil forstå, hvordan folk tænker (og føler) om nye teknologier, det er vigtigt at forstå, hvordan medier tænker (og skriver) om nye teknologier. En nylig analyse a
- Hvad er de 4 hoveddele af en blomst?
- Det er uundgåeligt, at internettet ændrer, hvordan vi forholder os – det, der betyder noget, er
- Hvad har Animals -celler den plante?
- Hvad er nogle eksempler på trådlignende svampe?
- Skriv den kemiske ligning, der repræsenterer fremstilling af ethen ud fra ethanol?
- Hvad er multiplikation?


