Hvordan virker håndvarmere? Et videnskabeligt blik
1. Aktivering :Du snapper eller ryster håndvarmeren for at igangsætte en kemisk reaktion.
2. Natriumacetat-krystallisation :Reaktionen omdanner superafkølet natriumacetat til faste natriumacetatkrystaller.
3. Varmeproduktion :Krystallisationsprocessen frigiver varme, hvilket hæver temperaturen på opløsningen og håndvarmeren.
4. Jernkatalysator :Jern eller jernoxid hjælper med at fremskynde krystallisationsreaktionen.
5. Eksoterm reaktion :Processen er eksoterm, hvilket betyder, at der frigives varme.
6. Opvarmningsvarighed :Varmen varer flere timer, så længe der er uomsat natriumacetat.
Genanvendelige håndvarmere:
1. Kernepunkt :Disse håndvarmere har en metalskive, der fungerer som et kernedannelsespunkt for krystallisation.
2. Bøjning :Du bøjer eller bøjer metalskiven for at starte krystallisationsreaktionen.
3. Varmefrigivelse :Reaktionen genererer varme, hvilket hæver temperaturen på håndvarmeren.
4. Køling :Efterhånden som reaktionen afsluttes, køler håndvarmeren ned.
5. Genkogning :Du placerer den afkølede håndvarmer i kogende vand for at smelte natriumacetatet.
6. Omkrystallisering :Natriumacetatet omkrystalliserer, når du fjerner det fra vandet og lader det køle af.
Gel-baserede håndvarmere :
1. Klik på Aktivering :Du klikker på en metalskive eller knap for at starte en kemisk reaktion.
2. Eksoterm reaktion :Den kemiske reaktion skaber varme gennem en oxidationsproces.
3. Gelopvarmning :Gelen inde i håndvarmeren indeholder salte og vand, som absorberer varmen.
4. Varmefordeling :Gelen fordeler varmen jævnt i hele håndvarmeren.
5. Varighed og genopladning :Nogle gel-baserede håndvarmere kan genoplades ved kogning til fremtidig brug.
Sidste artikelHvis temperaturen er 30 grader F, hvorfor får vi nogle gange sne
Næste artikelHeliummangel! Hvad hvis vi løb tør for helium?
 Varme artikler
Varme artikler
-
 Forbedring af diamantens kvantesansevneEn diamantprøve oplyst af grønt lys i specialbygget mikroskop. Prøven placeres på en speciel holder, inden for et printkort, bruges til at levere mikrobølger, der tillader kvantemanipulationer og magn
Forbedring af diamantens kvantesansevneEn diamantprøve oplyst af grønt lys i specialbygget mikroskop. Prøven placeres på en speciel holder, inden for et printkort, bruges til at levere mikrobølger, der tillader kvantemanipulationer og magn -
 Alternativt materiale til superledende radiofrekvenshulrumFotomontage viser en prøve af faststof, ren niob før belægning (venstre), og belagt med et tyndt lag Nb3Sn (højre). Kredit:HZB I moderne synkrotronkilder og frielektronlasere, superledende radiofr
Alternativt materiale til superledende radiofrekvenshulrumFotomontage viser en prøve af faststof, ren niob før belægning (venstre), og belagt med et tyndt lag Nb3Sn (højre). Kredit:HZB I moderne synkrotronkilder og frielektronlasere, superledende radiofr -
 Revolutionerende superledende magnetplade design og analyseKredit:CC0 Public Domain Ved produktion af integrerede kredsløb (computerchips), kontinuerlig innovation er afgørende for at forblive konkurrencedygtig. Et stort mål er at øge produktiviteten af
Revolutionerende superledende magnetplade design og analyseKredit:CC0 Public Domain Ved produktion af integrerede kredsløb (computerchips), kontinuerlig innovation er afgørende for at forblive konkurrencedygtig. Et stort mål er at øge produktiviteten af -
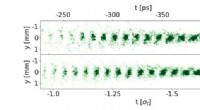 AWAKE-samarbejdet opnår kontrol over ustabiliteten af en protonbundt i plasmaBilledet opsummerer en af avisens vigtige pointer:at elektronbundtet sætter protonbunkens selvmodulation i gang (timingen af mikrobundtoget kan reproduceres fra begivenhed til begivenhed), og at n
AWAKE-samarbejdet opnår kontrol over ustabiliteten af en protonbundt i plasmaBilledet opsummerer en af avisens vigtige pointer:at elektronbundtet sætter protonbunkens selvmodulation i gang (timingen af mikrobundtoget kan reproduceres fra begivenhed til begivenhed), og at n
- Hvordan forudsagde Benjamin Gompertz vores dødsfald?
- Hvem ejer historien? Head-to-head undersøgelse af velgørenhedsledede vs. deltagerledede fundraisin…
- Undersøgelse identificerer ny vej for Grønlands smeltevand til at nå havet
- Kraftfuld ny enhed til at studere forvirrende proces
- Afsidesliggende østrandplastik peger på større affaldsproblem
- Green Deal:Godt for et klimaneutralt Europa, dårligt for planeten


