Forskere løser et magnesiummysterium i genopladeligt batteris ydeevne

Kredit:CC0 Public Domain
Genopladelige batterier baseret på magnesium, i stedet for lithium, har potentialet til at udvide elbilernes rækkevidde ved at pakke mere energi ind i mindre batterier. Men uforudsete kemiske vejspærringer har bremset den videnskabelige udvikling.
Og de steder, hvor fast stof møder væske - hvor de modsat ladede batterielektroder interagerer med den omgivende kemiske blanding kendt som elektrolytten - er de kendte problempunkter.
Nu, et forskerhold ved U.S. Department of Energy's Joint Center for Energy Storage Research, ledet af forskere ved Lawrence Berkeley National Laboratory (Berkeley Lab), har opdaget et overraskende sæt kemiske reaktioner, der involverer magnesium, som forringer batteriets ydeevne, selv før batteriet kan lades op.
Resultaterne kan være relevante for andre batterimaterialer, og kunne styre designet af næste generations batterier mod løsninger, der undgår disse nyligt identificerede faldgruber.
Holdet brugte røntgeneksperimenter, teoretisk modellering, og supercomputersimuleringer for at udvikle en fuld forståelse af den kemiske nedbrydning af en flydende elektrolyt, der forekommer inden for titusvis af nanometer fra en elektrodeoverflade, der forringer batteriets ydeevne. Deres resultater er offentliggjort online i tidsskriftet Materialernes kemi .
Batteriet, de testede, havde magnesiummetal som dets negative elektrode (anoden) i kontakt med en elektrolyt bestående af en væske (en type opløsningsmiddel kendt som diglyme) og et opløst salt, Mg(TFSI)2.
Mens kombinationen af materialer, de brugte, menes at være kompatible og ikke-reaktive i batteriets hviletilstand, eksperimenter ved Berkeley Labs Advanced Light Source (ALS), en røntgenkilde kaldet en synkrotron, afdækkede, at dette ikke er tilfældet og førte undersøgelsen i nye retninger.
"Folk havde troet, at problemerne med disse materialer opstod under batteriets opladning, men i stedet viste eksperimenterne, at der allerede var en vis aktivitet, " sagde David Prendergast, der leder Theory of Nanostructured Materials Facility på Molecular Foundry og fungerede som en af undersøgelsens ledere.
"På det tidspunkt blev det meget interessant, " sagde han. "Hvad kan muligvis forårsage disse reaktioner mellem stoffer, der formodes at være stabile under disse forhold?"
Molecular Foundry-forskere udviklede detaljerede simuleringer af det punkt, hvor elektroden og elektrolytten mødes, kendt som grænsefladen, angiver, at der ikke bør forekomme spontane kemiske reaktioner under ideelle forhold, enten. Simuleringerne, selvom, tog ikke højde for alle de kemiske detaljer.
"Før vores undersøgelser, " sagde Ethan Crumlin, en ALS-forsker, der koordinerede røntgeneksperimenterne og ledede undersøgelsen sammen med Prendergast, "Der var mistanke om opførselen af disse materialer og mulige forbindelser til dårlig batteriydelse, men de var ikke blevet bekræftet i et fungerende batteri."
Kommercielt populære lithium-ion-batterier, som driver mange bærbare elektroniske enheder (såsom mobiltelefoner, bærbare computere, og elværktøj) og en voksende flåde af elektriske køretøjer, shuttle lithium ioner - lithium atomer, der bliver ladet ved at kaste en elektron - frem og tilbage mellem de to batteri elektroder. Disse elektrodematerialer er porøse på atomær skala og lades alternativt op eller tømmes for lithium-ioner, efterhånden som batteriet oplades eller aflades.
I denne type batteri, den negative elektrode er typisk sammensat af kulstof, som har en mere begrænset kapacitet til at lagre disse lithium-ioner end andre materialer ville.
Så at øge tætheden af lagret lithium ved at bruge et andet materiale ville gøre det lettere, mindre, kraftigere batterier. Brug af lithiummetal i elektroden, for eksempel, kan pakke flere lithiumioner ind i samme rum, selvom det er et meget reaktivt stof, der brænder, når det udsættes for luft, og kræver yderligere forskning i, hvordan man bedst pakker og beskytter det for langsigtet stabilitet.
Magnesiummetal har en højere energitæthed end lithiummetal, hvilket betyder, at du potentielt kan lagre mere energi i et batteri af samme størrelse, hvis du bruger magnesium frem for lithium.
Magnesium er også mere stabilt end lithium. Dens overflade danner et selvbeskyttende "oxideret" lag, da det reagerer med fugt og ilt i luften. Men inden for et batteri, dette oxiderede lag menes at reducere effektiviteten og forkorte batteriets levetid, så forskere leder efter måder at undgå dens dannelse.
For at udforske dannelsen af dette lag mere detaljeret, holdet brugte en unik røntgenteknik udviklet for nylig på ALS, kaldet APXPS (omgivelsestryk røntgenfotoelektronspektroskopi). Denne nye teknik er følsom over for den kemi, der forekommer på grænsefladen mellem et fast stof og en væske, hvilket gør det til et ideelt værktøj til at udforske batterikemi på overfladen af elektroden, hvor det møder den flydende elektrolyt.
Allerede før en strøm blev ført ind i testbatteriet, røntgenresultaterne viste tegn på kemisk nedbrydning af elektrolytten, specifikt ved grænsefladen af magnesiumelektroden. Resultaterne tvang forskerne til at genoverveje deres molekylære billede af disse materialer, og hvordan de interagerer.
Det de besluttede er, at den selvstabiliserende, tyndt oxidoverfladelag, der dannes på magnesiumet, har defekter og urenheder, der driver uønskede reaktioner.
"Det er ikke selve metallet, eller dets oxider, det er et problem, " sagde Prendergast. "Det er det faktum, at du kan have ufuldkommenheder i den oxiderede overflade. Disse små forskelle bliver steder for reaktioner. Den nærer sig selv på denne måde."
En yderligere runde af simuleringer, som foreslog mulige defekter i den oxiderede magnesiumoverflade, viste, at defekter i anodens oxiderede overfladelag kan afsløre magnesiumioner, der så fungerer som fælder for elektrolyttens molekyler.
Hvis fritsvævende hydroxidioner - molekyler indeholdende et enkelt oxygenatom bundet til et brintatom, der kan dannes som spormængder af vand reagerer med magnesiummetallet - møder disse overfladebundne molekyler, de vil reagere.
Dette spilder elektrolyt, udtørring af batteriet over tid. Og produkterne af disse reaktioner forurener anodens overflade, forringe batteriets funktion.
Det tog flere gentagelser frem og tilbage, mellem de eksperimentelle og teoretiske medlemmer af holdet, at udvikle en model i overensstemmelse med røntgenmålingerne. Indsatsen blev støttet af millioner af timers computerkraft på laboratoriets National Energy Research Scientific Computing Center.
Forskere bemærkede vigtigheden af at have adgang til røntgenteknikker, nanoskala ekspertise, og computerressourcer på det samme laboratorium.
Resultaterne kan være relevante for andre typer batterimaterialer, også, herunder prototyper baseret på lithium- eller aluminiummetal. Prendergast sagde, "Dette kunne være et mere generelt fænomen, der definerer elektrolytstabilitet."
Crumlin tilføjede, "Vi er allerede begyndt at køre nye simuleringer, der kunne vise os, hvordan man modificerer elektrolytten for at reducere ustabiliteten af disse reaktioner." Ligeledes, han sagde, det kan være muligt at skræddersy overfladen af magnesium for at reducere eller eliminere noget af den uønskede kemiske reaktivitet.
"I stedet for at tillade det at skabe sin egen grænseflade, du kunne konstruere det selv for at kontrollere og stabilisere grænsefladekemien, " tilføjede han. "Lige nu fører det til ukontrollerbare begivenheder."
 Varme artikler
Varme artikler
-
 Ren, elektrisk drevet proces til at adskille kommercielt vigtige metaller fra sulfidmineraler i ét …MIT postdoc Sulata Sahu (til venstre) og kandidatstuderende Brian Chmielowiec holder en prøve af næsten rent kobber aflejret på en jernelektrode. Kredit:Denis Paiste/Material Processing Center MIT
Ren, elektrisk drevet proces til at adskille kommercielt vigtige metaller fra sulfidmineraler i ét …MIT postdoc Sulata Sahu (til venstre) og kandidatstuderende Brian Chmielowiec holder en prøve af næsten rent kobber aflejret på en jernelektrode. Kredit:Denis Paiste/Material Processing Center MIT -
 5 Brug af gæringFermentering sker, når en mikroorganisme, såsom gær eller bakterier, omdanner kulhydrater til et andet kemikalie. Det er en af de første kemiske reaktioner, mennesker har nogensinde observeret. F
5 Brug af gæringFermentering sker, når en mikroorganisme, såsom gær eller bakterier, omdanner kulhydrater til et andet kemikalie. Det er en af de første kemiske reaktioner, mennesker har nogensinde observeret. F -
 Elementer findes i husholdningsprodukterMillioner af mennesker bruger husholdningsprodukter hver dag til rengøring, skønhedsregimer, madlavning og medicinske formål. Disse er så almindelige og tilgængelige, at de fleste forbrugere tænker ik
Elementer findes i husholdningsprodukterMillioner af mennesker bruger husholdningsprodukter hver dag til rengøring, skønhedsregimer, madlavning og medicinske formål. Disse er så almindelige og tilgængelige, at de fleste forbrugere tænker ik -
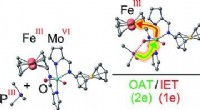 Bioinspireret enzymmodel med redox -switchKredit:Wiley Koblede oxygenoverførsler og elektronoverførselsreaktioner, der anvender kofaktorer, er enzymatiske reaktioner af afgørende betydning for alle livsformer fra bakterier til hvirveldyr.
Bioinspireret enzymmodel med redox -switchKredit:Wiley Koblede oxygenoverførsler og elektronoverførselsreaktioner, der anvender kofaktorer, er enzymatiske reaktioner af afgørende betydning for alle livsformer fra bakterier til hvirveldyr.
- Intel meddelelse blitz:Xeon Platinum 9200 er kirsebær på toppen
- Billede:Jupiter blues
- Kvantesimulator letter forskning i teoretiske supermaterialer
- Hvorfor det er godt for børn at have venner fra forskellige socioøkonomiske baggrunde
- Elon Musk-firmaet benyttede sig af at bygge Chicago højhastighedstransport
- Kvantemekanik:forviklinger i ultrakølede atomskyer


