Autonomt voksende syntetiske DNA-strenge
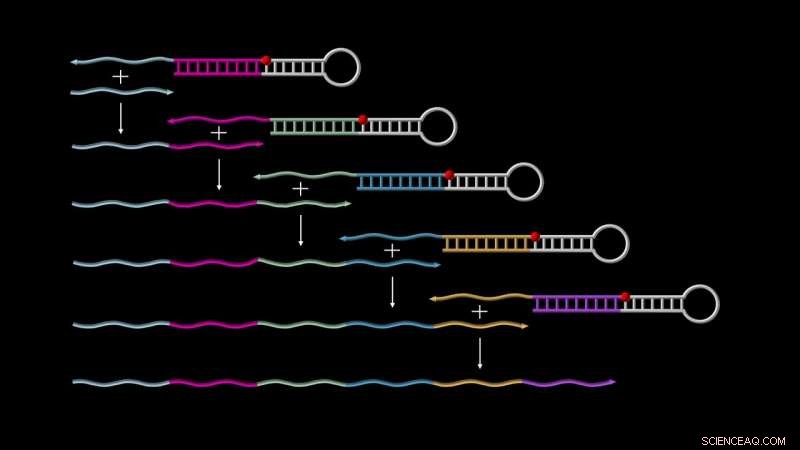
Primer Exchange Reaction (PER) kaskader muliggør autonom vækst af enkeltstrengede DNA'er. På toppen, en 'katalytisk PER-hårnål' binder en første 'primer' (vist som en kort grå streng), udløser dens forlængelse med en sekvens kodet af selve hårnålen, og frigiver den for at starte endnu en cyklus med den allerede forlængede primer, og så videre, indtil et langt udskrift er genereret. Kredit:Wyss Institute ved Harvard University
Syntetiske biologer og nanobiologer genbruger DNA, det arvelige materiale, der findes i næsten alle kroppens celler, som et smart og stabilt selvsamlende materiale til at bygge nanofabrikker, lægemiddelleverende nanostrukturer og molekylære enheder, der kan mærke deres miljø og reagere på forskellige måder ved, for eksempel, opdager betændelse i kroppen eller toksiner i miljøet. Disse applikationer i nanoskala involverer ofte syntesen af store sekvenser, der omfatter tusindvis af de byggesten, som DNA er lavet af, kendt som A, T, C og G nukleotidbaser, som kan foldes og struktureres yderligere på grund af de specifikke baseparringsevner mellem As og Ts, og Cs og Gs, henholdsvis.
Imidlertid, indtil nu, forskere har ikke værktøjer til deres rådighed, der gør det muligt for større enkeltstrengede sekvenser at vokse autonomt og derefter slutte sig til hinanden ende-til-ende efter en molekylær designplan, en kapacitet, der kunne generere strukturer og enheder med forskellige kapaciteter.
Udgivet i dag i Naturkemi , forskning af Peng Yin ved Harvard's Wyss Institute for Biologically Inspired Engineering giver en bredt anvendelig løsning på dette problem. Yin og hans team har udviklet en metode, der tillader prædesignede DNA-sekvenser autonomt at vokse og sammenkædes langs specifikke samlingsruter, giver dermed grundlaget for en ny generation af programmerbare molekylære enheder. Ved at sætte deres nye koncept med såkaldte 'Primer Exchange Reaction' (PER) kaskader på prøve, de konstruerede med succes et første sæt enheder med forskellige funktioner, såsom selvbyggende DNA-origami og DNA-nanostrukturer, der fornemmer, forstærke, registrere eller logisk evaluere miljøsignaler.
Tidligere metoder producerede identiske kopier af en fast mindre sekvens, men de er ikke i stand til at tilføje forskellige syntetiserede sekvenser til hinanden i definerede mønstre for at generere større samlinger autonomt uden brugermedieret intervention. "De autonome og programmerbare funktioner, som PER-kaskader tilbyder, kunne skabe en helt ny generation af programmerbare molekylære enheder og applikationer og lukke huller i designindsatsen, for hvilke der allerede findes mange bevægelige dele, " sagde Wyss Institute Core Faculty-medlem Peng Yin, Ph.D., der ledede undersøgelsen og er også professor i systembiologi ved Harvard Medical School (HMS). "Vi leverer proof-of-concept data for PER i en bred vifte af state-of-the-art syntetisk biologi applikationer, der klart fremhæver teknologiens brede potentiale."
Wyss Institutes team brugte det nye koncept til at designe en række sådanne PER DNA -transkripter til meget forskellige applikationer, herunder autonom syntese af store DNA-nanostrukturer kendt som DNA-origamis, og syntetisk biologi tilgange, hvor syntesen af et DNA-transkript afhænger af en trigger, såsom et kræft-associeret lille mikro-RNA. Deres PER-tilgang kan endda generere DNA-transkriptioner som følge af en logisk evalueret kombination af forskellige triggere, svarende til RNA Ribocomputing Devices, som Yins team offentliggjorde tidligere i år. Interessant nok, PER DNA-transkriptioner kan selv blive katalytiske, at være i stand til at skære et vilkårligt mål-RNA, bliver fluorescensmærkede prober, der forstærker tilstedeværelsen af en bestemt molekylær stimulus, eller "molekylære optagere", der trofast angiver den rækkefølge, hvor bestemte molekylære signaler vises i deres miljøer.
For at starte PER-kaskaden, to grundlæggende komponenter er nødvendige. Den ene kaldes en "katalytisk DNA-hårnålsformidler", som er et enkeltstrenget DNA-molekyle, der delvist parrer sig med sig selv for at danne en hårnålestruktur med en kort overhængende enkeltstreng. Dette udhæng er designet til at fange PER-kaskadernes anden komponent, "primeren, " som indeholder en region, der er komplementær til overhænget. Gennem en række forlængelses- og forskydningsreaktioner, primeren forlænges med en sekvens leveret af den katalytiske hårnålemediator og udstødes derefter. Dette frigør den katalytiske hårnålemediator til at kaskadere den næste runde af processen, enten ved at fange en ny startprimer eller den allerede aflange primer – og så videre.
Disse komplekse syntesestier forløber autonomt, sammenlignes med en molekylær robot, der udfører en given opgave, og ved en enkelt temperatur, hvilket gør teknologien meget robust. "Tilgangen giver os en enorm kreativ frihed:vi kan ikke kun syntetisere det samme stykke DNA igen og igen som nye tilføjelser af en voksende sekvens, men vi kan også variere typerne af DNA-sekvenser, der skal tilføjes, blot ved at ændre sammensætningen af katalytiske hårnåle-DNA'er og primere i blandingen, mens samlingen er i gang. Dette giver os mulighed for at få syntesen til at forgrenes i forskellige retninger og indvikle indviklet sammensætningen af det endelige DNA -transkript, " sagde undersøgelsens første forfatter Jocelyn Kishi, der som National Science Foundation (NSF) Graduate Research Fellow ved HMS arbejder på Yins Wyss Institute-team. "Vi arbejder nu på at implementere PER-kaskader til en række forskellige applikationer, herunder molekylære optagere, sofistikeret diagnostik, og billeddannelse af væv. Vi håber også, at disse systemer en dag kan bruges i levende celler som enheder, der kan optage hændelser eller omprogrammere celleadfærd på bestemte måder, " sagde Kishi.
"Dette nye fremskridt, der viser, hvordan DNA-molekyler kan programmeres til selv at samle sig i specifikke 3D-strukturer og udføre foruddefinerede funktioner og opgaver, repræsenterer et stort skridt fremad inden for Molecular Robotics, og giver et indblik i fremtiden for enheder til både medicinske og ikke-medicinske applikationer, " sagde Wyss Institutes stiftende direktør Donald Ingber, M.D., Ph.D., som også er Judah Folkman-professor i vaskulær biologi ved HMS og Vascular Biology Program på Boston Children's Hospital, samt professor i bioingeniør ved Harvard John A. Paulson School of Engineering and Applied Sciences (SEAS).
 Varme artikler
Varme artikler
-
 Lifes byggesten observeret i rumlignende omgivelserLavenergi-elektronpåvirkning formidler skabelsen af nye komplekse organiske molekyler, såsom ethanol, i astrofysiske/planetariske modelis indeholdende metan og ilt; mens nogle af de nye arter desorb
Lifes byggesten observeret i rumlignende omgivelserLavenergi-elektronpåvirkning formidler skabelsen af nye komplekse organiske molekyler, såsom ethanol, i astrofysiske/planetariske modelis indeholdende metan og ilt; mens nogle af de nye arter desorb -
 Forskere opdager stabilitet i hybride fotoelektriske nanomaterialerFig. 1. En computermodel af kulstofnanorør dækket af phthalocyaniner. Kredit:Pavel Krasnov Et hold af sibiriske forskere og udenlandske kolleger beregnede de parametre, der påvirker intensiteten a
Forskere opdager stabilitet i hybride fotoelektriske nanomaterialerFig. 1. En computermodel af kulstofnanorør dækket af phthalocyaniner. Kredit:Pavel Krasnov Et hold af sibiriske forskere og udenlandske kolleger beregnede de parametre, der påvirker intensiteten a -
 Vaccineingredienser kan gemme sig i små molekylebibliotekerForskerne fandt et molekyle, der kan bruges som vaccineadjuvans og styrker immunresponset, når det tilsættes en vaccine. Kredit:Mindy Takamiya/Kyoto University iCeMS Mange vacciner indeholder ingr
Vaccineingredienser kan gemme sig i små molekylebibliotekerForskerne fandt et molekyle, der kan bruges som vaccineadjuvans og styrker immunresponset, når det tilsættes en vaccine. Kredit:Mindy Takamiya/Kyoto University iCeMS Mange vacciner indeholder ingr -
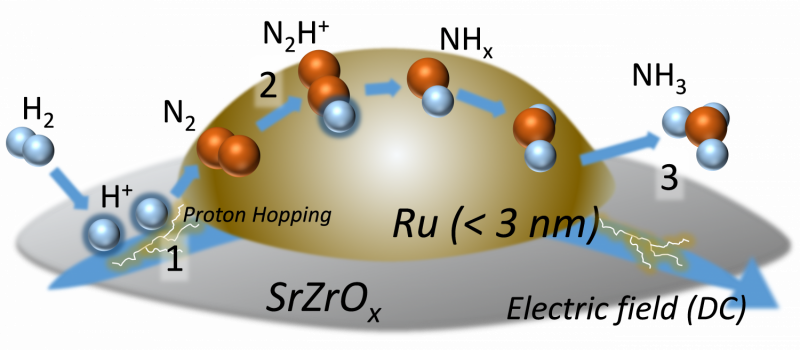 Ammoniak on-demand? Alternativ produktionsmetode for en bæredygtig fremtidProtonhopping spiller en vigtig rolle i reaktionen, da det aktiverer nitrogengas selv ved lave temperaturer og modererer de skrappe tilstandskrav. Kredit:Waseda University Vores samfund har mere e
Ammoniak on-demand? Alternativ produktionsmetode for en bæredygtig fremtidProtonhopping spiller en vigtig rolle i reaktionen, da det aktiverer nitrogengas selv ved lave temperaturer og modererer de skrappe tilstandskrav. Kredit:Waseda University Vores samfund har mere e
- Det tager år at komme sig helt efter store storme som Sandy
- Forskelle mellem polar og nonpolar i kemi
- Bayer står over for nyt maraton efter den enorme Monsanto-fusion
- Drik ikke og drøn, siger japanske parlamentsmedlemmer
- Forskere foreslår nano-indeslutningsstrategi for at danne sub-nanometer-reaktorer
- Havopvarmning har fiskeri på farten, hjælper nogle, men gør mere ondt


