Cellemembran som materiale til knogledannelse
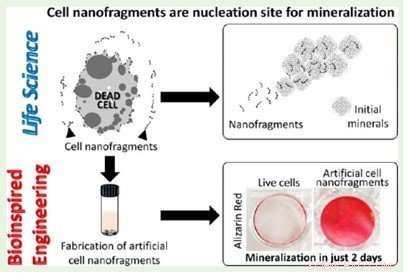
Forståelse af biologiske fænomener fra en tværfaglig tilgang muliggør udvikling og optimering af bioinspirerede materialer. Kredit:Bioinspired Engineering
Udbruddet af celler, der danner brusk, er forbundet med mineralisering i de tidlige stadier af knogledannelse, og nanofragmenter af cellemembranerne kan fungere som kernedannelsessteder for amorft calciumphosphat, som rapporteret i to undersøgelser, der netop er offentliggjort i Integrativ biologi og ASC Biomaterials Science and Engineering .
Brusk har en meget vigtig stilladslignende funktion for udviklingen af knogler; under endokondral ossifikation, chondrocytterne, cellerne, der danner brusk, udskiller matrixproteiner og mineraliseringsfaktorer, der optimerer miljøet for mineralisering. Mekanismerne for knogledannelse er ikke fuldstændigt belyst, og at manipulere mineralisering er udfordrende endnu. At få kontrol over denne proces er relevant, da det ville resultere i forbedrede bioingeniørteknikker til syntese og rekonstruktion af bruskvæv, og til kontrol af knogledannelse.
For at få yderligere forståelse i de indledende trin med mineraldannelse, Professor Takuya Matsumoto og adjunkt Emilio Satoshi Hara fra Okayama University Graduate School of Medicine, Tandpleje og farmaceutiske videnskaber studerede knogledannelse i lårbenets epifyse (dvs. den afrundede ende af knoglen) hos mus under sekundær ossifikation i de første postnatale dage.
I en første undersøgelse, forskerne observerede, at chondrocytter brister nær det mineraliserede område, som de foreslår kan være en pladsskabende mekanisme til mineralekspansion. Det rum, der blev skabt efter celleudbruddet, stemmer faktisk godt overens med det, der senere blev optaget af mineralerne i slutningen af processen, som demonstreret ved time-lapse-billeder af den indledende knogledannelsesproces. For at demonstrere sammenhængen mellem burst og mineraldannelse og ekspansion, Professor Matsumoto og kolleger brugte eksterne stimuli til at fremkalde burst og manipulere knoglevævsdannelse. I særdeleshed, to eksterne faktorer var forbundet med at udløse eksplosionen:mekanisk og osmotisk tryk. Ja, ex-vivo kultur af lårbenets epifyse i hypotonisk tilstand eller under mekanisk trykforbedret mineraldannelse, og in-vivo undersøgelser af mekanisk tryks rolle viste, at reduceret tryk på leddene resulterer i undertrykt knogledannelse i lårbenets epifyse.
I den forskning, der blev præsenteret i det andet papir, forskerne brugte en række forskellige teknikker til at observere de dynamiske ændringer i organisk og uorganisk materiale i brusken på en tids- og stadiespecifik måde, bekræfter, at de tidlige trin af mineralisering er baseret på aktiviteten af chondrocytter. En omhyggelig analyse af nanofragmenter observeret nær det mineraliserede område afslørede, at de var nanofragmenter af chondrocytmembran, og kunne være kernedannelsessteder for amorft calciumphosphat, som derefter transformerede til apatitkrystaller. Phospholipiderne i fragmenterne kunne tilvejebringe det nødvendige fosfat til denne proces. Forskerne syntetiserede også kunstige celle -nanofragmenter, og viste, at de fremmer mineraldannelse in vitro.
Kontrol af chondrocytudbrud ved hjælp af eksterne stimuli kan resultere i nye tilgange til brusk- og knoglevævsmanipulation. I øvrigt, fordi cellemembran -nanofragmenter tilvejebringer nukleationssteder for mineraldannelse, disse kunne bruges til at manipulere biomineralisering, som forfatterne kommenterer:"manipulation af chondrocytsprængninger med eksterne mekano-kemiske stimuli kunne være en yderligere tilgang til brusk- og knoglevævsmanipulation, "og" i fremtiden, cellemembranfragmentbaserede materialer kan også udvikles og anvendes i knoglevævsteknik og regenerering ".
Der er to typer af forbeningscentre, primær og sekundær. Primært ossifikationscenter vises under prænatal udvikling, der henviser til, at sekundært ossifikationscenter vises i postnatal- og ungdomsårene. I lange knogler, det primære ossifikationscenter forekommer i den centrale del af knoglen, det sekundære ossifikationscenter i enderne.
To processer resulterer i dannelsen af knoglevæv:i intramembranøs ossifikation, knogle lægges direkte ned i det primitive bindevæv. Ved endokondral ossifikation, den der blev undersøgt i forskningen diskuteret her, brusk fungerer som en forløber, og nedbrydes gradvist og erstattes af knogle.
Fordi denne forskning afslører to måder at fremkalde burst af chondrocytter (som igen styrer knogledannelse ved at give plads til mineraliseret væv), ved hjælp af mekanisk og osmotisk tryk, det åbner vejen til nye metoder til at konstruere knoglevæv. Afsløringen af membranfragmenters rolle som nukleationscentre for knogledannelse giver en ny vej til udvikling af biomaterialer til knoglevævsteknik og regenerering. Begge resultater åbner nye muligheder for bioingeniør af knoglevæv.
Sidste artikelDatabase for steganalyse af retsmedicinsk bevis
Næste artikelLysaktiverede kræftlægemidler uden toksiske bivirkninger
 Varme artikler
Varme artikler
-
 Dyrkning af HCA -krystallerKredit:ESS/Fisher Zoë Fisher og Katarina Koruza fra ESS Deuteration and Macromolecular Crystallization (DEMAX) Support lab og Lunds Universitet har brugt dampdiffusionsmetoder til at dyrke store p
Dyrkning af HCA -krystallerKredit:ESS/Fisher Zoë Fisher og Katarina Koruza fra ESS Deuteration and Macromolecular Crystallization (DEMAX) Support lab og Lunds Universitet har brugt dampdiffusionsmetoder til at dyrke store p -
 Sådan forhindrer du rust med belægningerFerrometaller som jern og stål kan oxideres til dannelse af rust. Dette svækker metalet og kan forårsage fejl i delen. For at undgå rust og korrosion kan en række forskellige belægninger påføres metal
Sådan forhindrer du rust med belægningerFerrometaller som jern og stål kan oxideres til dannelse af rust. Dette svækker metalet og kan forårsage fejl i delen. For at undgå rust og korrosion kan en række forskellige belægninger påføres metal -
 Hvad er tilskuerioner?Tilskuereioner er ioner, der findes i en opløsning, men ikke deltager i en opløsnings kemiske reaktion. Når reaktanter dissocieres til ioner, kan nogle af ionerne kombineres og danne en ny forbindelse
Hvad er tilskuerioner?Tilskuereioner er ioner, der findes i en opløsning, men ikke deltager i en opløsnings kemiske reaktion. Når reaktanter dissocieres til ioner, kan nogle af ionerne kombineres og danne en ny forbindelse -
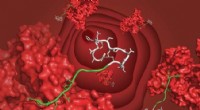 En ny ligand forlænger halveringstiden for peptider fra minutter til dageEt bicyklisk peptid (hvidt) bundet til serumalbumin (rødt) gennem den nyudviklede ligand (grøn), flyder i blodbanen. Kredit:C. Heinis/EPFL EPFL-forskere har udviklet et ligandmolekyle, der forbind
En ny ligand forlænger halveringstiden for peptider fra minutter til dageEt bicyklisk peptid (hvidt) bundet til serumalbumin (rødt) gennem den nyudviklede ligand (grøn), flyder i blodbanen. Kredit:C. Heinis/EPFL EPFL-forskere har udviklet et ligandmolekyle, der forbind
- Suomi NPP satellit spotter Lidia forsvinde
- Ingeniører finder, at antioxidanter forbedrer nanoskala visualisering af polymerer
- En kæde i Mælkevejen forbundet med galaktisk kollision
- Sådan laver du en regnbue i en flaske
- SoftBank-fonden investerer stort i selvkørende leverancer
- Røntgenøjne kigger dybere ind i dødbringende patogen


