Forudsigelse af udfaldet af våbenkapløbet mellem mennesker og bakterier
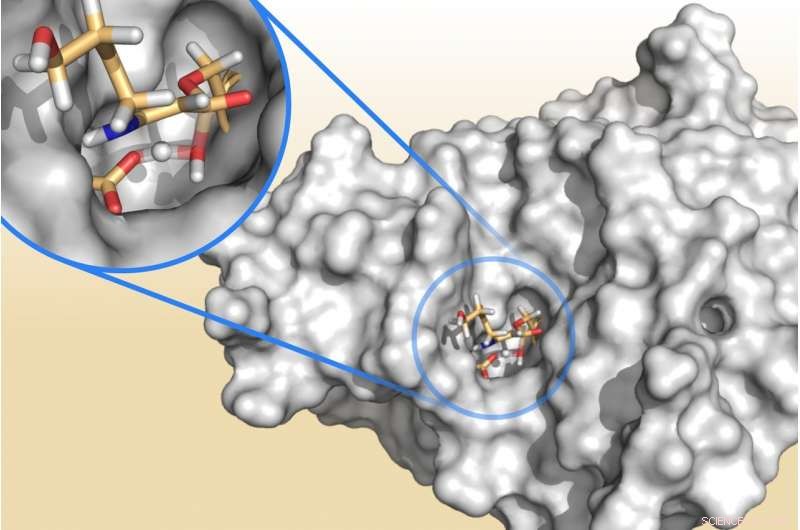
Et bakterieenzym, der frigiver fragmenter af clavulansyre, en "resistensblokker" designet til at overvinde antibiotikaresistente infektioner. Destruktion af clavulansyre gør det muligt for enzymet at beskytte bakterier mod virkningerne af antibiotika. Kredit:Marc van der Kamp
Gennem computersimuleringer, forskere kan forudsige, om bakterier kan stoppes med populære antibakterielle terapier eller ej - et gennembrud, som vil hjælpe med at udvælge og udvikle effektive behandlinger for bakterielle infektioner.
Stigende resistens over for antibiotika er en af de alvorligste globale sundhedstrusler, vi står over for. Der er et presserende behov for at udvikle nye antibiotika, der er omkostningseffektive, da det anslås, at i 2050, 10 millioner liv om året vil være i fare for antibiotika-resistente infektioner. I et forsøg på at hjælpe med at tackle denne udfordring, forskere ved University of Bristol har udviklet computersimuleringer, som kan være nøglen til at komme videre i det igangværende 'våbenkapløb' med bakterier.
Forskere fokuserede på enzymer i bakterier, der kan splitte strukturen af antibiotika af penicillin-typen, fører til modstand. For at genoprette effektiviteten af disse antibiotika, 'resistensblokerende' molekyler er blevet udviklet til at blokere aktiviteten af disse enzymer. Ved at behandle patienter med de rigtige kombinationer af antibiotika og resistensblokkere, læger er i stand til at få overtaget i kampen. Desværre, bakterier kan lave mange forskellige enzymer i stand til at ødelægge penicilliner, og tilgængelige modstandsblokkere virker kun mod nogle af disse.
Nye fund, udgivet i Biokemi , vise, at det nu er muligt at bruge computersimuleringer til at forudsige, om disse modstandsblokkere vil være effektive eller ej. Det er håbet, at denne information vil hjælpe videnskabsmænd med at udvikle forbedrede resistensblokkere, som kan genoprette virkningen af populære antibiotika mod en bredere vifte af resistente bakterier.
Ved hjælp af en computersimuleringsteknik kaldet QM/MM (kvantemekanik/molekylærmekaniksimuleringer) var Bristol-forskerholdet i stand til at få et molekylært indblik i, hvordan resistensenzymer reagerer med resistensblokkere.
Forskere fokuserede specifikt på clavulansyre, et lægemiddel, der forhindrer ødelæggelse af almindelige penicillinlignende antibiotika. Clavulansyre bruges almindeligvis i kombination med antibiotikummet amoxicillin til behandling af øre, bihule- og urinvejsinfektioner (co-amoxiclav). Nogle sådanne bakterielle infektioner, imidlertid, bliver meget vanskeligere at behandle, fordi clavulansyre ikke virker effektivt mod de enzymer, de producerer.
QM/MM-simuleringerne undersøgte, hvordan clavulansyre interagerer med disse bakterielle enzymer og afslørede det vigtigste trin i at bestemme, om enzymet er effektivt blokeret. Et enzym, der ikke kan stoppes, frigiver et nedbrudt molekyle af clavulansyre og fortsætter med at nedbryde det antibiotikum, som det administreres med, resulterer i antibiotikaresistens. Hvis nedbrydningen af clavulansyre tager lang tid, så bliver enzymet "tilstoppet" og er ude af stand til at nedbryde antibiotikaen, som derefter kan dræbe bakterien og rydde infektionen.
Dr. Marc van der Kamp, fra Bristol University's School of Biochemistry, sagde:
"Vi er spændte på at se, hvordan vores computersimuleringer i fremtiden kan bruges til at teste enzymer fra bakterier og forudsige, hvornår en resistensblokerende hæmmer vil være effektiv.
Vi håber, at dette vil identificere, hvordan vi bedre kan blokere sådanne bakterielle enzymer, så antibiotika kan bruges effektivt til behandling af lægemiddelresistente infektioner.
Vores simuleringer kan også være et værdifuldt værktøj til at hjælpe med at vælge, hvilke kombinationer af lægemidler der er bedst til behandling af et bestemt infektionsudbrud, giver os mulighed for at være bedre rustet i dette 'våbenkapløb' med bakterier."
Sidste artikelUber medicin levering til kræftpatienter
Næste artikelSupramolekylær kompleksdannelse - anthracen makrocyklus og C60 fulleren
 Varme artikler
Varme artikler
-
 Et nyt antibiotisk bindingssted fundet i ribosometKredit:CC0 Public Domain En gruppe videnskabsmænd fra Rusland, Tyskland og USA, ledet af Skoltech-forskerne Ilya Osterman, Petr Sergiev, Olga Dontsova og Daniel Wilson fra Hamborg Universitet, har
Et nyt antibiotisk bindingssted fundet i ribosometKredit:CC0 Public Domain En gruppe videnskabsmænd fra Rusland, Tyskland og USA, ledet af Skoltech-forskerne Ilya Osterman, Petr Sergiev, Olga Dontsova og Daniel Wilson fra Hamborg Universitet, har -
 Aktivering af prodrug ved hjælp af proteinindkapslet guldkatalysatorKredit:CC0 Public Domain Som en del af deres bestræbelser på at udtænke måder at minimere bivirkningerne af lægemidler til behandling af kræft, fire RIKEN-kemikere har fundet en biokompatibel måde
Aktivering af prodrug ved hjælp af proteinindkapslet guldkatalysatorKredit:CC0 Public Domain Som en del af deres bestræbelser på at udtænke måder at minimere bivirkningerne af lægemidler til behandling af kræft, fire RIKEN-kemikere har fundet en biokompatibel måde -
 Udførelse af kemi i flydende dråberKredit:California Institute of Technology Kunne kemikere være klar til at droppe det ærværdige reagensglas, selve symbolet på kemi i mange menneskers sind? Måske ikke helt endnu men Caltechs Jack
Udførelse af kemi i flydende dråberKredit:California Institute of Technology Kunne kemikere være klar til at droppe det ærværdige reagensglas, selve symbolet på kemi i mange menneskers sind? Måske ikke helt endnu men Caltechs Jack -
 Ledende skal for bakterierKredit:Wiley Under anaerobe forhold, visse bakterier kan producere elektricitet. Denne adfærd kan udnyttes i mikrobielle brændselsceller, med særligt fokus på spildevandsbehandlingsordninger. Et s
Ledende skal for bakterierKredit:Wiley Under anaerobe forhold, visse bakterier kan producere elektricitet. Denne adfærd kan udnyttes i mikrobielle brændselsceller, med særligt fokus på spildevandsbehandlingsordninger. Et s
- Mars-missionsastronauter øver sig på vandlandinger ud for Texas
- Varmerelaterede dødsfald vil sandsynligvis stige betydeligt, efterhånden som de globale temperatur…
- Hvordan man identificerer en kobberhoved Vs. en mælke slange
- Klasseværelsesaktiviteter efter den videnskabelige metode
- Piraten i den sydlige himmel
- Kolloide quantum dot fotodetektorer kan nu se længere end før


