Kemikere lærer et enzym et nyt trick, med potentiale til at bygge nye molekyler

Todd Hysters forskergruppe ved Princeton University har fundet en måde at få et naturligt forekommende enzym til at antage et nyt, kunstig rolle. Fra venstre:David Miller, postdoktor; Kyle Biegasiewicz, postdoktor; Todd Hyster, adjunkt i kemi, holder en 3D-trykt model af enzymet; Megan Emmanuel, kandidatstuderende; Simon Cooper, kandidatstuderende. Kredit:C. Todd Reichart, Institut for Kemi
Princeton -kemikere har fundet en måde at få et naturligt forekommende enzym til at antage et nyt, kunstig rolle, som har betydelige konsekvenser for moderne kemi, herunder farmaceutisk produktion. Deres arbejde fremgår af journalen Naturkemi .
"Vi har fundet en helt ny måde at få enzymer til at udføre en ikke-naturlig reaktion, "sagde Todd Hyster, en adjunkt i kemi. "Et traditionelt perspektiv siger, at enzymer kun vil gøre én ting. Dette papir viser, at dette måske ikke er sandt for alle enzymer. Endnu vigtigere er, strategien beskrevet i dette papir kan potentielt anvendes på andre enzymfamilier, hvilket betyder, at vi vil kunne bruge denne fremgangsmåde til at opfinde helt nye enzymatiske reaktioner. Jeg tror, at dette har potentiale til at ændre måden, vi bygger molekyler på. "
Enzymer er naturens katalysatorer, nøglerne til at få kritiske biokemiske reaktioner til at ske hurtigt nok til at opretholde livet. Organiske kemikere har udnyttet dette i over 100 år, men indtil nu, deres anvendelse har været begrænset, da individuelle enzymer ofte kun er i stand til at katalysere en enkelt reaktion.
Nu, forskerne i Hysters laboratorium har fjernet et enzym fra dets naturlige omgivelser, tilføjet et par nye ingredienser, og det lykkedes at få det til at katalysere en anden type kemisk reaktion - hvor det fungerede overraskende godt.
"Todd afdækker skjulte evner i biologiens enorme repertoire af kemi, hvoraf nogle måske ikke er nyttige til biologi, men vil være meget nyttige for os, "sagde Frances Arnold, Linus Pauling -professor i kemiteknik, Bioingeniør og biokemi ved California Institute of Technology, som ikke var involveret i denne undersøgelse.
"Han viser, at enzymer er i stand til mange bedrifter, "sagde Arnold, der tog eksamen fra Princeton i 1979. "Alt du skal gøre er at stille de rigtige spørgsmål."
Nøglen var at forenkle deres forståelse af, hvordan et enzym katalyserer en reaktion, Sagde Hyster.
"Jeg tror, jeg altid er overrasket over, at vores forenklede tilgang til enzymkatalyse faktisk virker, "Sagde Hyster." Som studerende, vi lærer, at enzymer er utrolig komplicerede og specifikke katalysatorer. ... hver gang vi opdager, at de er i stand til at gøre noget helt nyt, som naturen aldrig havde til hensigt, det er overraskende og spændende. "
I deres reaktion, forskerne tilføjede en lille mængde af et nøje udvalgt fotoexcitabelt farvestof til enzymet og oversvømmede det med grønt lys. Derved, de samlede to normalt uafhængige grene af kemi, bemærkede Kyle Biegasiewicz, en postdoc forsker i Hysters laboratorium og en af to co-first-forfattere på papiret.
"Vi har opdaget et utroligt spændende ægteskab mellem enzymatisk katalyse (biokatalyse) og fotoredoks katalyse, "Sagde Biegasiewicz.
Til kemikere, at få mere af den reaktion, du ønsker, og mindre af en reaktion, du ikke gør, er kendt som "selektivitet". Enzymer er meget mere "selektive" end de fleste små molekylkatalysatorer, og denne nye teknik gør det muligt for forskere at udnytte det til deres egne ønskede reaktioner. "Væsentligt, denne nye transformation viser høje niveauer af selektivitet for en klasse af reaktioner, der tidligere var meget vanskelige at kontrollere, "Sagde Hyster.
I det væsentlige, deres gennembrud giver mulighed for en ny "plug-and-play" tilgang, ved hjælp af enzymer til at aktivere ny katalytisk reaktivitet, som har mange spændende konsekvenser, Sagde Biegasiewicz. "Selvom jeg ikke kan give nogen detaljer om igangværende projekter i gruppen, Jeg vil informere det syntetiske samfund om at følge med - de nyeste ting er virkelig fede! "
Denne nye opdagelse er et andet aspekt af det synlige lys fotokatalyse, der transformerer moderne kemi, Sagde Hyster.
"Katalysefeltet er blevet revolutioneret i det sidste årti ved at udvikle metoder, der bruger lys, "sagde han." Princeton har virkelig været en chauffør i dette område. Princeton kemiprofessorer [David] MacMillan, [Abigail] Doyle og [Robert] Knowles bruger alle lys til at gøre virkelig utrolige ting ved hjælp af små molekylkatalysatorer. Vi har vist, at lysets anvendelighed ikke er begrænset til små molekylkatalysatorer; det kan også udvide de typer ting, vi kan gøre med enzymer. Det synes jeg er ret pænt. "
Ideen til denne forskningsvej kom fra at følge "brødkrummerne" i tidligere forskning, sagde Simon Cooper, en kandidatstuderende i Hysters laboratorium og en co-first-author på papiret. Andre forskere havde demonstreret, at udsættelse for ultraviolet lys forårsagede en betydelig ændring i adfærden hos et rigeligt molekyle, nicotinamid adenin dinucleotidphosphat (NADPH), som Hysters team tilføjede til enzymet sammen med det lysfølsomme farvestof.
"Når det udsættes for UV -lys, NADPH kan skifte fra at overføre to elektroner og en proton i et enkelt trin til at overføre først en elektron og derefter et hydrogenatom (en elektron og en proton), "Sagde Cooper." Vi troede, at hvis vi kunne drage fordel af denne nye vej inde i et enzym, værdifulde nye reaktioner ventede på opdagelse. ... Det vigtigste aspekt af fundene i dette papir er at kontrollere overførslen af et hydrogenatom for kun at skabe en af to mulige spejlbilledformer af et molekyle. Denne type valg mellem to spejlbilledformer har traditionelt været meget vanskelig at opnå for overførsel af et hydrogenatom, og metoderne beskrevet her er en løsning på denne udfordring. "
Cooper tilføjede:"Når vi går videre i det 21. århundrede, hvis en voksende verdensbefolkning skal opleve bekvemmelighederne ved det, vi tager for givet i den udviklede verden, vi får brug for mere omkostningseffektive og bæredygtige former for kemisk katalyse for at levere mange af de produkter, der kan tilskrives den moderne livsstil. Metoderne beskrevet i vores papir vil begynde at bane vejen, måske."
"Vores kemi kan synes at være niche eller esoterisk, men disse eksempler tjener kun som bevis-på-koncept for, hvad der kan blive stærke metoder til at lave nye molekyler, der kan have en håndgribelig samfundsmæssig indvirkning:lægemidler, landbrugskemikalier, dufte og listen fortsætter, "sagde Megan Emmanuel, en kandidatstuderende i Hysters laboratorium og en medforfatter på papiret. "Betydningen af, at vores arbejde kan en dag, bruges til at yde meningsfulde bidrag til menneskers liv er spændende. "
Papiret, "Katalytisk promiskuitet aktiveret ved fotoredox-katalyse i nicotinamidafhængige oxidoreduktaser" af Kyle Biegasiewicz, Simon Cooper, Megan Emmanuel, David Miller og Todd Hyster, blev offentliggjort i Naturkemi den 11. juni, 2018.
 Varme artikler
Varme artikler
-
 Uventet ny dynamik for store DNA -molekyler i flydende suspensionKredit:CC0 Public Domain Polymerfysikere ved University of Massachusetts Amherst rapporterer i dag om den uventede og tidligere ukendte opførsel af et ladet makromolekyle, såsom DNA indlejret i en
Uventet ny dynamik for store DNA -molekyler i flydende suspensionKredit:CC0 Public Domain Polymerfysikere ved University of Massachusetts Amherst rapporterer i dag om den uventede og tidligere ukendte opførsel af et ladet makromolekyle, såsom DNA indlejret i en -
 Forskere skaber brintbrændstof fra havvandEn prototype -enhed brugte solenergi til at skabe brintbrændstof fra havvand. Kredit:H. Dai, Yun Kuang, Michael Kenney Stanford -forskere har udtænkt en måde at generere brintbrændstof ved hjælp a
Forskere skaber brintbrændstof fra havvandEn prototype -enhed brugte solenergi til at skabe brintbrændstof fra havvand. Kredit:H. Dai, Yun Kuang, Michael Kenney Stanford -forskere har udtænkt en måde at generere brintbrændstof ved hjælp a -
 Undersøgelse detaljerede regulering af en multi-drug transporter(venstre mod højre):Reza Dastvan, Ph.d., Smriti Mishra, Ph.d., og Hassane Mchaourab, Ph.d., studerer den indre funktion af en proteinpumpe, der bidrager til kemoterapiresistens mod kræft. Kredit:Vande
Undersøgelse detaljerede regulering af en multi-drug transporter(venstre mod højre):Reza Dastvan, Ph.d., Smriti Mishra, Ph.d., og Hassane Mchaourab, Ph.d., studerer den indre funktion af en proteinpumpe, der bidrager til kemoterapiresistens mod kræft. Kredit:Vande -
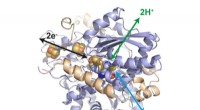 Enzymsystem til brintindustrienStruktur af hydrogenasen fra Desulfovibrio desulfuricans. I sit aktive center, en jern-svovl-klynge katalyserer oxidation af hydrogen til protoner samt reduktion af protoner til hydrogen. Yderligere j
Enzymsystem til brintindustrienStruktur af hydrogenasen fra Desulfovibrio desulfuricans. I sit aktive center, en jern-svovl-klynge katalyserer oxidation af hydrogen til protoner samt reduktion af protoner til hydrogen. Yderligere j
- Den første AI-universsim er hurtig og præcis - og dens skabere ved ikke, hvordan den fungerer
- NASA sender grønt lys til SpaceX-besætningskapseltest til ISS
- Forskere afslører et fuldstændigt fysisk scenarie med sympatisk udbrud af to solfilamenter
- Undersøgelse viser, at integrerede økologiske afgrøde- og husdyrproduktionssystemer kan overholde…
- Banebrydende kemi tilgang kunne føre til mere robust blød elektronik
- At se stivelse:Ny teknik muliggør skånsom observation af biobrændstofmaterialer


