Superopløsningsmikroskopi:Kommer endnu tættere på grænsen
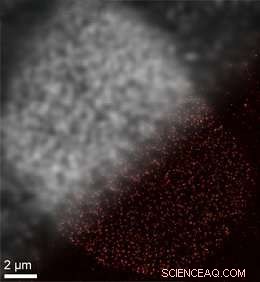
SOMAmer-baseret DNA-PAINT superopløsningsmikroskopi muliggør forbedret rumlig opløsning. Øverst til venstre:Traditionelt diffraktionsbegrænset billede af nuklear porekompleksproteiner på en nuklear cellemembran. Nederst til højre:DNA-PAINT superopløsningsbillede opnået med SOMAmer-bindere. Kredit:Jungmann/LMU
Ralf Jungmann er interesseret i processer, der foregår inden for utroligt små rumlige dimensioner. Jungmann har et professorat i eksperimentel fysik ved Ludwig-Maximilians-Universitaet (LMU) i München, og leder en forskningsgruppe i molekylær billeddannelse og bionanoteknologi ved Max Planck Institute for Biochemistry (Martinsried), og fokuserer på at udvide mulighederne for optisk mikroskopi. Hans mål er at visualisere de molekylære interaktioner, der finder sted i individuelle celler. For at overvåge proteinnetværkene involveret i sådanne processer, han bruger korte DNA-strenge kovalent bundet til forskellige fluorescensmarkører som prober til at lokalisere målproteiner, der bærer komplementære DNA-mærker. Ved at udnytte sekvensspecificiteten og alsidigheden af DNA-hybridisering, det er muligt at afbilde fordelingen af et stort antal molekyler i enkelte celler i superopløsning. Kombinationen af DNA-sekvenser med forskellige fluorescerende forbindelser forklarer, hvorfor teknikken bærer navnet DNA-PAINT.
En af de største begrænsninger for potentialet for super-opløsningsfluorescensmikroskopi har at gøre med de markører, der anvendes til at påvise mål af biologisk interesse - de er simpelthen for store. "Vi arbejder med en instrumentel opløsning på mindre end 10 nanometer. Men de fluorescerende etiketter, der konventionelt bruges til at mærke proteiner, er meget større end det. Og denne faktor har hæmmet udviklingen af hele dette forskningsfelt, " forklarer Jungmann. Det er det, der motiverede arbejdet beskrevet i en ny undersøgelse, som står i journalen Naturens metoder . I denne avis, Jungmann og hans kolleger udforsker brugen af det, der kaldes SOMAmers, en særlig klasse af DNA-aptamerer, som et middel til at reducere de markører, der bruges i DNA-PAINT. Udtrykket 'aptamer' blev oprindeligt opfundet for at henvise til enkeltstrengede RNA-molekyler, der foldes til definerede tredimensionelle former og er i stand til specifikt at detektere unikke proteinarter. Jungmanns aptamerer er enkeltstrengede DNA-molekyler, som foldes til definerede tredimensionelle former, der kan binde direkte til specifikt målrettede proteiner.
"Den ideelle etiket, der bruges til at mærke proteiner effektivt og specifikt skal opfylde flere kriterier, " siger Sebastian Strauss, medlem af Jungmanns gruppe og førsteforfatter til den nye undersøgelse. "Det skal være så lille som muligt, og det bør binde sig til mål støkiometrisk for at muliggøre præcis kvantificering. Ud over, det ville være ideelt at syntetisere hele biblioteker af disse forbindelser og hurtigt identificere egnede markører for proteinerne af interesse. For at vurdere potentialet af DNA-aptamerer, LMU-teamet samarbejdede med det amerikanske firma SomaLogic, som allerede havde designet, til andre formål, et stort udvalg af modificerede aptamerer (SOMAmerer), der specifikt kan binde tusindvis af forskellige proteiner. I den nye undersøgelse, forskerne fra München modificerede et udvalg af disse aptamerer til DNA-PAINT og udviklede effektive mærkningsprotokoller for fikserede celler og livceller. Den nuværende undersøgelse viser, at det faktisk er muligt at forbedre den opløsning, der kan opnås med konventionelle fluorescensmærker ved at bruge disse nye mærkningsreagenser i kombination med DNA-PAINT super-opløsningsmikroskopi.
"Vi forventer, at den nye metode vil give et markant løft til superopløsningsmikroskopi, især med hensyn til dets anvendelsesområde inden for biologi, " siger Ralf Jungmann. Hans mål er at bruge DNA-PAINT til samtidigt at visualisere og overvåge så mange proteiner og deres interaktioner som muligt. I fremtidige eksperimenter planlægger han og hans kolleger at bruge den nye mærkningsmetode til at afbilde hele proteinnetværk i høj opløsning. "Vi vil være i stand til at løse biologiske og biomedicinske spørgsmål, som hidtil har været eksperimentelt utilgængelige."
Sidste artikelOmdannelse af kuldioxid
Næste artikelBærbar ferskvandshøster kunne trække op til 10 gallons i timen fra luften
 Varme artikler
Varme artikler
-
 Studie baner vejen for nye lysfølsomme materialerAvisens forfattere, der arbejder i laboratoriet:Lauren Heald, Scott Sayres, Jake Garcia. Kredit:Biodesign Institute ved Arizona State University Fotokatalysatorer er nyttige materialer, med et uta
Studie baner vejen for nye lysfølsomme materialerAvisens forfattere, der arbejder i laboratoriet:Lauren Heald, Scott Sayres, Jake Garcia. Kredit:Biodesign Institute ved Arizona State University Fotokatalysatorer er nyttige materialer, med et uta -
 Enkel metode til omdannelse af carboxylsyrer til boronatestere og boronsyrerKredit:(c) Videnskab (2017). DOI:10.1126/science.aam7355 (Phys.org) – Et team af forskere fra Scripps Research Institute har udviklet en enkel, praktisk metode til omdannelse af carboxylsyrer ti
Enkel metode til omdannelse af carboxylsyrer til boronatestere og boronsyrerKredit:(c) Videnskab (2017). DOI:10.1126/science.aam7355 (Phys.org) – Et team af forskere fra Scripps Research Institute har udviklet en enkel, praktisk metode til omdannelse af carboxylsyrer ti -
 Undersøgelse kaster nyt lys over produktionen af hydroxylradikaler, som hjælper med at nedbryde …Et forskerhold, der omfattede Argonne-kemikeren Stephen Klippenstein, undersøgte produktionen af hydroxylradikaler, som hjælper med at nedbryde luftforurenende stoffer, i et nyt lys. Kredit:LALS STO
Undersøgelse kaster nyt lys over produktionen af hydroxylradikaler, som hjælper med at nedbryde …Et forskerhold, der omfattede Argonne-kemikeren Stephen Klippenstein, undersøgte produktionen af hydroxylradikaler, som hjælper med at nedbryde luftforurenende stoffer, i et nyt lys. Kredit:LALS STO -
 Copycat-celler behersker nye kommunikationsevnerMedlemmer af Devaraj Research Group står klar for vejledning fra professor Neal Devaraj (yderst til højre). Kredit:Michelle Fredricks Fra kryptonit til Superman til plantning af toksiner til Poiso
Copycat-celler behersker nye kommunikationsevnerMedlemmer af Devaraj Research Group står klar for vejledning fra professor Neal Devaraj (yderst til højre). Kredit:Michelle Fredricks Fra kryptonit til Superman til plantning af toksiner til Poiso


