Fujitsu udvikler teknologi til at forudsige biokemiske reaktioner, afklaring af mekanismerne for genetiske lidelser
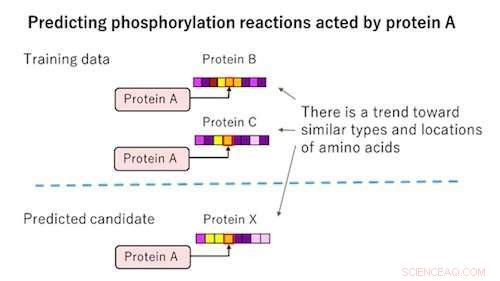
Figur 1:Konventionel AI-teknologi. Kredit:Fujitsu
Fujitsu Laboratories Ltd., Insight Center for Data Analytics, en dataanalytisk forskningsinstitution baseret i Irland, og Fujitsu (Ireland) Limited annoncerede i dag udviklingen af en teknologi, der gør det muligt at forudsige store mængder ukendte kemiske reaktioner, omkring dobbelt så mange som den konventionelle procedure. Ved alvorlige sygdomme, herunder kræft, det er almindeligt, at der er abnormiteter i phosphoryleringsreaktioner, som er kemiske reaktioner, der opstår mellem proteiner. Derfor, der er store forventninger til, at afklaring af fosforyleringsreaktioner vil føre til effektive behandlinger. På nuværende tidspunkt imidlertid, fordi kun nogle få fosforyleringsreaktioner er blevet identificeret, der har været et problem med at forudsige store mængder phosphoryleringsreaktioner forårsaget af kombinationer af ukendte proteiner. Nu, ved at bygge en vidensgraf, der kan omfatte et overblik over sammenhængen mellem proteiner, det er muligt at kontrollere forholdet mellem nye proteiner, hvor phosphoryleringsreaktioner kan forudsiges. På denne måde denne teknologi vil bidrage til fremskridt inden for medicin, da det kan forventes at være nyttigt på frontlinjen inden for forskning i lægemiddelopdagelse, og har skræddersyede applikationer inden for præcisionsmedicin.
Udviklingsbaggrund
Biologiske systemer i kroppen vedligeholdes ved udveksling af information gennem de kemiske reaktioner af forskellige proteiner i celler. I de seneste år, videnskaben har forstået, at mange alvorlige sygdomme, såsom kræft, er delvist forårsaget af abnormiteter i phosphoryleringsreaktioner, som er repræsentative for de kemiske reaktioner mellem proteiner. Hvis der kunne udvikles lægemidler, der reparerede unormale fosforyleringsreaktioner, som ville muliggøre mere effektive behandlinger. På nuværende tidspunkt imidlertid, kun få fosforyleringsreaktioner er godt forstået, så der er behov for opdagelse af ukendte fosforyleringsreaktioner, og at berige dataene om phosphoryleringsreaktioner.
Problemer
Fosforyleringsreaktioner er kemiske reaktioner, hvor et protein binder en fosforylgruppe til de aminosyrer, der udgør et andet protein. For at opdage dem, det er nødvendigt at kontrollere de kombinationer af proteiner, der forårsager fosforyleringsreaktioner gennem biologiske eksperimenter. Ikke desto mindre, da der er mere end omkring 800, 000 mulige kombinationer bare med proteiner, og fordi der kræves betydelige omkostninger og tid til biologiske eksperimenter, det er nødvendigt lige fra starten at forudsige kombinationer med høj sandsynlighed. Det er kendt, om en phosphoryleringsreaktion vil forekomme, afhænger af strukturen af aminosyresekvensen, der udgør proteinet. AI-teknologi bliver derfor allerede brugt til at forudsige nye fosforyleringsreaktioner ved at træne AI på strukturen af aminosyresekvenser, som allerede vides at forårsage fosforyleringsreaktioner. Selvom denne teknologi kan forudsige reaktioner, hvor strukturen af aminosyresekvensen ligner dem, der vides at forårsage phosphoryleringsreaktioner, den har ikke været i stand til at forudsige dem, hvor strukturen af aminosyresekvensen er væsentligt forskellig fra de allerede kendte phosphoryleringsreaktioner.
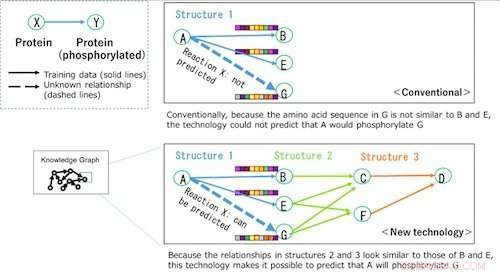
Figur 2:Eksempel på forudsigelse af fosforyleringsreaktioner ved hjælp af vidensgrafer. Kredit:Fujitsu
Ifølge nyere medicinsk forskning, der er et fænomen, hvor proteiner, der har gennemgået reaktioner, kan phosphorylere andre proteiner i en kædereaktion (kædet information), og dette kan være nøglen til at forudsige nye, ukendte phosphoryleringsreaktioner relateret til dette fænomen. Baseret på en sådan forskning, Fujitsu Laboratories, Indsigtscentret, og Fujitsu Ireland har nu ikke kun inkluderet strukturel information om aminosyresekvenser i vidensgrafen, men også lænket information. Organisationerne har udviklet en teknologi (patentanmeldt) til at repræsentere de komplekse mønstre af kemiske reaktioner som optimerede egenskaber, som er knyttet til linjerne i vidensgrafen. Da disse attributter blev skræddersyet til den sofistikerede konstruktion af vidensgrafen, de kan føre til meget nøjagtige forudsigelsesresultater. Konventionelt, forholdet mellem proteiner kunne kun kontrolleres gennem et enkelt led i kæden. Men ved omfattende at vise forholdet mellem proteiner som forbindelser til fosforyleringsreaktioner (kædet information), det bliver muligt at afklare placeringen af de forskellige proteiner ud fra et holistisk perspektiv, og at forudsige ukendte forhold.
Effekter
Da denne teknologi blev testet ved hjælp af evalueringsdata, modellen blev trænet i phosphoryleringsreaktioner (9, 802 reaktioner), og forudsagde 11, 581, 940 nye fosforyleringsreaktioner. Dette viste sin evne til at forudsige omkring dobbelt så mange phosphoryleringsreaktioner sammenlignet med konventionel teknologi, der trænede AI på strukturen af aminosyresekvenser, uden væsentlig ændring af forudsigelsesnøjagtigheden. Ud over, for at teste, om phosphoryleringsreaktioner, der forudsiges ved hjælp af denne teknologi, faktisk kan forekomme i et levende væsen, test blev udført af Systems Biology Ireland, en irsk biologisk forskningsinstitution og en fælles forskningspartner, ved brug af massespektrometriudstyr og antistoffer. I denne test, eksperter i biologi udvalgte og testede nogle få fosforyleringsreaktionsforudsigelsesresultater for proteiner relateret til cancer, og var i stand til at bekræfte ni phosphoryleringsreaktioner, hvoraf otte var reaktioner, der ikke kunne have været forudsagt med konventionel teknologi. Systems Biology Ireland (SBI) direktør Walter Kolch, en verdensførende autoritet inden for systembiologisk forskning, sagde om disse resultater "Kombination af Fujitsus videngrafteknologi med SBI's forståelse af biologiske netværk, vi har udviklet en ny beregningsmetode, der kan forudsige, hvilken kinase der phosphorylerer hvilke substrater. Metoden er nøjagtig og kunne opdage hidtil ukendte fosforyleringssteder, et stort skridt fremad for udvikling af nye lægemidler og mere fokuseret præcisionsmedicin."
Ved at kombinere data om nye phosphoryleringsreaktioner forudsagt af denne teknologi med andre biomedicinske data, det forventes at forbinde de kemiske reaktioner fra årsagerne til en sygdom (abnormiteter i phosphoryleringsreaktioner) til sygdommens symptomer, som derefter kan gives til dem, der er i frontlinjen af forskning, som nyttig information i forbindelse med opdagelse af lægemidler. Effektiviteten af behandlinger for sygdomme som kræft kan variere meget mellem patienter. Denne teknologi, imidlertid, forventes at tydeliggøre den individuelle variation i effekterne af behandlinger, bidrage til at fremme medicin skræddersyet til individuelle patienter. Fujitsu Laboratories, Indsigtscentret, og Fujitsu Ireland vil fortsætte med at forbedre nøjagtigheden af denne teknologi yderligere til at behandle biomedicinske data med vidensgrafer, udvidelse af teknologien til biomedicinske projekter hos Fujitsu Limited i regnskabsåret 2018. Desuden, ved at inkorporere denne teknologi i Fujitsus AI-teknologi, inklusive Fujitsu Human Centric AI Zinrai, organisationerne planlægger at accelerere den biomedicinske forretning.
 Varme artikler
Varme artikler
-
 En forbedret ruthenium-baseret katalysator til primær aminsynteseDirekte aminering af alkoholer over Ru-MgO/TiO2 aktiveret ved elektrondonation fra MgO. Kredit:Yusuke Kita Forskere ved Tokyo Institute of Technology (Tokyo Tech) har udviklet en højtydende genanv
En forbedret ruthenium-baseret katalysator til primær aminsynteseDirekte aminering af alkoholer over Ru-MgO/TiO2 aktiveret ved elektrondonation fra MgO. Kredit:Yusuke Kita Forskere ved Tokyo Institute of Technology (Tokyo Tech) har udviklet en højtydende genanv -
 Naturlignende belægning gør batterier mere holdbare og effektiveCarbon nanorør belagt med en belægning ved anvendelse af kuldioxid i molekylær lagdeponering. Kredit:Aalto University Når batterier oplades og bruges, et komplekst SEI (fast elektrolytinterfase) l
Naturlignende belægning gør batterier mere holdbare og effektiveCarbon nanorør belagt med en belægning ved anvendelse af kuldioxid i molekylær lagdeponering. Kredit:Aalto University Når batterier oplades og bruges, et komplekst SEI (fast elektrolytinterfase) l -
 Udforskning af biomimik – opbygning af den næste generation af tilpasningsdygtige materialer fra na…En vaskulariseret polymer inspireret af venestrukturen i et blad. De vaskulære kanaler i polymeren kan bruges til at indføre forskellige typer forbindelser i materialet, som så kan diffundere til over
Udforskning af biomimik – opbygning af den næste generation af tilpasningsdygtige materialer fra na…En vaskulariseret polymer inspireret af venestrukturen i et blad. De vaskulære kanaler i polymeren kan bruges til at indføre forskellige typer forbindelser i materialet, som så kan diffundere til over -
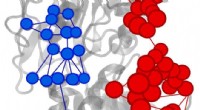 Kemikere finder et nyt værktøj til at forstå enzymer – GoogleEffektorudløst stigning (rød) eller reduktion (blå) af informationsstrømmen i IGPS-enzym. Kredit:Uriel Morzan Yale-forskere har taget en ny tilgang til at optrevle den komplekse struktur og regule
Kemikere finder et nyt værktøj til at forstå enzymer – GoogleEffektorudløst stigning (rød) eller reduktion (blå) af informationsstrømmen i IGPS-enzym. Kredit:Uriel Morzan Yale-forskere har taget en ny tilgang til at optrevle den komplekse struktur og regule


