Nikkelkatalysator letter oprettelsen af en enkelt stereoisomer med to kirale centre
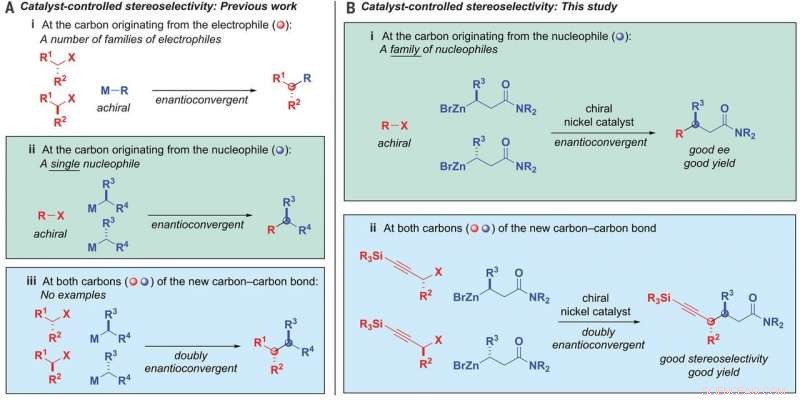
Alkyl-alkylbindingsdannelse. (A) Katalysatorstyret stereoselektivitet-tidligere arbejde. (B) Katalysatorstyret stereoselektivitet-denne undersøgelse. ee, enantiomert overskud; M, metal; R, substituent; X, forlader gruppen. Kredit: Videnskab (2020). DOI:10.1126/science.aaz3855
Et team af forskere ved California Institute of Technology har fundet en nikkelkatalysator, der binder alkylnukleofil og alkylelektrofiler til en enkelt stereoisomer med to kirale centre. I deres papir offentliggjort i tidsskriftet Videnskab , gruppen beskriver deres proces. Jianyu Xu og Mary Watson fra University of Delaware har udgivet et perspektivstykke om det arbejde, teamet udførte i det samme journalnummer.
I kemi, reaktioner, der resulterer i materialer med carbon-carbon-bindinger, er ønskelige, fordi de bruges i store applikationer, såsom lægemidler og landbrugsprodukter. Sådanne reaktioner er typisk afhængige af overgangsmetalbaserede katalysatorer-men der er begrænsninger, der forhindrer mange i at blive brugt. Mange arbejder kun med alkylforbindelser, hvilket kan føre til uønskede bivirkninger. Også, mange sådanne reaktioner resulterer i racemiske blandinger af produkter, resulterer i ineffektivitet (racemiske blandinger er dem, der har lige store mængder venstre- og højrehåndede enantiomerer af et chiralt molekyle).
Historisk set har det været anset for at være meget vanskeligt at forbinde racemiske blandinger af to alkyler med opretholdelse af kontrollen med stereokemien i begge ender af produktet. Men nu, det har ændret sig, takket være arbejdet fra teamet på CIT, og det har ført til en metode til at udføre reaktioner, der fører til ønskelige carbon-carbonbundne materialer.
I deres arbejde, teamet udviklede en nikkelkatalysator, der tillader en alkylnukleofil at binde sig til en alkylelektrofil. Især begge er racemiske carbonforbindelser. De brugte en ligand, der var bidentat - som tillod åbne pletter på nikkelen at binde sig med ilt på nukleofilerne.
Reaktionen involverede også anvendelse af β-zinkerede amidnukleofiler og propargyliske halogenidelektrofiler. Og den blev styret af katalysatoren. Ved at tilsidesætte chiral information i begge startprodukterne og derefter bringe dem sammen igen på en foruddefineret måde, carbon-carbon-bindingerne blev dannet. Resultatet var en enkelt stereoisomer, der havde to kirale centre. Ved brug af nikkelkatalysatoren, gruppen koblede en racemisk blanding med nukleofiler og elektrofiler med op til 95 procent stereoselektivitet og 82 procent udbytte. Testning viste også, at den var kompatibel med 19 funktionelle grupper.
© 2020 Science X Network
 Varme artikler
Varme artikler
-
 Hvordan folder cellemaskiner fejlfoldede proteiner ud?Kredit:Leiden University Proteinkæder foldes typisk for at fungere. Foldning er en kompleks proces, og hvis det gøres korrekt, fører det til en unik funktionel foldetopologi for en given proteinkæ
Hvordan folder cellemaskiner fejlfoldede proteiner ud?Kredit:Leiden University Proteinkæder foldes typisk for at fungere. Foldning er en kompleks proces, og hvis det gøres korrekt, fører det til en unik funktionel foldetopologi for en given proteinkæ -
 Sådan beregnes reaktionshastighedHastigheden, hvormed kemiske stoffer reagerer, varierer meget. En søm kan tage år at ruste, mens sprængstoffer sprænger i tusindedels sekund. Generelt involverer en reaktionshastighed ændringen i konc
Sådan beregnes reaktionshastighedHastigheden, hvormed kemiske stoffer reagerer, varierer meget. En søm kan tage år at ruste, mens sprængstoffer sprænger i tusindedels sekund. Generelt involverer en reaktionshastighed ændringen i konc -
 Uregerbart kræftprotein bliver narkotika, takket være buskCurcusone D, den første syntetiserede BRAT-1-hæmmer, stammer oprindeligt fra roden af Jatropha curcas, en busk hjemmehørende i Amerika. Kredit:Forest og Kim Starr En kemiker fra Purdue Universit
Uregerbart kræftprotein bliver narkotika, takket være buskCurcusone D, den første syntetiserede BRAT-1-hæmmer, stammer oprindeligt fra roden af Jatropha curcas, en busk hjemmehørende i Amerika. Kredit:Forest og Kim Starr En kemiker fra Purdue Universit -
 Brug af en to-trins tilgang til at omdanne alifatiske aminer til unaturlige aminosyrerStrategi for enantiokontrol af N-H insertionsreaktioner af alifatiske aminer med carbener. (A) Repræsentative lægemidler, der demonstrerer allestedsnærværelsen af chirale alifatiske aminer i bioakti
Brug af en to-trins tilgang til at omdanne alifatiske aminer til unaturlige aminosyrerStrategi for enantiokontrol af N-H insertionsreaktioner af alifatiske aminer med carbener. (A) Repræsentative lægemidler, der demonstrerer allestedsnærværelsen af chirale alifatiske aminer i bioakti
- Ultrafølsom sensor ved hjælp af N-doteret grafen
- Lyndødsfald i USA er langt,
- NASA ser vindakseffekter på den tropiske cyklon Yvette
- Hvilke klipper er fluorescerende under et UV-lys?
- Udvikling af en nanotrådsanordning til at opdage kræft med en urintest
- Hvad dannes når to eller flere atomer kombineres?


