Katalysator muliggør reaktioner ved hjælp af grønt lys

Kolber indeholdende titaniumkatalysatoren og det røde farvestof, som bestråles med grønt lys i laboratoriet på Kekulé Institute of Organic Chemistry and Biochemistry ved universitetet i Bonn. Kredit:Zhenhua Zhang
For første gang, kemikere ved University of Bonn og Lehigh University i USA har udviklet en titaniumkatalysator, der gør lys anvendeligt til selektive kemiske reaktioner. Det giver et omkostningseffektivt og ikke-toksisk alternativ til ruthenium- og iridiumkatalysatorer, der anvendes i øjeblikket, som er baseret på meget dyre og giftige metaller. Den nye katalysator kan bruges til at fremstille meget selektive kemiske produkter, der kan danne grundlag for antivirale lægemidler eller selvlysende farvestoffer, for eksempel. Resultaterne er offentliggjort i den internationale udgave af tidsskriftet Angewandte Chemie .
Elektroner i kemiske molekyler er tilbageholdende med at leve et enkelt liv; de forekommer normalt i par. Så er de særligt stabile og har ikke tendens til at skabe nye partnerskaber i form af nye obligationer. Imidlertid, hvis nogle af elektronerne bringes til et højere energiniveau ved hjælp af lys (fotoner), tingene begynder at se anderledes ud, når det kommer til denne "monogami":I sådan en ophidset tilstand, molekylerne kan lide at donere eller acceptere en elektron. Dette skaber såkaldte "radikale", ' der har elektroner, er meget reaktive og kan bruges til at danne nye bindinger.
Bestråling med grønt lys
Denne nye katalysator er baseret på dette princip:I sin kerne er titanium, som er forbundet med en kulstofring, hvori elektronerne er særligt mobile og let kan exciteres. Grønt lys er tilstrækkeligt til at bruge katalysatoren til elektronoverførsel til at producere reaktive organiske mellemprodukter, som ellers ikke er let tilgængelige. "I laboratoriet, vi bestrålede en reaktionskolbe indeholdende titaniumkatalysatoren, der kan ses som et 'rødt farvestof' med grønt lys, " rapporterer prof. Dr. Andreas Gansäuer fra Kekulé Institute of Organic Chemistry and Biochemistry ved Bonn Universitet. "Og det virkede med det samme." Blandingen genererer radikaler fra organiske molekyler, der initierer mange reaktionscyklusser, hvorfra en bred vifte af kemikalier produkter kan fremstilles.
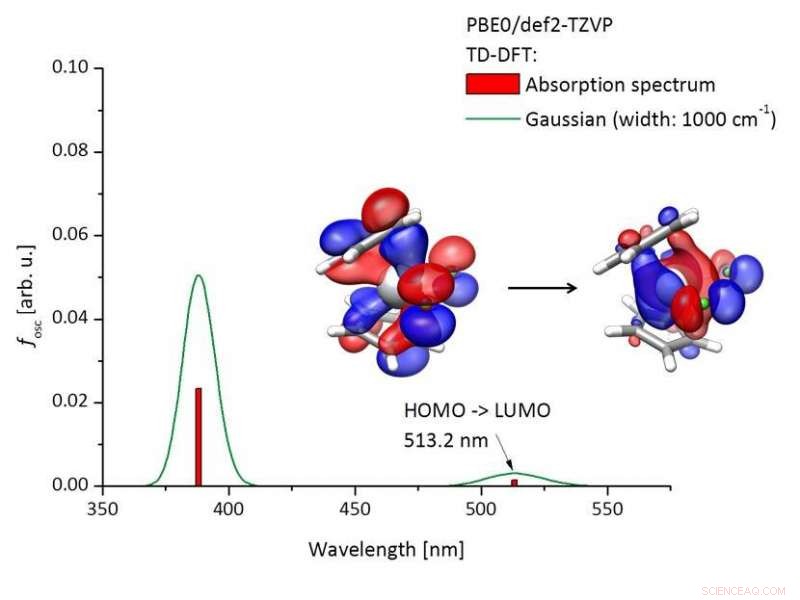
Beregnet absorptionsspektrum for Titanocendichlorid [(C5H4)2TiCl2)] og molekylære orbitaler involveret i excitationen. Kredit:Tobias Hilche
En nøglefaktor i reaktioner med denne fotoredox-katalysator er bølgelængden af det lys, der bruges til bestråling. "Ultraviolet stråling er uegnet, fordi den er alt for energirig og ville ødelægge de organiske forbindelser, " siger Gansäuer. Grønt lys fra LED-lamper er både mildt og energirigt nok til at udløse reaktionen.
Katalysatorer er stoffer, der øger hastigheden af kemiske reaktioner og reducerer aktiveringsenergien uden at blive forbrugt selv. Det betyder, at de er tilgængelige løbende og kan udløse reaktioner, som ellers ikke ville opstå i denne form. Katalysatoren kan skræddersyes til de ønskede produkter afhængigt af det organiske molekyle, som titanium er bundet med.
Byggesten til antivirale lægemidler eller selvlysende farvestoffer
Den nye titaniumkatalysator letter reaktionerne af epoxider, en gruppe kemikalier, som epoxyharpiks er lavet af. Disse bruges som klæbemiddel eller til kompositter. Imidlertid, forskerne sigter ikke efter dette masseprodukt, men til syntese af meget mere værdifulde finkemikalier. "Det titanium-baserede, skræddersyede fotoredox-katalysatorer kan for eksempel bruges til at fremstille byggesten til antivirale lægemidler eller selvlysende farvestoffer, " siger Gansäuer. Han er overbevist om, at disse nye katalysatorer giver et omkostningseffektivt og mere bæredygtigt alternativ til de ruthenium- og iridiumkatalysatorer, der hidtil er blevet brugt, som er baseret på meget dyre og giftige metaller.
Udviklingen er en international samarbejdsindsats af Zhenhua Zhang, Tobias Hilche, Daniel Slak, Niels Rietdijk og Andreas Gansäuer fra University of Bonn og Ugochinyere N. Oloyede og Robert A. Flowers II fra Lehigh University (U.S.). Mens forskerne fra universitetet i Bonn undersøgte, hvordan de ønskede forbindelser bedst kunne syntetiseres med den nye katalysator, deres kolleger fra USA udførte målinger for at bevise reaktionsvejene. "Luminescensfænomenet åbner virkelig interessant plads til at overveje design af nye bæredygtige reaktioner, der fortsætter gennem frie radikaler mellemprodukter, " siger prof. Robert Flowers fra Lehigh University.
 Varme artikler
Varme artikler
-
 Forskere udvikler ultrahøjtydende plasmoniske metaloxidmaterialerKredit:CC0 Public Domain I en undersøgelse offentliggjort i Avancerede materialer , forskere fra Hefei National Laboratory for Physical Sciences på Microscale, University of Science and Technolo
Forskere udvikler ultrahøjtydende plasmoniske metaloxidmaterialerKredit:CC0 Public Domain I en undersøgelse offentliggjort i Avancerede materialer , forskere fra Hefei National Laboratory for Physical Sciences på Microscale, University of Science and Technolo -
 Inspirerer folk til at træffe bedre livsstilsvalg – gennem isotoperForskerne Amrita Rhoads og Gwyneth Gordon måler isotopforhold i en hårprøve for at vurdere, hvad deltagerne typisk spiste. Kredit:ASU Fitnessmål er typisk på forkant med nytårsforsæt for mange ame
Inspirerer folk til at træffe bedre livsstilsvalg – gennem isotoperForskerne Amrita Rhoads og Gwyneth Gordon måler isotopforhold i en hårprøve for at vurdere, hvad deltagerne typisk spiste. Kredit:ASU Fitnessmål er typisk på forkant med nytårsforsæt for mange ame -
 Hvad er råmaterialerne i plastflasker?Plast gennemgår en fremstillingsproces for at ende op som flasker til flydende stoffer som mælk, soda, motorolie og shampoo og til tørre produkter såsom medicin og kosttilskud. I sin rå tilstand bestå
Hvad er råmaterialerne i plastflasker?Plast gennemgår en fremstillingsproces for at ende op som flasker til flydende stoffer som mælk, soda, motorolie og shampoo og til tørre produkter såsom medicin og kosttilskud. I sin rå tilstand bestå -
 Mindre er mere, når det kommer til at forudsige molekylers ledningsevneUChicago-studerende Manas Sajjan, venstre, og prof. David Mazziotti, holde en model, der viser et molekyle, hvorpå de testede en bedre tilgang til at forudsige ledningsevne. Kredit:Jean Lachat/Univers
Mindre er mere, når det kommer til at forudsige molekylers ledningsevneUChicago-studerende Manas Sajjan, venstre, og prof. David Mazziotti, holde en model, der viser et molekyle, hvorpå de testede en bedre tilgang til at forudsige ledningsevne. Kredit:Jean Lachat/Univers
- Ø-hopping:Genetik afslører, hvordan mennesker bosatte sig i det fjerne Stillehav
- Tidlig Mars klima var periodisk varmt
- En ende på huller for folk med følsomme tænder?
- Naturkatastrofer udvider racemæssig velstandskløft
- USA øger jordens beskyttelse mod asteroider, kometer
- At give en stemme til indvandrermødre fra Latina, der er ramt af COVID-19


