Teknikken tillader praktisk, præcis optisk billeddannelse af individuelle proteiner
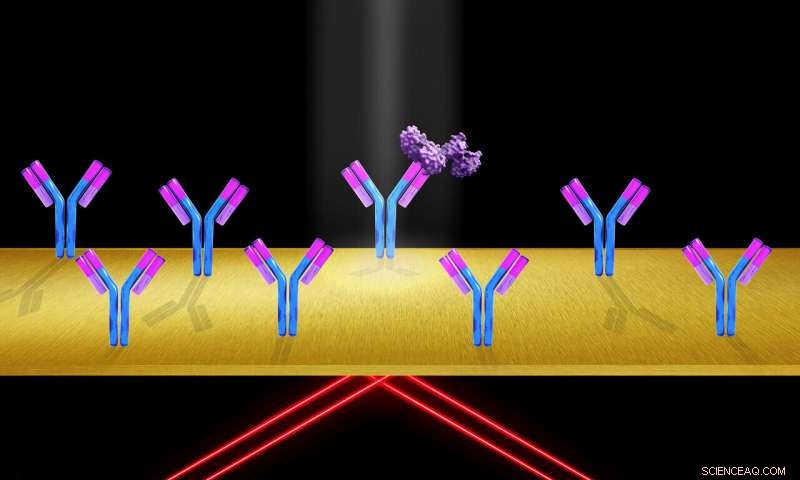
Når proteinmolekyler (lilla) binder sig til immobiliserede receptormolekyler, (som de Y-formede antistoffer, der er fastgjort til objektglassets overflade), brydningsindekset ved guldoverfladen ændres, ændring af overfladens plasmonresonans, og producerer en stigning i signalintensitet. Kredit:Shireen Dooling
Betragtes ofte som kroppens arbejdsheste, proteiner er blandt de vigtigste biomolekyler, der er kritiske for livsprocesser. De giver strukturelt fundament for celler og væv og udfører en svimlende række opgaver, fra at metabolisere energi og hjælpe celler med at kommunikere med hinanden til at forsvare kroppen mod patogener og styre celledeling og vækst.
Fordi proteindysfunktion er impliceret i så mange alvorlige sygdomme, proteiner er de primære mål for de fleste terapeutiske lægemidler.
I en ny undersøgelse, Shaopeng Wang og hans kolleger beskriver en metode til at undersøge proteiner i detaljer. At gøre dette, hans gruppe gør smart brug af et fænomen kendt som overfladeplasmonresonans (SPR), indarbejde det i en innovativ type mikroskop.
Mens SPR har været en kraftfuld teknik til at undersøge de meget smås verden, herunder interaktioner mellem bakterier og vira, undersøgelsen markerer den første lejlighed, hvor SPR med succes er blevet brugt til at billede enkelte molekyler, I dette tilfælde, proteiner. Den nye metode er kendt som plasmon -spredningsmikroskopi.
Ifølge Wang:"Løbet om at udvikle denne teknologi startede faktisk for 20 år siden." Sammen med hovedforfatter NJ Tao beregnede gruppen, at en modificeret form for SPR skulle have følsomhed til at løse enkelte proteiner, skønt der var krævet meget forberedende arbejde for at gøre dette til virkelighed.
Wang er forsker i Biodesign Center for Bioelektronik og Biosensorer. Den nye forskning fremgår af den avancerede online tilføjelse af tidsskriftet Naturmetoder . Pengfei Zhang, en postdoc i midten, er hovedforfatter af papiret.
Ved hjælp af SPR kan forskere undersøge dynamikken i celleoverfladeproteiner-primære mål for lægemiddeldesign-som er særligt udfordrende at observere ved hjælp af røntgenkrystallografi eller NMR-spektroskopi, de to konventionelle teknikker blev normalt brugt til at karakterisere proteiner.
Men hvad er en overfladeplasmon? "En egenskab ved metal er, at du har mange frie elektroner, "Wang siger, refererer til elektroner, der ikke er bundet til atomer. "Når tilstanden af indfaldende lys på disse elektroner er helt rigtige, energien i lyset får disse elektroner til at resonere. Disse oscillerende elektroner producerer en bølge hen over metaloverfladen. Dette er overfladeplasmonresonans. "
For at detektere bindingen af et analytmolekyle (som et protein) til et receptormolekyle ved hjælp af SPR, receptormolekylet er normalt immobiliseret på sensoroverfladen, og analytmolekylet tilsættes til en vandig opløsning. Polariseret lys rettes typisk under overfladen af en tynd guldfilm, hvor overfladeplasmoner genereres i en bestemt vinkel af det indfaldende lys. Overfladens indeslutning af lys ved overfladeplasmon ses som et fald i intensiteten af reflekteret lys.
Når proteinmolekyler binder sig til immobiliserede receptormolekyler, brydningsindekset ved guldoverfladen ændres, ændring af overfladeplasmonresonansbetingelsen og frembringelse af en stigning i signalintensitet.
For at forfine og kalibrere systemet, forskerne observerede først bindingshændelser ved hjælp af polystyren -nanopartikler, hvis størrelse kan kontrolleres præcist. Nanopartiklerne har også fordelen ved at producere højere kontrast, hjælpe deres påvisning af SPR. Brug af mindre og mindre nanopartikler tillod gruppen at nå de små dimensioner af et biologisk protein.
For at opnå en så imponerende opløsning, forskerne brugte en variant af SPR -teknikken, detektering af lys på proteinbindingshændelserne ovenfra, frem for nedenfor, som dramatisk eliminerer baggrundsstøj, frembringer et skarpt billede. Fordi bundne proteiner spreder SPR -lyset i alle retninger, Registrering fra toppen undgår det reflekterede lys, stærkt forbedret billedkvalitet.
Wang sammenligner effekten med at se stjerner mod mørkets baggrundsgardin, der henviser til, at stjerner er usynlige for øjet mod den støjende baggrund af dagslys. Påvisning af enkeltproteiner kan realiseres uden en meget kraftig lyskilde, da SPR producerer stærk forbedring af lysfeltet nær sensoroverfladen, præcisering af proteinsignalet.
Ved at slå ind på proteinbindingsaffinitet, en af de centrale parametre, der er afgørende for design af sikrere, mere effektive lægemidler, den nye SPR -teknik skulle have en lys fremtid på den biomedicinske arena samt kaste nyt lys over fundamentale spørgsmål på molekylær skala.
 Varme artikler
Varme artikler
-
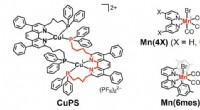 Store fremskridt for kulstoffangst ved hjælp af jordrige elementer som fotokatalytisk systemStrukturen af CuPS, kobberkomplekset, der opfører sig som en redox -lysfølsomhed, og den manganbaserede katalysator udviklet i undersøgelsen. Kredit: Journal of the American Chemical Society Fo
Store fremskridt for kulstoffangst ved hjælp af jordrige elementer som fotokatalytisk systemStrukturen af CuPS, kobberkomplekset, der opfører sig som en redox -lysfølsomhed, og den manganbaserede katalysator udviklet i undersøgelsen. Kredit: Journal of the American Chemical Society Fo -
 Neutronundersøgelse af glaukomlægemidler giver fingerpeg om enzymmål for aggressive kræftformerDet aktive sted for hCA II. Det aktive sted er flankeret af hydrofile (violette) og hydrofobe (grønne) bindingslommer, der kan bruges til at designe specifikke lægemidler rettet mod cancer-associerede
Neutronundersøgelse af glaukomlægemidler giver fingerpeg om enzymmål for aggressive kræftformerDet aktive sted for hCA II. Det aktive sted er flankeret af hydrofile (violette) og hydrofobe (grønne) bindingslommer, der kan bruges til at designe specifikke lægemidler rettet mod cancer-associerede -
 Afslører svindel med kød og fisk med en håndholdt MasSpec Pen på få sekunderMasSpec Pen kan autentificere typen og renheden af kødprøver på så lidt som 15 sekunder. Kredit: Tidsskrift for landbrugs- og fødevarekemi Svindel med kød og fisk er globale problemer, koster f
Afslører svindel med kød og fisk med en håndholdt MasSpec Pen på få sekunderMasSpec Pen kan autentificere typen og renheden af kødprøver på så lidt som 15 sekunder. Kredit: Tidsskrift for landbrugs- og fødevarekemi Svindel med kød og fisk er globale problemer, koster f -
 Video:Den eneste detox, du nogensinde får brug forKredit:The American Chemical Society Folk taler hele tiden om, hvordan de skal afgifte. Og der er en række virksomheder, der er en kilometer lang og venter på at sælge juicer og smoothies til dig
Video:Den eneste detox, du nogensinde får brug forKredit:The American Chemical Society Folk taler hele tiden om, hvordan de skal afgifte. Og der er en række virksomheder, der er en kilometer lang og venter på at sælge juicer og smoothies til dig
- Det Sydkinesiske Hav viste sig at have forhøjede niveauer af menneskeskabt overfladenitrogen
- Atomenergi kan se rolle aftage, FN-agentur siger
- Rusland siger farvel til den første mand, der gik i rummet
- Facebook dræber demokratiet med sine personlighedsprofileringsdata
- Plasts skæbne i havene
- Metoder til Factoring Trinomials


