Forskere bruger membraner, der fjerner salt fra vand for at hjælpe med at spalte havvand til brændstof
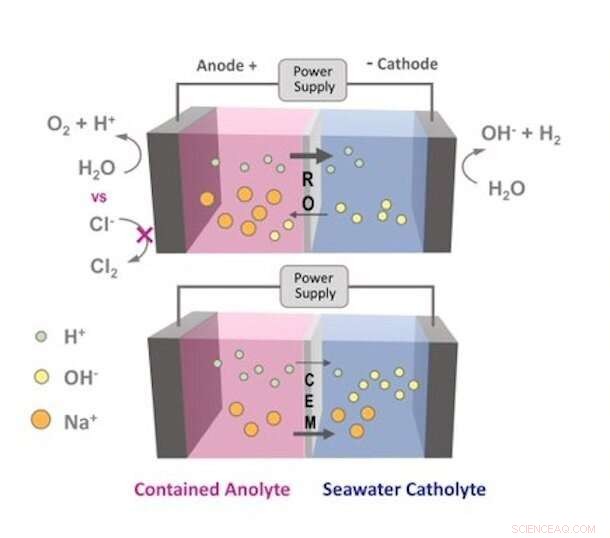
Her er en visuel repræsentation af, hvordan ionbevægelse påvirkes af en omvendt osmose (RO) membran versus en kationbyttermembran. Kloridioner fra havvandet er ikke i stand til at passere gennem RO -membranen og oxidere til klorgas. Kredit:Logan Research Group
Solens kraft, vind og hav kan snart kombinere til at producere rentbrændende brintbrændstof, ifølge et hold af Penn State-forskere. Holdet integrerede vandrensningsteknologi i et nyt proof-of-concept design til en havvandselektrolysator, som bruger en elektrisk strøm til at adskille brint og ilt i vandmolekyler.
Denne nye metode til "spaltning af havvand" kunne gøre det lettere at omdanne vind- og solenergi til et opbevaringsbart og bærbart brændstof, ifølge Bruce Logan, Kappe professor i miljøteknik og professor ved Evan Pugh University.
"Brint er et fantastisk brændstof, men du skal klare det Logan sagde. "Den eneste bæredygtige måde at gøre det på er at bruge vedvarende energi og producere den fra vand. Du skal også bruge vand, som folk ikke vil bruge til andre ting, og det ville være havvand. Så, den hellige gral ved at producere brint ville være at kombinere havvandet og vind- og solenergien, der findes i kyst- og offshoremiljøer."
På trods af overflod af havvand, det er ikke almindeligt brugt til vandspaltning. Medmindre vandet afsaltes inden det kommer ind i elektrolysatoren - et dyrt ekstra trin - bliver chloridionerne i havvandet til giftig klorgas, som nedbryder udstyret og siver ud i miljøet.
For at forhindre dette, forskerne indsatte en tynd, semipermeabel membran, oprindeligt udviklet til at rense vand i omvendt osmose (RO) behandlingsprocessen. RO-membranen erstattede ionbytningsmembranen, der almindeligvis anvendes i elektrolysatorer.
"Idéen bag RO er, at man lægger et rigtig højt tryk på vandet og skubber det gennem membranen og holder kloridionerne bagved, " sagde Logan.
I en elektrolysator, havvand ville ikke længere blive skubbet gennem RO-membranen, men indeholdt i det. En membran bruges til at hjælpe med at adskille de reaktioner, der forekommer i nærheden af to nedsænkede elektroder - en positivt ladet anode og en negativt ladet katode - forbundet med en ekstern strømkilde. Når strømmen er tændt, vandmolekyler begynder at spalte ved anoden, frigiver små brintioner kaldet protoner og skaber iltgas. Protonerne passerer derefter gennem membranen og kombineres med elektroner ved katoden for at danne brintgas.
Med RO-membranen isat, havvand holdes på katodesiden, og chloridionerne er for store til at passere gennem membranen og nå anoden, afværge produktionen af klorgas.
Men i vandspaltning, Logan bemærkede, andre salte opløses bevidst i vandet for at gøre det ledende. Ionbyttermembranen, som filtrerer ioner ved elektrisk ladning, tillader saltioner at passere igennem. Det gør RO-membranen ikke.

Havvand kan omdannes til brintbrændstof ved hjælp af dette design til en havvandselektrolysator, ifølge forskere fra Penn State. Kredit:Tyler Henderson
"RO-membraner hæmmer saltbevægelse, men den eneste måde du genererer strøm på i et kredsløb er fordi ladede ioner i vandet bevæger sig mellem to elektroder, " sagde Logan.
Med bevægelsen fra de større ioner begrænset af RO -membranen, forskerne skulle se, om der var nok små protoner, der bevægede sig gennem porerne til at holde en høj elektrisk strøm.
"I bund og grund, vi måtte vise, at det, der lignede en grusvej, kunne være en mellemstat, " sagde Logan. "Vi skulle bevise, at vi kunne få en høj mængde strøm gennem to elektroder, når der var en membran mellem dem, der ikke ville tillade saltioner at bevæge sig frem og tilbage."
Gennem en række eksperimenter, der for nylig blev offentliggjort i Energi- og miljøvidenskab , forskerne testede to kommercielt tilgængelige RO-membraner og to kationbyttermembraner, en type ionbyttermembran, der tillader bevægelse af alle positivt ladede ioner i systemet.
Hver blev testet for membranmodstand mod ionbevægelse, mængden af energi, der skal til for at fuldføre reaktioner, produktion af brint og ilt, interaktion med chloridioner og membranforringelse.
Logan forklarede, at mens en RO-membran viste sig at være en "jordvej, " den anden klarede sig godt i forhold til kationbyttermembranerne. Forskerne undersøger stadig, hvorfor der var så stor forskel på de to RO-membraner.
"Idéen kan virke, " sagde han. "Vi ved ikke præcis, hvorfor disse to membraner har fungeret så forskelligt, men det er noget, vi skal finde ud af."
For nylig, forskerne modtog en $300, 000 tilskud fra National Science Foundation (NSF) til at fortsætte med at undersøge havvandselektrolyse. Logan håber, at deres forskning vil spille en kritisk rolle i reduktionen af kuldioxidemissioner rundt om i verden.
"Verden leder efter vedvarende brint, " sagde han. "F.eks. Saudi-Arabien har planlagt at bygge et brintanlæg til $5 milliarder, der skal bruge havvand. Lige nu, de skal afsalte vandet. Måske kan de bruge denne metode i stedet for."
 Varme artikler
Varme artikler
-
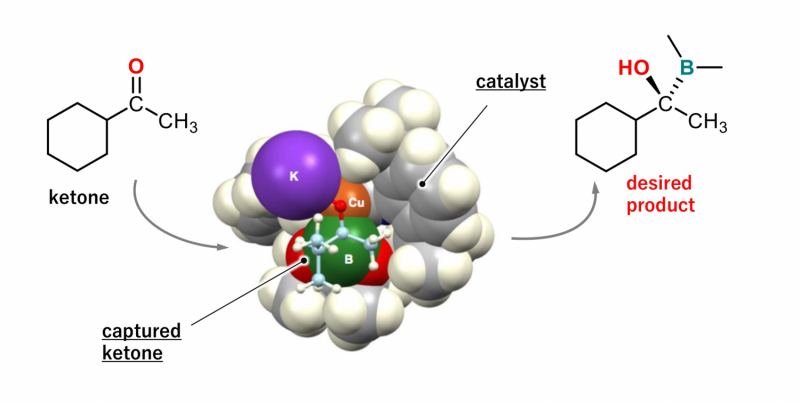 Verdens første succes inden for asymmetrisk borylering af ketonerIllustration af en katalysator, der fanger en keton og lader en bor binde til ketonen bagfra. Kredit:Hokkaido University Et team af forskere fra Hokkaido University har udviklet verdens første met
Verdens første succes inden for asymmetrisk borylering af ketonerIllustration af en katalysator, der fanger en keton og lader en bor binde til ketonen bagfra. Kredit:Hokkaido University Et team af forskere fra Hokkaido University har udviklet verdens første met -
 Nobel Kemipris:Stor pris for molekylære forholdKredit:Wikipedia Nobelprisen i kemi belønner forskere for store fremskridt i at studere de uendeligt små stykker materiale, der er livets byggesten. De seneste priser er gået til forskere, der ud
Nobel Kemipris:Stor pris for molekylære forholdKredit:Wikipedia Nobelprisen i kemi belønner forskere for store fremskridt i at studere de uendeligt små stykker materiale, der er livets byggesten. De seneste priser er gået til forskere, der ud -
 Undersøgelse detaljerede regulering af en multi-drug transporter(venstre mod højre):Reza Dastvan, Ph.d., Smriti Mishra, Ph.d., og Hassane Mchaourab, Ph.d., studerer den indre funktion af en proteinpumpe, der bidrager til kemoterapiresistens mod kræft. Kredit:Vande
Undersøgelse detaljerede regulering af en multi-drug transporter(venstre mod højre):Reza Dastvan, Ph.d., Smriti Mishra, Ph.d., og Hassane Mchaourab, Ph.d., studerer den indre funktion af en proteinpumpe, der bidrager til kemoterapiresistens mod kræft. Kredit:Vande -
 Forskere først til at forbinde silicium atomer på overfladerSkematisk repræsentation af de involverede discipliner (i midten) og transformationen af ideen (venstre) til det endelige produkt (højre). I baggrunden til højre er et scanning tunneling mikroskop b
Forskere først til at forbinde silicium atomer på overfladerSkematisk repræsentation af de involverede discipliner (i midten) og transformationen af ideen (venstre) til det endelige produkt (højre). I baggrunden til højre er et scanning tunneling mikroskop b
- En ny måde at skabe molekyler til lægemiddeludvikling
- NASA ser den kompakte tropiske storm Jangmi forlade det østkinesiske hav
- Multitasking-katalysatoren
- Google afslører søgeændringer for at berolige EU
- Hvordan man forfalsker kvantepenge
- uSEE -gennembrud låser op for nanoskalaverdenen på standardbiologisk laboratorieudstyr


