Lovende anticancer-molekyle identificeret
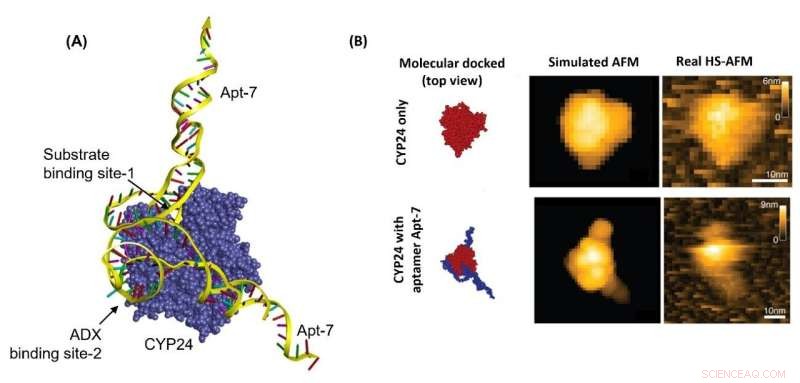
Figur 1. En integreret tilgang til HS-AFM og molekylær docking for at afsløre bindingsmekanismen for Apt-7 til CYP24 (A) Den tredimensionelle visning af de toprangerede dockede konformationer af CYP24 og Apt-7. De forudsagte bindingssteder for Apt-7 er vist med pil. Aptamer binder til substratbindingsstedet for CYP24 (bindingssted-1) og til ADX-bindingsstedet for CYP24 (bindingssted-2). (B) Sammenligning af pseudo-HS-AFM-grafikken af CYP24-Apt-7 ved hjælp af molekylær docking-genereret topplacering af CYP24-Apt-7-komplekset med realtidsbillederne taget af HS-AFM. Kredit:Kanazawa University
Forskere ved Kanazawa University i samarbejde med hold fra Toyama Prefectural University og BioSeeds Corporation rapporterer i ACS Applied Materials &Interfaces identifikation af et molekyle med øget antiproliferativ aktivitet i cancerceller. Den underliggende biomolekylære mekanisme er hæmningen af et enzym, der overproduceres i flere typer kræft.
Vitamin D3 har vigtige biologiske funktioner, herunder opretholdelse af knoglemineraltæthed, hvilket minimerer risikoen for knoglebrud. Men D3-vitamin menes også at have anticanceraktivitet, da lave D3-vitaminniveauer og den tilhørende overproduktion af et enzym kaldet CYP24 er forbundet med en dårlig prognose for kræftpatienter. Molekyler, der begrænser eller hæmmer virkningen af CYP24 og molekyler, der efterligner funktionen af vitamin D3, er i dag meget undersøgt som potentielle antiproliferative midler til kræftbehandling.
Imidlertid har mange af de inhibitorer og D3-analoger, der er syntetiseret indtil videre, vist utilstrækkelig klinisk respons, såvel som uønskede bivirkninger. Nu har Madhu Biyani fra Kanazawa University og kolleger identificeret et DNA-afledt molekyle, der binder til og hæmmer funktionen af CYP24 og viser lovende antiproliferativ aktivitet. Forskerholdet giver også detaljeret indsigt i de relevante molekylære processer, der er i spil.
Forskerne screenede et stort antal DNA-aptamerer - stykker af enkeltstrenget DNA med særlige tredimensionelle strukturer, der kan binde til specifikke målmolekyler og have en funktionel effekt ved binding. De ledte efter DNA-aptamerer, der binder til CYP24, men ikke til det lignende enzym CYP271B, som er ansvarligt for syntesen af vitamin D3.
En indledende langliste på 18 aptamer-kandidater blev reduceret til 11 repræsentanter med specifikke molekylære strukturer. Forskerne kontrollerede CYP24-hæmningsaktiviteten af de 11 repræsentative aptamerer in vitro. Fire kandidater, der resulterede i hæmning af CYP24, men ikke i hæmning af CYP27B1, var tilbage, hvoraf en (Apt-7) blev bibeholdt til yderligere undersøgelse.
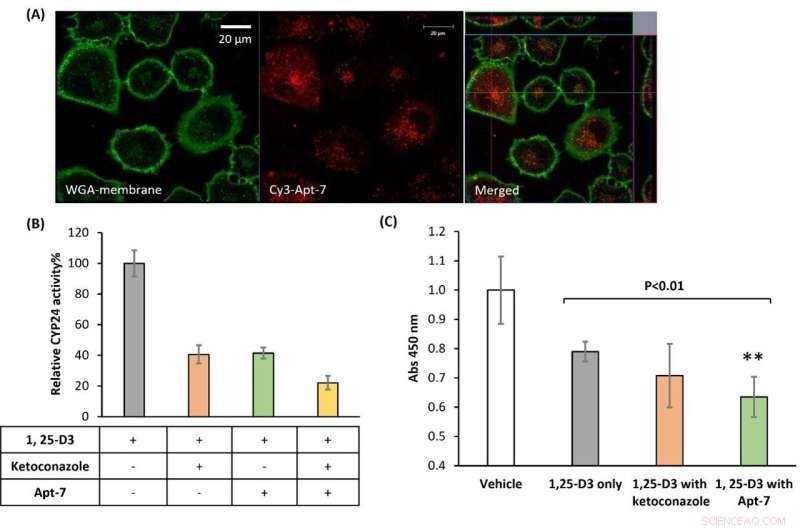
Figur 2. Internalisering af aptamer i A549-celler er uundværlig for CYP24-hæmning og forstærkning af 1,25-D3-medieret cellevæksthæmning. (A) Internalisering af Aptamer i A549-celler. A549 lungecancerceller blev behandlet med 500 nM aptamer Apt-7 og deres membraner blev farvet grønne (Wheat Germ Agglutinin (WGA) Conjugates). Konfokal mikroskopi afslørede det intracellulære signal, afledt af internaliseret aptamer (rød fluorescens, Cy3). (B) Apt-7 hæmmer den CYP24-medierede katabolisme af 1,25-D3 i A549-celler. Efter 18 timers aptamerbehandling blev 1,25-D3 metabolitomdannelsesforhold og relativ CYP24-aktivitet bestemt ved HPLC. (C) Apt-7 forbedrer den antiproliferative funktion af 1,25-D3 i A549-celler. Kredit:Kanazawa University
Biyani og kolleger udførte simuleringer af Apt-7-binding til CYP24. Et molekylært docking-scenarie blev opnået, som de kontrollerede eksperimentelt ved at sammenligne adfærden af en blanding af vitamin D3 og CYP24 med og uden Apt-7. Simuleringerne og eksperimenterne viste, at Apt-7 resulterer i hæmning af CYP24-aktivitet, og at det, der sker, er, at aptameren sandsynligvis interfererer med enzymets aktive sted. Forskerne udførte også højhastigheds atomkraftmikroskopi på bindingen af CYP24 og Apt-7 i realtid, hvilket bekræftede det molekylære docking-scenarie opnået fra simuleringer.
Endelig undersøgte forskerholdet effekten af Apt-7 på celleniveau ved at introducere molekylet til kræftceller. De observerede signifikant CYP24-hæmning for en cancercellelinje, der er kendt for at overudtrykke CYP24-enzymet, hvilket viser antiproliferativ aktivitet. Citerer Biyani og kolleger, disse resultater "klart karakteriserede og foreslog, at et DNA-aptamer-baseret molekyle kunne være en lovende hovedkandidat til anticancerterapi." + Udforsk yderligere
Forskere udvikler en ny beregningsmodel til generering af aptamer med brede applikationer
 Varme artikler
Varme artikler
-
 Forskere foreslår en ny strategi for elektrokemisk reduktion af kuldioxidDifferentialladningsdiagrammet for SnS/Aminated-C for (a) og den delvise strømtæthed af formiatproduktion for SnS og SnS/Aminated-C for (b). Kredit:CHEN Zhipeng Kuldioxid (CO 2 ) emission er ble
Forskere foreslår en ny strategi for elektrokemisk reduktion af kuldioxidDifferentialladningsdiagrammet for SnS/Aminated-C for (a) og den delvise strømtæthed af formiatproduktion for SnS og SnS/Aminated-C for (b). Kredit:CHEN Zhipeng Kuldioxid (CO 2 ) emission er ble -
 Cryo-EM afslører kronelignende struktur af protein, der er ansvarlig for at regulere blodgennemstrø…Human TRPM4 bundet med agonisten Ca+ og modulator DVT ved 3,8 Å. Kredit:Wei Lü, Ph.D. Et hold ledet af forskere ved Van Andel Research Institute (VARI) har for første gang afsløret strukturen på a
Cryo-EM afslører kronelignende struktur af protein, der er ansvarlig for at regulere blodgennemstrø…Human TRPM4 bundet med agonisten Ca+ og modulator DVT ved 3,8 Å. Kredit:Wei Lü, Ph.D. Et hold ledet af forskere ved Van Andel Research Institute (VARI) har for første gang afsløret strukturen på a -
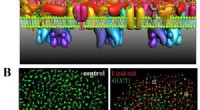 Super-opløsning billeddannelse afslører mekanisme af GLUT1 klyngedannelseA) Dette er PLLPI-modellen af cellemembranen. B) dSTORM-billeder af GLUT1 på cellemembranen; GLUT1 og lipid rafts; og GLUT1-fordeling efter MβCD- og NaN3-behandling. Skala barer, 5 μm. Kredit:GAO Ji
Super-opløsning billeddannelse afslører mekanisme af GLUT1 klyngedannelseA) Dette er PLLPI-modellen af cellemembranen. B) dSTORM-billeder af GLUT1 på cellemembranen; GLUT1 og lipid rafts; og GLUT1-fordeling efter MβCD- og NaN3-behandling. Skala barer, 5 μm. Kredit:GAO Ji -
 Visualisering af hvert trin i cycloaddition-reaktioner på overfladenScanning af tunnelmikroskopibilleder af halogenerede aromatiske forstadier deponeret på en sølvoverflade. Individuelle atomer kan ses i disse billeder. Kredit:WILEY-VCH Verlag GmbH &Co. KGaA, Weinheim
Visualisering af hvert trin i cycloaddition-reaktioner på overfladenScanning af tunnelmikroskopibilleder af halogenerede aromatiske forstadier deponeret på en sølvoverflade. Individuelle atomer kan ses i disse billeder. Kredit:WILEY-VCH Verlag GmbH &Co. KGaA, Weinheim
- Hvordan Minnesotas lille, forurenede Crow River overskygger Mississippi
- At finde en ny måde at bekæmpe sepsis i sen fase ved at øge cellernes antibakterielle egenskaber
- Forskere forbedrer processen til at omdanne svært genanvendeligt plastikaffald til brændstof
- Samtidig overvågning af overflader og proteinfordeling i celler
- Selvkørende laboratorium fremskynder forskning, syntese af energimaterialer
- Mars:kirkegård for ødelagte drømme og landere


