Ny undersøgelse tilbyder en renere vej til at kontrollere vand og omdanne drivhusgasser
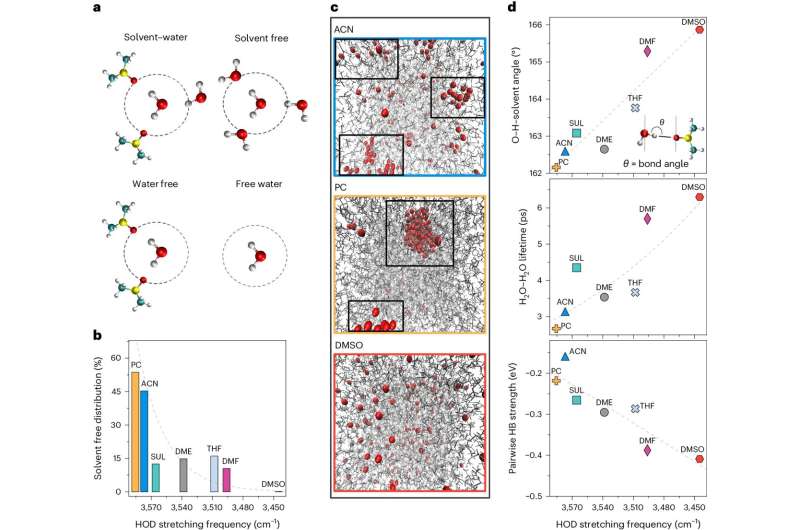
Forskere, der ønsker at omdanne kuldioxid til rene brændstoffer og nyttige kemikalier, laver ofte brintgas og karbonater som uønskede biprodukter. Et nyt papir fra UChicago Pritzker School of Molecular Engineering har fundet en renere vej.
Kuldioxid er drivhusgassen, der alene er ansvarlig for 78 % af ændringen i energibalancen i Jordens atmosfære mellem 1990 og 2022.
Et biprodukt af afbrænding af fossile brændstoffer, kuldioxid kommer ind i atmosfæren fra biludstødning og kulfyrede kraftværker. Selv nogle vedvarende energiressourcer producerer en lille mængde kuldioxid, selvom det er en lille brøkdel af den mængde kul og naturgas skaber.
I sin kerne er dette molekyle blot et arrangement af et kulstof- og to oxygenatomer, der kan reorganiseres gennem en proces kaldet elektrokemisk kuldioxidreduktion (CO2 R) til rene brændstoffer og nyttige kemikalier. Men processen foregår ofte med tab, hvor konkurrerende processer trækker atomerne i uønskede retninger, der skaber uønskede biprodukter.
I et papir offentliggjort i dag i Nature Catalysis , skitserede forskere fra UChicago Pritzker School of Molecular Engineerings Amanchukwu Lab en måde at manipulere vandmolekyler for at lave CO2 R mere effektiv med det ultimative mål at skabe en ren energisløjfe.
Gennem deres nye metode var holdet i stand til at udføre CO2 R med næsten 100 % effektivitet under mildt sure forhold, med enten guld eller zink som katalysatorer.
"Forestil dig, at vi kan have grøn elektricitet fra sol og vind, og så bruge denne elektricitet til at omdanne eventuel kuldioxid tilbage til brændstoffer," sagde PME Ph.D. kandidat Reggie Gomes, første forfatter til det nye papir.
Konkurrerer med HER
Elektrokemisk adskillelse af et molekyle er som pauseskuddet i et spil pool. Det tidligere arrangement forsvinder, og boldene spredes ud over bordet og falder til ro i nye kombinationer – ikke altid dem, spilleren havde til hensigt.
På samme måde udfører forskere CO2 R bruge el og vand til at bryde op og omorganisere den skadelige drivhusgas. Dette sender kulstof- og iltatomer fra kuldioxiden, der karomerer hen over bordet med brintatomer fra vandet.
Hvis det virker efter hensigten, danner atomerne andre, mere ønskværdige molekyler, der kan bruges som brændstoffer eller kemikalier.
Men efterhånden som atomerne spredes, dannes der ofte stabile parringer af to brintatomer, en proces kaldet hydrogenudviklingsreaktionen (HER). Dette gør CO2 R mindre effektiv, da energi og atomer, der bliver til brintgas, ikke kan være en del af de molekyler, forskerne forsøgte at skabe.
Selv i små mængder vand, CO2 R konkurrerer altid med HENDE.
Amanchukwu Lab – som er mest bemærkelsesværdigt for sin batteriforskning – anvendte indsigt fra vandige batterier på problemet, idet den antog, at kontrol af vandet med organiske opløsningsmidler kunne give en løsning.
Alt det glimter
Begge CO2 R og HER er afhængige af vand som protondonor. Ved hjælp af organiske opløsningsmidler og syretilsætningsstoffer var holdet i stand til at justere vandets adfærd og finde det søde sted, hvor det donerede den rigtige mængde protoner til at skabe de tilsigtede molekyler, ikke brintgassen og andre uønskede materialer som karbonater.
"I generel kemi lærer vi, at kuldioxid reagerer med hydroxid og danner carbonat. Det er uønsket, fordi det udtømmer det molekyle, vi ønsker at værdiansætte," sagde Neubauer Family Assistant Professor of Molecular Engineering Chibueze Amanchukwu.
Mange af de mest effektive måder at udføre CO2 på R stole på ædle metaller.
"Platin, sølv, guld - til forskningsformål er de gode katalysatorer," sagde Gomes. "De er meget stabile materialer. Men når du tænker på industrielle applikationer, bliver de uoverkommelige."
Ved at konstruere elektrolytten kan den nye metode opnå lignende resultater ved at bruge billigere, mere rigelige materialer.
"Lige nu er den bedste måde at gøre dette på elektrokemisk ved stuetemperatur at bruge ædelmetaller. Guld og sølv kan undertrykke hydrogenudviklingsreaktionen en lille smule," sagde Amanchukwu. "På grund af vores opdagelse kan vi nu bruge et jordrigt metal, zink, fordi vi nu har en separat måde at kontrollere vand på."
Flere oplysninger: Reginaldo J. Gomes et al., Modulering af vandhydrogenbinding i et ikke-vandigt miljø styrer dets reaktivitet i elektrokemiske transformationer, Nature Catalysis (2024). DOI:10.1038/s41929-024-01162-z
Journaloplysninger: Naturkatalyse
Leveret af University of Chicago
 Varme artikler
Varme artikler
-
 Kemiker udvikler blomsterlignende katalysatorer fra grafenKredit:RUDN University En RUDN -kemiker og kolleger fra Iran har udviklet en ny strategi til fremstilling af hule, porøse katalysatorer til Heck -koblingsreaktionen. Disse katalysatorer er kendete
Kemiker udvikler blomsterlignende katalysatorer fra grafenKredit:RUDN University En RUDN -kemiker og kolleger fra Iran har udviklet en ny strategi til fremstilling af hule, porøse katalysatorer til Heck -koblingsreaktionen. Disse katalysatorer er kendete -
 Den nyopdagede arkitektur af et kobber-nitrenoid kompleks kan revolutionere kemisk synteseBetley og hans team af samarbejdspartnere har karakteriseret arkitekturen af et kobber-nitrenoid kompleks, en katalysator jaget i over et halvt århundrede. Kredit:Harvard University At lave sæbe
Den nyopdagede arkitektur af et kobber-nitrenoid kompleks kan revolutionere kemisk synteseBetley og hans team af samarbejdspartnere har karakteriseret arkitekturen af et kobber-nitrenoid kompleks, en katalysator jaget i over et halvt århundrede. Kredit:Harvard University At lave sæbe -
 Undersøgelse ser til is for at fremstille nyttige porøse materialerXiao Cheng Zeng (til venstre) og Chonqin Zhou. Kredit:University of Nebraska-Lincoln At opdage en måde at udnytte isrekrystallisering på kunne muliggøre fremstilling af højeffektive materialer til
Undersøgelse ser til is for at fremstille nyttige porøse materialerXiao Cheng Zeng (til venstre) og Chonqin Zhou. Kredit:University of Nebraska-Lincoln At opdage en måde at udnytte isrekrystallisering på kunne muliggøre fremstilling af højeffektive materialer til -
 Forskere genopdager hurtigtvirkende tysk insekticid tabt i kølvandet på Anden VerdenskrigEn monofluoranalog af DDT, set gennem et optisk mikroskop. Faste fluorerede former for DDT dræbte insekter hurtigere end DDT. Kredit:Xiaolong Zhu og Jingxiang Yang, NYU Institut for Kemi En ny und
Forskere genopdager hurtigtvirkende tysk insekticid tabt i kølvandet på Anden VerdenskrigEn monofluoranalog af DDT, set gennem et optisk mikroskop. Faste fluorerede former for DDT dræbte insekter hurtigere end DDT. Kredit:Xiaolong Zhu og Jingxiang Yang, NYU Institut for Kemi En ny und
- NASA-NOAAs Suomi NPP-satellit finder den tropiske storm Noul ved at falme over Laos
- At lære børn at læse under coronavirus-pandemien:5 spørgsmål besvaret
- Dette er nanowood, en opfindelse, der kunne reducere menneskehedens CO2-fodaftryk
- Observationer kaster mere lys over atmosfæren i den hvide dværg GD 424
- Hvad er de to grundfamilier af enkle maskiner?
- Smeltning af Himalaya -gletsjere er fordoblet i de seneste år


