Forskere finder nye måder at omdanne inhibitorer til nedbrydere, hvilket baner vejen for fremtidige lægemiddelopdagelser
Forskere har opdaget måder, hvorpå man kan omdanne inhibitor-stil målrettede kræftlægemidler til små molekyler kendt som nedbrydere, som hjælper med at ødelægge kræftfremmende proteiner i celler.
Forskerne udvalgte molekyler, der vides at hæmme visse proteiner – stopper deres funktion – og modificerede dem på forskellige måder for at omdanne dem til proteinnedbrydere, som nedbryder proteinet.
Andre videnskabsmænd kan nu kopiere denne nye tilgang til at udvikle og optimere en række proteinnedbrydende produkter. På lang sigt kan dette hjælpe med at gøre eksisterende kræftbehandlinger mere effektive og skabe nye behandlinger for at målrette mod forskellige proteiner involveret i kræft, herunder proteiner, der tidligere kan være blevet betragtet som "umodtagelige."
Forskningen, som blev ledet af forskere ved The Institute of Cancer Research, London, er offentliggjort i ACS Chemical Biology .
Behovet for at optimere målrettet proteinnedbrydning
Forskere verden over har undersøgt målrettet proteinnedbrydning som en måde at eliminere specifikke proteiner, der vides at spille en rolle i udviklingen eller progressionen af kræft. Celler nedbryder naturligt beskadigede eller unødvendige proteiner, og det er muligt at kapere denne proces ved at introducere de rigtige lægemiddelmolekyler, så cellerne ødelægger kræftproteiner.
ICR er forpligtet til at forske i målrettet proteinnedbrydning som en måde at opdage nye kræftbehandlinger på. I 2022 gjorde en stor filantropisk donation det muligt at åbne et nyt Center for Proteinnedbrydning inden for ICR's Center for Cancer Drug Discovery.
Forskere har allerede opnået en vis succes ved at bruge proteolysemålrettede kimærer (PROTAC'er). Disse binder til både proteinet af interesse og et enzym kaldet en E3 ubiquitin-ligase for at bringe de to tæt sammen. Enzymet mærker derefter proteinet med ubiquitin, som markerer det til ødelæggelse af cellen.
Imidlertid begrænser den relativt høje molekylvægt af PROTAC'er deres anvendelse, da de ikke opløses godt i vand og kan kæmpe for at komme ind i celler i en høj nok koncentration til at være effektive. Omvendt, hvis koncentrationen bliver for høj, binder PROTAC'erne alle til kun én af de to forbindelser - enzymet eller målproteinet - i stedet for begge, hvilket betyder, at proteinnedbrydningen er ufuldstændig.
En nyere opdagelse har været brugen af monovalente nedbrydningsmidler, ofte omtalt som molekylære lime. Disse virker på samme måde som PROTAC'er, men de modificerer kemisk overfladen af enten enzymet eller målproteinet, så de to direkte kan binde. Disse forbindelser overvinder begrænsningerne ved PROTAC'er, fordi de er mindre og stadig effektive ved højere koncentrationer.
Et molekylært lim-lægemiddel, opdaget efter et forskningsprogram på ICR, er allerede i tidlig fase af kliniske forsøg.
Forvandling af inhibitorer til nedbrydere
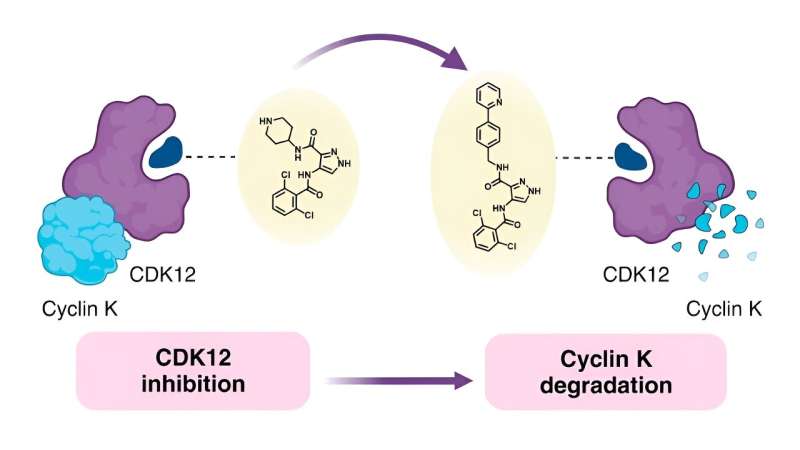
Da de ønskede at forstå sammenhængen mellem den kemiske struktur af molekylære lime, og hvordan de opfører sig - kendt som struktur-aktivitetsforholdet (SAR) - besluttede forskerne bag det aktuelle studie at bruge en kendt monovalent nedbryder kaldet CR8 som udgangspunkt. CR8 hæmmer alle cyclin-afhængige kinaser (CDK'er), som har flere roller i tumorudvikling, men det nedbryder også proteinet cyclin K, som fremmer kræftsignalveje.
Tidligere forskning har vist, at CR8 binder til CDK12 og en E3-ligasekomponent kaldet beskadiget DNA-bindende protein 1 (DDB1). Dette gør det muligt for cellen at nedbryde cyclin K bundet til CDK12.
Bevæbnet med denne information forsøgte holdet at erstatte pyridinet i CR8 med en bred vifte af erstatninger. De forsøgte først at bruge simple grupper, herunder fluor, methyl og hydroxy, før de gik videre til mere komplekse formationer for at bestemme, hvordan disse ændringer påvirkede nedbrydningsevnen.
I den anden del af undersøgelsen anvendte forskerne deres øgede forståelse af nedbryder SAR til andre CDK-hæmmere for at afgøre, om deres resultater kunne overføres. De fandt ud af, at molekylære komponenter, der inducerede proteinnedbrydning, kunne bruges til at omdanne flere forskellige inhibitorer til nedbrydere. De identificerede også visse erstatninger, der førte til forbedret nedbrydning.
Førsteforfatter Katie Thomas, en ph.d. studerende i afdelingen for kræftterapi ved ICR, sagde:"Det var overraskende at se, at en så bred vifte af grupper kunne bruges til at inducere cyclin K-nedbrydning. Dette betyder, at interaktionsgrænsefladen mellem degrader bound-CDK12 og DDB1 ikke skal være perfekt optimeret, for at nedbrydning kan ske. Dette er lovende for fremtiden med at bruge monovalente lime som terapeutiske modaliteter – det vil hjælpe os med at udvikle molekyler fra opdagelse til optimering."
Nedbrydere er mere effektive end hæmmere
Proteinkinasehæmmere er blevet brugt i kræftbehandling i mere end to årtier. De virker ved at blokere virkningen af proteinkinaser, enzymer, der styrer proteinernes funktion og kan føre til ureguleret cellevækst, hvis de bliver muterede.
Selvom disse behandlinger kan fungere godt, er der risiko for, at kræften bliver resistent over for dem. Dette skyldes, at inhibitorer blokerer kræftrelaterede proteiner i stedet for at ødelægge dem, og tumorcellerne kan nogle gange genaktivere dem.
Derudover, når nogle proteinkinaser blokeres af inhibitorer, kompenserer cellen ved at bruge andre kinaser til at udføre de samme handlinger.
At slippe af med proteinerne helt gennem proteinnedbrydning fjerner disse risici.
Et grundlag for videre arbejde
Denne undersøgelse tjener som udgangspunkt for andre forskere, der søger at designe molekylære lime, identificere lovende proteinmål for nedbrydning og udvikle nye molekyler, der kan fungere som nedbrydningsterapier.
Thomas sagde:"Vi antager, at andre små molekylehæmmere kan omdannes til nedbrydere gennem tilføjelse af visse grupper. Vores team undersøger i øjeblikket, om visse grupper kan forbindes med andre typer kinaseinhibitorer for at gøre dem til monovalente nedbrydere. Arbejdet er også i gang for at afgøre, om disse forbindelser kan nedbryde andre proteiner."
I teorien vil det være muligt at fjerne en række kræftfremmende proteiner på tværs af forskellige typer kræft, når forskerne har opnået en fuld forståelse af nedbryder SAR. Denne tilgang kunne derfor åbne døren til nye effektive kræftbehandlinger.
Tilsvarende forfatter Dr. Benjamin Bellenie, Senior Staff Scientist i afdelingen for Cancer Therapeutics ved ICR, sagde:"Denne undersøgelse har væsentligt forbedret vores forståelse omkring designet af monovalente nedbrydningsmidler. Vi har fokuseret specifikt på cyclin K-nedbrydere og er nødt til at træne. om vi kan kopiere denne tilgang til nye mål, men vi mener, at vores forskning kan muliggøre fremtidige lægemiddelopdagelser."
Flere oplysninger: Katie L. Thomas et al., Degradation by Design:New Cyclin K Degraders from Old CDK Inhibitors, ACS Chemical Biology (2024). DOI:10.1021/acschembio.3c00616
Journaloplysninger: ACS Kemisk Biologi
Leveret af Institute of Cancer Research
 Varme artikler
Varme artikler
-
 Frugtkagestruktur observeret i organiske polymererForskere har analyseret egenskaberne af en organisk polymer med potentielle anvendelser i fleksibel elektronik og afdækket variationer i hårdhed på nanoskala, første gang en så fin struktur er blevet
Frugtkagestruktur observeret i organiske polymererForskere har analyseret egenskaberne af en organisk polymer med potentielle anvendelser i fleksibel elektronik og afdækket variationer i hårdhed på nanoskala, første gang en så fin struktur er blevet -
 Overraskende opdagelse af celledød giver fingerpeg om fødselsdefekterForskere har gjort en overraskende opdagelse, der kunne omskrive vores forståelse af den rolle, programmeret celledød spiller i embryonisk udvikling og medfødte fosterskader. ledet af Dr. Francine Ke
Overraskende opdagelse af celledød giver fingerpeg om fødselsdefekterForskere har gjort en overraskende opdagelse, der kunne omskrive vores forståelse af den rolle, programmeret celledød spiller i embryonisk udvikling og medfødte fosterskader. ledet af Dr. Francine Ke -
 Hvordan stabilisering af forstyrrede proteiner kan føre til den næste generation af medicinske app…LCST IDPPer udviser en bred vifte af hysteretisk faseadfærd. (A) Analyse af den reversible faseadfærd af LCST IDPPer i vores bibliotek afslørede tre grupper af gentagne motiver, hvor motiver i hver gr
Hvordan stabilisering af forstyrrede proteiner kan føre til den næste generation af medicinske app…LCST IDPPer udviser en bred vifte af hysteretisk faseadfærd. (A) Analyse af den reversible faseadfærd af LCST IDPPer i vores bibliotek afslørede tre grupper af gentagne motiver, hvor motiver i hver gr -
 Nye gelbelægninger kan føre til bedre katetre og kondomerMIT ingeniører har designet et gel-lignende materiale, der kan belægges på standard plast- eller gummienheder, giver en blødere, mere glat ydre, der betydeligt kan lette en patients ubehag under opera
Nye gelbelægninger kan føre til bedre katetre og kondomerMIT ingeniører har designet et gel-lignende materiale, der kan belægges på standard plast- eller gummienheder, giver en blødere, mere glat ydre, der betydeligt kan lette en patients ubehag under opera
- Nye kemiske forbindelser gør katalysatorer mere effektive
- Kønsstereotyper begrænser kvindelige præsidenters magt på tværs af kulturer, undersøgelse vise…
- Fysikere kaster lys over sjældent set metalbearbejdningsteknik fra 1500-tallet
- Hvorfor polariserede politikere bedst kan repræsentere borgerne
- Ny forklaring forbinder konkurrerende teorier om oprindelsen af antarktisk istid, fremhæver kompl…
- Fireweed:The Pink Pioneer


