Ny teknik giver indsigt i, hvordan proteiner involveret i cellulære processer kommunikerer via ekstracellulære vesikler
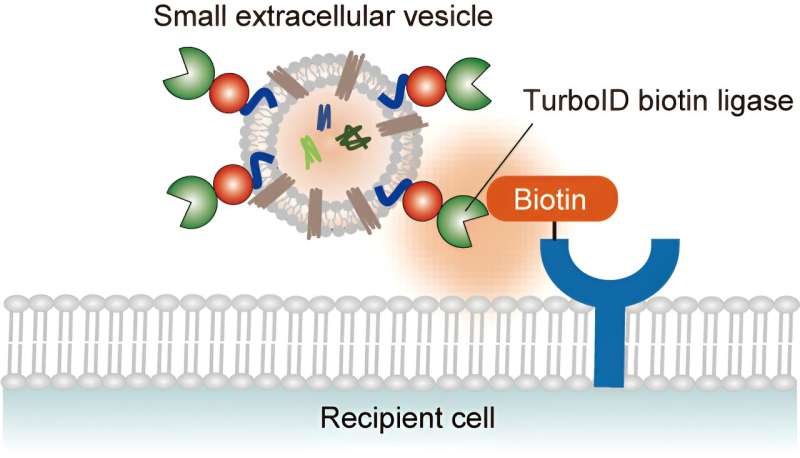
En måde, hvorpå celler kommunikerer med hinanden, er gennem sekretion og optagelse af ekstracellulære vesikler (EV'er). Elbiler transporterer et væld af laster, herunder proteiner, lipider og nukleinsyrer. Deres optagelse påvirker funktionen af modtagerceller ved at påvirke signalprocesser og genekspression.
På trods af omfattende undersøgelser af elbiler vides der ikke meget om deres cellespecifikke optagelse af modtagerceller.
"Det er afgørende at forstå, hvordan modtagerceller optager elbiler, for at dechifrere de bredere mekanismer, der styrer celle-til-celle kommunikation i cellulære processer i både sundhed og sygdom," forklarer Koshi Imami fra RIKEN Center for Integrative Medical Sciences.
Imami og kolleger har nu udviklet en ny metode til at spore interaktionen mellem elbiler og modtagerceller. TurboID-EV-systemet virker ved at mærke modtagerens cellulære proteiner tæt på EV'er med biotin (vitamin B7). Forskningen er publiceret i tidsskriftet Analytical Chemistry .
"I modsætning til traditionelle teknikker, der mærker EV'er med fluorescerende proteiner eller bruger mikroskopi, giver vores metode et globalt overblik over proteiner involveret i EV-optagelse og interaktioner i modtagerceller," siger Imami.
Ved at identificere de biotinmærkede proteiner ved hjælp af biokemisk berigelse og massespektrometri kan forskerne samle spor i de molekylære mekanismer, der ligger til grund for EV-optagelse.
Imami og kolleger udtrykte en biotinligase, der er konstrueret til at fusionere med EV-membraner i humane embryonale nyreceller uden at forstyrre EV-sekretion. Ved at indsamle udskilte TurboID-EV'er og inkubere dem med modtagerceller mærket med tunge aminosyrer og suppleret med biotin, kunne de undersøge biotinyleringsbegivenheder, der opstår under optagelsen af EV'er.
Forskerne identificerede mere end 450 biotinylerede recipientproteiner. De inkluderede velkendte involveret i den proces, hvorved celler opsluger eksterne stoffer for at bringe dem ind. Holdet fandt også proteiner involveret i intracellulær transport og membran-associerede proteiner, som kunne være nøglen til EV-optagelse i denne model.
Metoden kan tilpasses til forskellige EV-undertyper og celletyper. "Vores alsidighed gør det muligt for forskere at undersøge specificiteten af EV-optagelsesmekanismer i mange biologiske sammenhænge," siger Imami.
At opdage de proteiner, der er involveret i EV-optagelse, kan fremme vores forståelse af, hvordan kræftceller spredes og hjælpe med at udvikle EV-baserede lægemiddelleveringssystemer, der målretter mod specifikke celletyper.
Imamis team forsøger nu at anvende TurboID-EV-systemet til en musemodel for at forstå, hvordan kræft spredes mellem organer. "Tumor-afledte EV'er er kendt for at blive optaget af organspecifikke celler for at forberede sig på, at kræft kan sprede sig til nye organer," forklarer Imami. "Vi ønsker at karakterisere funktionen af disse elbiler."
Flere oplysninger: Yuka Li et al., TurboID-EV:Proteomisk kortlægning af recipientcellulære proteiner proksimalt til små ekstracellulære vesikler, analytisk kemi (2023). DOI:10.1021/acs.analchem.3c01015
Journaloplysninger: Analytisk kemi
Leveret af RIKEN
 Varme artikler
Varme artikler
-
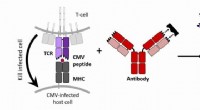 Udstyrelse af T -celleceptorer til bekæmpelse af en udbredt og undertiden dødelig virusT-celler er dygtige til at dræbe cytomegalovirus (CMV)-inficerede celler i kraft af en T-cellereceptor (TCR), der genkender intracellulære CMV-associerede proteiner, der bliver præsenteret på celleove
Udstyrelse af T -celleceptorer til bekæmpelse af en udbredt og undertiden dødelig virusT-celler er dygtige til at dræbe cytomegalovirus (CMV)-inficerede celler i kraft af en T-cellereceptor (TCR), der genkender intracellulære CMV-associerede proteiner, der bliver præsenteret på celleove -
 Pesticid, der er dødeligt for bier, kan nu let opdages i honningProfessor Janusz Pawliszyn forvandlede sin græsplæne til en vildblomsteng for at tiltrække bier. Kredit:Janusz Pawliszyn Et almindeligt insekticid, der er en stor fare for honningbier, er nu effek
Pesticid, der er dødeligt for bier, kan nu let opdages i honningProfessor Janusz Pawliszyn forvandlede sin græsplæne til en vildblomsteng for at tiltrække bier. Kredit:Janusz Pawliszyn Et almindeligt insekticid, der er en stor fare for honningbier, er nu effek -
 Radikale trin mod ren indkapslingEn polymer, der både kan samle sig til stjerneformede nanopartikler og nedbrydes, når den ikke længere er nødvendig, kan påvirke kemisk indkapslingsteknologi. Kredit:Royal Society of Chemistry En
Radikale trin mod ren indkapslingEn polymer, der både kan samle sig til stjerneformede nanopartikler og nedbrydes, når den ikke længere er nødvendig, kan påvirke kemisk indkapslingsteknologi. Kredit:Royal Society of Chemistry En -
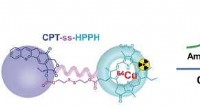 Nanopartikler med multifunktionel lægemiddelprecursor til synergistisk tumorterapiKredit:Wiley Til effektiv kræftbehandling med få bivirkninger, det aktive lægemiddel bør selektivt opnå høj koncentration i tumoren. I journalen Angewandte Chemie , videnskabsmænd har introducer
Nanopartikler med multifunktionel lægemiddelprecursor til synergistisk tumorterapiKredit:Wiley Til effektiv kræftbehandling med få bivirkninger, det aktive lægemiddel bør selektivt opnå høj koncentration i tumoren. I journalen Angewandte Chemie , videnskabsmænd har introducer
- Forskere tager et skridt i retning af at udvide brugen af magnetiske væsker i medicin
- Hvad mener forskningsorganisationer om open access publicering?
- Forskning bekræfter, at ingrediens i husholdningsrens kan forbedre fusionsreaktioner
- Boligustabilitet underminerer folkesundhedens reaktion på COVID-19-pandemien
- Sporer oprindelsen af det sydlige Californiens seneste invasive skadedyr
- Billede:ESA centrifuge


