Betydningen af hydrogenbinding
Hydrogenbinding er vigtig i mange kemiske processer. Hydrogenbinding er ansvarlig for vandets unikke opløsningsmiddelegenskaber. Hydrogenbindinger holder komplementære DNA-tråde sammen, og de er ansvarlige for at bestemme den tredimensionelle struktur af foldede proteiner, inklusive enzymer og antistoffer.
Et eksempel: Vand
En enkel måde at forklare brintbindinger er med vand. Vandmolekylet består af to hydrogener, der er kovalent bundet til et ilt. Da ilt er mere elektronegativt end brint, trækker ilt de delte elektroner tættere på sig selv. Dette giver oxygenatomet en lidt mere negativ ladning end nogen af hydrogenatomerne. Denne ubalance kaldes en dipol, hvilket får vandmolekylet til at have en positiv og negativ side, næsten som en lille magnet. Vandmolekyler justeres, så brintet på det ene molekyle står over for iltet på et andet molekyle. Dette giver vandet en større viskositet og tillader også vand at opløse andre molekyler, der enten har en lidt positiv eller negativ ladning.
Proteinfoldning
Proteinstruktur bestemmes delvist af hydrogenbinding. Hydrogenbindinger kan forekomme mellem et brint på en amin og et elektronegativt element, såsom ilt på en anden rest. Når et protein foldes på plads, "sætter" en serie af hydrogenbinding molekylet sammen og holder det i en bestemt tredimensionel form, der giver proteinet sin særlige funktion.
DNA
Hydrogenbindinger holder komplementære tråde af DNA sammen. Nukleotider parrer nøjagtigt på baggrund af placeringen af tilgængelige brintbindingsdonorer (tilgængelige, let positive hydrogener) og brintbindingsacceptorer (elektronegative oxygener). Nukleotidthyminet har en donor og et acceptorsted, der parrer perfekt med nukleotidadenens komplementære acceptor og donorsted. Cytosin parrer perfekt med guanin gennem tre hydrogenbindinger.
Antistoffer
Antistoffer er foldede proteinstrukturer, der præcist målretter mod og passer til et specifikt antigen. Når antistoffet er produceret og opnår sin tredimensionelle form (hjulpet med hydrogenbinding), vil antistoffet konforme sig som en nøgle i en lås til dets specifikke antigen. Antistoffet låser sig fast på antigenet gennem en række interaktioner, herunder hydrogenbindinger. Den menneskelige krop har kapacitet til at producere over ti milliarder forskellige typer antistoffer i en immunreaktion.
Chelation
Mens individuelle brintbindinger ikke er særlig stærke, er en række hydrogenbindinger meget sikker. Når et molekyle brint bindes gennem to eller flere steder med et andet molekyle, dannes en ringstruktur kendt som et chelat. Chelerende forbindelser er nyttige til fjernelse eller mobilisering af molekyler og atomer såsom metaller.
Sidste artikelBetydningen af en periodisk tabel
Næste artikelSådan identificeres, om en opløsning er neutral, base eller syre
 Varme artikler
Varme artikler
-
 Hvad er forskellene mellem blegemiddel og klor?Blegemiddel henviser til mange produkter med anvendelser, der spænder fra blegning af tøj til dræbning af bakterier til fremstilling af papir. Blegemidler fungerer ved at ændre kemiske forbindelser, e
Hvad er forskellene mellem blegemiddel og klor?Blegemiddel henviser til mange produkter med anvendelser, der spænder fra blegning af tøj til dræbning af bakterier til fremstilling af papir. Blegemidler fungerer ved at ændre kemiske forbindelser, e -
 Hvad er pH i saltvand?pH-skalaen bruges til at måle alkalinitet eller surhed i et stof som vand. Skalaen går fra 0 til 14. En pH-værdi under 7 indikerer, at det, du måler, er surt, og alt over 7 er alkalisk. Hvis et stof h
Hvad er pH i saltvand?pH-skalaen bruges til at måle alkalinitet eller surhed i et stof som vand. Skalaen går fra 0 til 14. En pH-værdi under 7 indikerer, at det, du måler, er surt, og alt over 7 er alkalisk. Hvis et stof h -
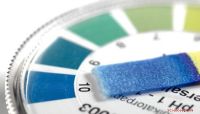 Sådan bruges lakmuspapirerNår du vil bestemme surhedsgraden eller alkaliteten af en flydende eller vandopløselig gas, er den nemmeste måde at udføre en lakmustest. Testen kræver lakmuspapir, som er smalle strimler af papir b
Sådan bruges lakmuspapirerNår du vil bestemme surhedsgraden eller alkaliteten af en flydende eller vandopløselig gas, er den nemmeste måde at udføre en lakmustest. Testen kræver lakmuspapir, som er smalle strimler af papir b -
 Hvad sker der i en Lewis-syre-basereaktion?I en Lewis-syre-base-reaktion accepterer syren elektroner, mens basen donerer elektroner. Dette syn på syrer og baser gør det muligt for kemikere at forstå bedre opførsel af stoffer, der ikke passer i
Hvad sker der i en Lewis-syre-basereaktion?I en Lewis-syre-base-reaktion accepterer syren elektroner, mens basen donerer elektroner. Dette syn på syrer og baser gør det muligt for kemikere at forstå bedre opførsel af stoffer, der ikke passer i


