Hvor mange atomer er der i en ilttank?
Ved STP fylder et mol af enhver gas cirka 22,4 liter volumen. Et mol oxygengas indeholder 6,02214076 × 10^23 oxygenmolekyler (kendt som Avogadros tal). Hvert iltmolekyle består af to iltatomer. Derfor indeholder et mol iltgas 2 × 6,02214076 × 10^23 =1,204428152 × 10^24 oxygenatomer.
Så hvis vi har en beholder med iltgas ved STP med et volumen på for eksempel 1 liter, kan vi estimere antallet af iltatomer i den beholder ved at bestemme brøkdelen af 1 liter sammenlignet med standardvolumenet på 22,4 liter. For en 1-liters beholder er fraktionen 1/22,4 ≈ 0,0446.
Hvis vi multiplicerer denne fraktion med antallet af atomer i et mol iltgas, får vi:
Antal oxygenatomer i 1 liter gas ved STP ≈ 0,0446 × 1,204428152 × 10^24 ≈ 5,36 × 10^22 atomer
Denne beregning forudsætter ideel gasadfærd og tager ikke højde for eventuelle afvigelser på grund af interaktioner mellem gasmolekyler eller iltens specifikke egenskaber. For mere præcise beregninger, især for ikke-ideelle gasser eller forskellige temperatur- og trykforhold, er det nødvendigt at bruge passende ligninger og overveje gassens specifikke egenskaber.
 Varme artikler
Varme artikler
-
 Teknologi, der detekterer RNase-aktivitetNanoskala (udgave 42, 2017). Kredit:KAIST Et KAIST forskerhold af professor Hyun Gyu Park ved Institut for Kemi og Biomolekylær Teknik udviklede en ny teknologi til at detektere aktiviteten af
Teknologi, der detekterer RNase-aktivitetNanoskala (udgave 42, 2017). Kredit:KAIST Et KAIST forskerhold af professor Hyun Gyu Park ved Institut for Kemi og Biomolekylær Teknik udviklede en ny teknologi til at detektere aktiviteten af -
 At finde unikke lægemiddelstrukturer med kunstig intelligens og kemiKredit:CC0 Public Domain I jagten på ny medicin mod sygdomme som kræft, et Leiden-team har udviklet en ny arbejdsgang. Denne tilgang kombinerer kunstig intelligens (AI) med molekylær modellering o
At finde unikke lægemiddelstrukturer med kunstig intelligens og kemiKredit:CC0 Public Domain I jagten på ny medicin mod sygdomme som kræft, et Leiden-team har udviklet en ny arbejdsgang. Denne tilgang kombinerer kunstig intelligens (AI) med molekylær modellering o -
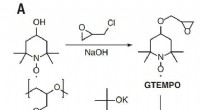 Forskere viser den højeste rapporterede ledningsevne for organisk radikal polymerDen monomersyntese og ringåbningspolymerisationsbaserede syntetiske skema, der bruges til at generere PTEO-radikalpolymeren. Kredit: Videnskab (2018). DOI:10.1126/science.aao7287 Et team af forsk
Forskere viser den højeste rapporterede ledningsevne for organisk radikal polymerDen monomersyntese og ringåbningspolymerisationsbaserede syntetiske skema, der bruges til at generere PTEO-radikalpolymeren. Kredit: Videnskab (2018). DOI:10.1126/science.aao7287 Et team af forsk -
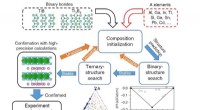 Find en nål i en høstak:Opdagelse af Ti2InB2 til syntetisering af lagdelt TiBMed strategien afbildet, det var muligt at foretage en teoretisk søgning med tusinder af indledende kandidater for endelig at opnå de bedste to MAX -faser for den potentielle syntese af TiB MXenes, so
Find en nål i en høstak:Opdagelse af Ti2InB2 til syntetisering af lagdelt TiBMed strategien afbildet, det var muligt at foretage en teoretisk søgning med tusinder af indledende kandidater for endelig at opnå de bedste to MAX -faser for den potentielle syntese af TiB MXenes, so
- Økologiske landbrugsfordele i biodiversitet og overskud afhænger af beliggenhed
- Nanopore-teknologi opnår gennembrud inden for påvisning af proteinvarianter
- Nye forbindelser opdaget i marine svampe kan dræbe lægemiddelresistente bakterier
- Hvordan man dræber europæiske Hornets
- Gamle afføring hjælper med at vise, at klimaændringer bidrog til Cahokias fald
- En partikel af en anden smag?


