Hvor mange molekyler er der i en 5,00 g prøve af dimethylkviksølv?
Avogadros tal er lig med 6,022 x 10^23 molekyler/mol, hvilket repræsenterer antallet af partikler (molekyler, atomer, ioner osv.), der er til stede i et mol af et stof.
Den molære masse af dimethylkviksølv (CH₃HgCH₃) kan beregnes ved at tilføje atommasserne af hvert atom i molekylet:
Molær masse af dimethylkviksølv =(2 x atommasse af C) + (2 x atommasse af H) + (2 x atommasse af Hg)
Molær masse af dimethylkviksølv =(2 x 12,01 g/mol) + (2 x 1,008 g/mol) + (2 x 200,59 g/mol)
Molær masse af dimethylkviksølv ≈ 406,62 g/mol
Nu kan vi beregne antallet af mol i en 5,00 g prøve af dimethylkviksølv ved hjælp af formlen:
Antal mol =masse af prøve / molær masse
Antal mol =5,00 g / 406,62 g/mol
Antal mol ≈ 0,0123 mol
Endelig kan vi beregne antallet af molekyler i 0,0123 mol dimethylkviksølv ved hjælp af Avogadros tal:
Antal molekyler =Antal mol x Avogadros antal
Antal molekyler ≈ 0,0123 mol x 6,022 x 10^23 molekyler/mol
Antal molekyler ≈ 7,43 x 10^21 molekyler
Derfor er der ca. 7,43 x 10^21 molekyler i en 5,00 g prøve af dimethylkviksølv.
Sidste artikelHvad er ekasilicons bindeevne?
Næste artikelHvilke grundstoffer er der i kaliumhydroxid?
 Varme artikler
Varme artikler
-
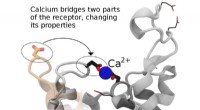 Forstå en celles dørklokkeFremme af design af lægemidler til bedre medicinske effekter kræver en kombination af eksperimentel og computersimuleringsforskning. Forskere ved Los Alamos National Laboratory, University of Toronto,
Forstå en celles dørklokkeFremme af design af lægemidler til bedre medicinske effekter kræver en kombination af eksperimentel og computersimuleringsforskning. Forskere ved Los Alamos National Laboratory, University of Toronto, -
 Forskere afslører, hvordan MRSA-bakterien håndterer stressEt internationalt hold af forskere har afsløret en grundlæggende mekanisme, der er ansvarlig for at håndtere stress hos stafylokokker, når de udsættes for antibiotika. Kredit:Ditlev E. Brodersen E
Forskere afslører, hvordan MRSA-bakterien håndterer stressEt internationalt hold af forskere har afsløret en grundlæggende mekanisme, der er ansvarlig for at håndtere stress hos stafylokokker, når de udsættes for antibiotika. Kredit:Ditlev E. Brodersen E -
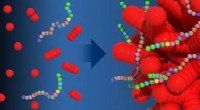 Koralformede nanopartikler bygget af design ved hjælp af konstruerede peptoiderI en ny undersøgelse ledet af PNNL-materialeforsker Chun-Long Chen, sekvensdefinerede peptoider (vist her som kæder af små farverige kugler) muliggjorde den forudsigelige morfologiske udvikling af sfæ
Koralformede nanopartikler bygget af design ved hjælp af konstruerede peptoiderI en ny undersøgelse ledet af PNNL-materialeforsker Chun-Long Chen, sekvensdefinerede peptoider (vist her som kæder af små farverige kugler) muliggjorde den forudsigelige morfologiske udvikling af sfæ -
 Patienter skal springe laboratoriet over, få øjeblikkelige resultater med ny blodprøveteknologiFørste mobile version af Enzyme Linked Immunosorbent Assay (ELISA), guldstandarden i biokemisk analyse. Kredit:Arsenii Zhdanov De ofte dyre, tidskrævende proces med at få blodprøver og urinanalyse
Patienter skal springe laboratoriet over, få øjeblikkelige resultater med ny blodprøveteknologiFørste mobile version af Enzyme Linked Immunosorbent Assay (ELISA), guldstandarden i biokemisk analyse. Kredit:Arsenii Zhdanov De ofte dyre, tidskrævende proces med at få blodprøver og urinanalyse
- Psykisk kontakt med UFO'er
- Forstadsdamme er en septisk buffet
- Hvordan vi opdagede, at Jordens indre kerne er ældre end tidligere antaget
- Racemæssig skævhed betyder noget på crowdfunding-sider som Indiegogo, Kickstarter, og GoFundMe
- Arktiske skyer meget følsomme over for luftforurening
- Hvad er reglerne for at multiplicere fraktioner?


