Hvor mange mol ioner produceres når 2 mol Na2CO3 dissocierer?
```
Na2CO3 (aq) → 2 Na+ (aq) + CO32- (aq)
```
Ud fra denne ligning kan vi se, at for hver 1 mol Na2CO3, der dissocierer, produceres 2 mol Na+ ioner og 1 mol CO32- ioner. Derfor, hvis 2 mol Na2CO3 dissocierer, kan vi beregne det samlede antal mol producerede ioner som følger:
Total mol af ioner =(2 mol Na2CO3) × (2 mol Na+ ioner/1 mol Na2CO3) + (2 mol Na2CO3) × (1 mol CO32- ioner/1 mol Na2CO3)
Totalt antal mol ioner =4 mol Na+ ioner + 2 mol CO32-ioner
Total mol ioner =6 mol ioner
Derfor, når 2 mol Na2CO3 dissocierer, dannes der i alt 6 mol ioner (4 mol Na+ ioner og 2 mol CO32- ioner).
Sidste artikelHvordan er bi- og hvepsestik relateret til sure baser?
Næste artikelHvad er forskellen mellem carbon 4 oxid og dioxid?
 Varme artikler
Varme artikler
-
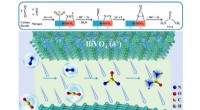 Nye katalysatorer forbedrer effektiviteten af urinstofsyntese ved omgivende betingelserDen skematiske elektrokatalytiske ureasyntesemekanisme baseret på Bi-BiVO 4 Mott-Schottky heterostruktur synergistiske effekter Kredit:Zhang Guangjin og Yuan Menglei Konvertering af både nitroge
Nye katalysatorer forbedrer effektiviteten af urinstofsyntese ved omgivende betingelserDen skematiske elektrokatalytiske ureasyntesemekanisme baseret på Bi-BiVO 4 Mott-Schottky heterostruktur synergistiske effekter Kredit:Zhang Guangjin og Yuan Menglei Konvertering af både nitroge -
 Fjernelse af bremser på planteolieproduktionBrug af biokemiske genetiske teknikker i plantecellekulturer, dette Brookhaven Lab-team evaluerer virkningerne af at frigive de biokemiske bremser på planteolieproduktionen. På billedet ses:Gruppelede
Fjernelse af bremser på planteolieproduktionBrug af biokemiske genetiske teknikker i plantecellekulturer, dette Brookhaven Lab-team evaluerer virkningerne af at frigive de biokemiske bremser på planteolieproduktionen. På billedet ses:Gruppelede -
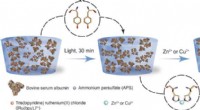 Kation-induceret formprogrammering og morphing i proteinbaserede hydrogelerSkema af fikseringsprocessen. (Venstre) BSA-baserede proteinhydrogeler fremstilles ved hjælp af en lysaktiveret reaktion, i nærværelse af ammoniumpersulfat (APS) og tris(bipyridin) ruthenium(II)chlori
Kation-induceret formprogrammering og morphing i proteinbaserede hydrogelerSkema af fikseringsprocessen. (Venstre) BSA-baserede proteinhydrogeler fremstilles ved hjælp af en lysaktiveret reaktion, i nærværelse af ammoniumpersulfat (APS) og tris(bipyridin) ruthenium(II)chlori -
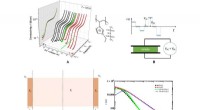 Kapacitans af tynde film indeholdende polymeriserede ioniske væskerDetaljer om bredbånds dielektrisk spektroskopi (BDS) målinger, kemisk struktur af PolyIL studeret i dette arbejde sammen med elektrodepolarisationsmodellen, der bruges til fortolkning af eksperimentel
Kapacitans af tynde film indeholdende polymeriserede ioniske væskerDetaljer om bredbånds dielektrisk spektroskopi (BDS) målinger, kemisk struktur af PolyIL studeret i dette arbejde sammen med elektrodepolarisationsmodellen, der bruges til fortolkning af eksperimentel
- Bionedbrydelig mikrorobot til behandling af kræft
- Robotic floats giver et nyt kig på havets sundhed og den globale kulstofcyklus
- Uprøvede teknologier er ikke en del af vejledningen om klimafiksering:Brancheorganisation
- Tror du, at chimpansesenge er mere beskidte end menneskelige? igen
- Melanins kemi
- Hovedproblemet med virtual reality? Det er næsten lige så dumt som det virkelige liv


