Hvor mange formelenheder er der i 22,4 g SnO2?
1. Beregn molmassen af SnO2:
Molær masse af Sn =118,710 g/mol
Molær masse af O =15,999 g/mol
Molær masse af SnO2 =(1 x 118,710 g/mol) + (2 x 15,999 g/mol) =150,698 g/mol
2. Omregn den givne masse (22,4 g) til mol:
Mol af SnO2 =masse / molær masse
Mol SnO2 =22,4 g / 150,698 g/mol
Mol SnO2 =0,1488 mol
3. Beregn antallet af formelenheder ved hjælp af Avogadros tal:
Avogadros tal =6,022 x 10^23 formelenheder/mol
Antal formelenheder =Mol SnO2 x Avogadros tal
Antal formelenheder =0,1488 mol x 6,022 x 10^23 formelenheder/mol
Antal formelenheder =8.956 x 10^22 formelenheder
Derfor er der 8,956 x 10^22 formelenheder i 22,4 g SnO2.
Sidste artikelHvilket stof kan nedbrydes kemisk CO Cu Ce Ca?
Næste artikelEr 50 ml vand og 20 ml salt koncentreret?
 Varme artikler
Varme artikler
-
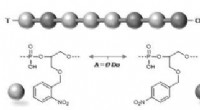 Hemmelige beskeder gemt i lysfølsomme polymererSkematisk fremstilling af et hemmeligt molekylært budskab afsløret af lys. Kredit:© Jean-François Lutz Forskere fra CNRS og Aix-Marseille Université har for nylig vist, hvor værdifulde lysfølsomme
Hemmelige beskeder gemt i lysfølsomme polymererSkematisk fremstilling af et hemmeligt molekylært budskab afsløret af lys. Kredit:© Jean-François Lutz Forskere fra CNRS og Aix-Marseille Université har for nylig vist, hvor værdifulde lysfølsomme -
 Udnyttelse af kropsvarmen til at drive elektroniske enhederUdviklingen af effektive termoelektriske materialer betyder, at kropsvarme alene fra, sige, en persons hånd, kan bruges til at drive små bærbare enheder, i dette tilfælde en rød LED. Kredit:A*STAR I
Udnyttelse af kropsvarmen til at drive elektroniske enhederUdviklingen af effektive termoelektriske materialer betyder, at kropsvarme alene fra, sige, en persons hånd, kan bruges til at drive små bærbare enheder, i dette tilfælde en rød LED. Kredit:A*STAR I -
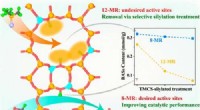 Ny strategi til at kontrollere fordelingen af syresteder i zeolitterGrafisk abstrakt. Kredit:ACS Catalysis (2022). DOI:10.1021/acscatal.1c05896 Zeolitter er en af de formselektive katalysatorer. Zeolitternes egenskaber, som kommer fra den strukturelle indeslutnin
Ny strategi til at kontrollere fordelingen af syresteder i zeolitterGrafisk abstrakt. Kredit:ACS Catalysis (2022). DOI:10.1021/acscatal.1c05896 Zeolitter er en af de formselektive katalysatorer. Zeolitternes egenskaber, som kommer fra den strukturelle indeslutnin -
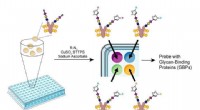 Ny TSRI-metode fremskynder undersøgelser af kulhydratbiologiEn ny metode til at samle et glycan-array. Kredit:Wu Lab / Scripps Research Institute 28. februar, 2018 - Næsten alle levende celler er besat med forgrenede kulhydratkæder kaldet glykaner. Glykane
Ny TSRI-metode fremskynder undersøgelser af kulhydratbiologiEn ny metode til at samle et glycan-array. Kredit:Wu Lab / Scripps Research Institute 28. februar, 2018 - Næsten alle levende celler er besat med forgrenede kulhydratkæder kaldet glykaner. Glykane
- Inspireret af stål, nanofremstilling får slidstærkt hårdmetalspids
- Online begravelsessæt hjælper sørgende indere
- Undersøgelse viser, hvorfor almindeligt eksplosivt PETN nogle gange svigter
- Nanopartikler med en kerne-skal struktur kan minimere overophedning af celler under bioimaging ekspe…
- Kinas efterspørgsel efter Jaguar Land Rover indeholder tab af Tata Motors
- Sådan ser du atmosfæren


