Hvad sker der, når man putter zink i saltsyre?
Zn + 2HCl → ZnCl2 + H2
Under reaktionen mister zinkatomerne elektroner til hydrogenionerne (H+) i saltsyren, hvilket resulterer i dannelsen af zinkioner (Zn2+) og brintgas. Den producerede brintgas frigives som bobler, hvilket forårsager opbrusning og brus.
Denne reaktion er et eksempel på en enkeltfortrængningsreaktion, hvor et grundstof (zink) erstatter et andet grundstof (brint) i en forbindelse (saltsyre). Reaktiviteten af zink med saltsyre er relativt høj, og reaktionen forløber med en moderat hastighed ved stuetemperatur.
Det er vigtigt at bemærke, at denne reaktion skal udføres med forsigtighed. Saltsyre er et ætsende stof og kan forårsage hudforbrændinger og øjenskader. Korrekte sikkerhedsforanstaltninger, såsom at bære handsker og øjenbeskyttelse, bør tages, når du arbejder med saltsyre.
Sidste artikelHvad sker der med zink, hvis det kommer i saltsyre?
Næste artikelHvordan kunne man adskille zinkchlorid fra siliciumoxid?
 Varme artikler
Varme artikler
-
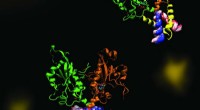 En molekylær dans af fosfolipidsynteseCCT er et nøgleenzym, der opretholder en afbalanceret sammensætning af cellemembranfosfolipider. Billedet fremhæver dynamikken i en del af enzymet CCT, der er afgørende for regulering af dets funktion
En molekylær dans af fosfolipidsynteseCCT er et nøgleenzym, der opretholder en afbalanceret sammensætning af cellemembranfosfolipider. Billedet fremhæver dynamikken i en del af enzymet CCT, der er afgørende for regulering af dets funktion -
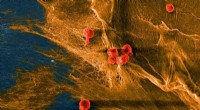 Blødt, men sejt:Biohybridmateriale fungerer som bruskMikrografi af et biohybrid kompositmateriale udviklet hos Cornell viser celler (røde) udsået på de fibrøse domæner (gule) af kollagen. Materialet efterligner naturligt væv i dets blødhed, sejhed og ev
Blødt, men sejt:Biohybridmateriale fungerer som bruskMikrografi af et biohybrid kompositmateriale udviklet hos Cornell viser celler (røde) udsået på de fibrøse domæner (gule) af kollagen. Materialet efterligner naturligt væv i dets blødhed, sejhed og ev -
 Forskere skabte spiselige film til fødevareemballageRammohan Aluru (til venstre) og Grigory Zyryanov (til højre) i forskningsgruppen skabte spiselige madfilm på tangen. Kredit:UrFU / Andrei Fomin En international gruppe af forskere fra Indien og Ru
Forskere skabte spiselige film til fødevareemballageRammohan Aluru (til venstre) og Grigory Zyryanov (til højre) i forskningsgruppen skabte spiselige madfilm på tangen. Kredit:UrFU / Andrei Fomin En international gruppe af forskere fra Indien og Ru -
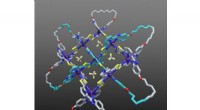 Forskere opdager en ny type molekylær knude ved hjælp af røntgendiffraktionsteknikkerDavid Leigh, University of Manchester. Forskere har udviklet en måde at flette tre molekylære tråde, så det er muligt at lave strammere og mere komplekse knuder, end det tidligere har været muligt
Forskere opdager en ny type molekylær knude ved hjælp af røntgendiffraktionsteknikkerDavid Leigh, University of Manchester. Forskere har udviklet en måde at flette tre molekylære tråde, så det er muligt at lave strammere og mere komplekse knuder, end det tidligere har været muligt
- Chloroplast & Mitochondria: Hvad er lighederne og forskellene?
- Træer og planter kan blive nye tilsætningsstoffer i lette fødevarer
- Initiativer til beskyttelse af amerikansk energinet og atomvåben systemer
- Hvordan så vores forfædre ud?
- Fotoelektrokemisk vandopdelingseffektivitet rammer 4,5%
- Struktur motiv-centreret læringsramme for uorganiske krystallinske systemer


