Hvorfor er vands overfladespænding højere end metan?
Hydrogenbinding er en dipol-dipol-interaktion, der forekommer mellem stærkt elektronegative atomer (såsom oxygen eller nitrogen) og hydrogenatomer bundet til disse elektronegative atomer. I vand er iltatomerne i molekylet delvist negative på grund af deres høje elektronegativitet, mens brintatomerne er delvist positive. Denne polaritet gør det muligt for vandmolekyler at danne stærke brintbindinger med nabomolekyler, hvilket skaber et sammenhængende netværk.
Vandmolekyler på overfladen oplever en ubalance af intermolekylære kræfter. På den ene side er de bundet til andre vandmolekyler i væsken, mens den anden side er udsat for luft eller en anden ublandbar væske. De stærke brintbindinger mellem vandmolekyler ved overfladen trækker dem tættere sammen, hvilket minimerer overfladearealet og reducerer vands interaktion med det omgivende miljø. Denne sammenhængende adfærd resulterer i en højere overfladespænding for vand.
I modsætning hertil er metan et ikke-polært molekyle, hvilket betyder, at dets elektroner er jævnt fordelt, og der er ingen signifikant elektronegativitetsforskel i molekylet. Som et resultat mangler metanmolekyler evnen til at danne stærke hydrogenbindinger med hinanden. De intermolekylære kræfter i metan er primært London-spredningskræfter, som er svage tiltrækningskræfter, der opstår som følge af de midlertidige fluktuationer i elektrontætheden.
由于甲烷分子之间的范德华力较弱,甲烷的表面张力小于水。
Derfor fører fraværet af stærke intermolekylære kræfter i metan til en svagere sammenhængende adfærd på dens overflade. Metanmolekyler oplever svagere van der Waals-kræfter, som er utilstrækkelige til at holde overfladen sammen så tæt som i tilfældet med vand. Dette resulterer i en lavere overfladespænding for metan sammenlignet med vand.
Sammenfattende er vands høje overfladespænding en konsekvens af den stærke brintbinding mellem dets molekyler, hvilket skaber et sammenhængende netværk og minimerer vands interaktion med det omgivende miljø. På den anden side mangler metan disse stærke intermolekylære kræfter, hvilket fører til en lavere overfladespænding på grund af svagere van der Waals-kræfter.
Sidste artikelHvad menes der med en blandet smeltepunktsbestemmelse?
Næste artikelNår vandet opvarmes, vil partiklerne?
 Varme artikler
Varme artikler
-
 Molekyle angriber coronavirus på en ny mådeI forgrunden, aptamerens sekundære struktur. I baggrunden ses den automatiserede SELEX -platform ved LIMES Institute ved University of Bonn. Kredit:Stefan Breuers/LIMES Forskere ved universitetet
Molekyle angriber coronavirus på en ny mådeI forgrunden, aptamerens sekundære struktur. I baggrunden ses den automatiserede SELEX -platform ved LIMES Institute ved University of Bonn. Kredit:Stefan Breuers/LIMES Forskere ved universitetet -
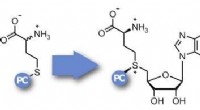 Enzymatisk photocaging til undersøgelse af genregulering gennem DNA-methyleringKredit:Wiley Tilføjelse og fjernelse af methylgrupper på DNA spiller en vigtig rolle i genregulering. For at studere disse mekanismer mere præcist, et tysk team har udviklet en ny metode, hvorved
Enzymatisk photocaging til undersøgelse af genregulering gennem DNA-methyleringKredit:Wiley Tilføjelse og fjernelse af methylgrupper på DNA spiller en vigtig rolle i genregulering. For at studere disse mekanismer mere præcist, et tysk team har udviklet en ny metode, hvorved -
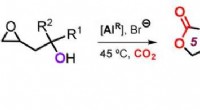 Kaskader med kuldioxidKredit: Angewandte Chemie Kuldioxid (CO 2 ) er ikke bare en uønsket drivhusgas, det er også en interessant kilde til råvarer, der er værdifulde og kan genbruges bæredygtigt. I journalen Angewa
Kaskader med kuldioxidKredit: Angewandte Chemie Kuldioxid (CO 2 ) er ikke bare en uønsket drivhusgas, det er også en interessant kilde til råvarer, der er værdifulde og kan genbruges bæredygtigt. I journalen Angewa -
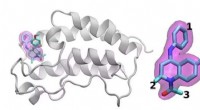 Forskningsgruppen bruger supercomputing til at målrette de mest lovende lægemiddelkandidater ud fr…En skematisk oversigt over BRD4 -proteinet bundet til et af 16 lægemidler baseret på det samme tetrahydroquinolin -stillads (fremhævet i magenta). Regioner, der er kemisk modificeret mellem de lægemid
Forskningsgruppen bruger supercomputing til at målrette de mest lovende lægemiddelkandidater ud fr…En skematisk oversigt over BRD4 -proteinet bundet til et af 16 lægemidler baseret på det samme tetrahydroquinolin -stillads (fremhævet i magenta). Regioner, der er kemisk modificeret mellem de lægemid
- Elfenbenskysten producerer rekordhøj kakaoafgrøde
- Astronomer udfører første søgning efter at danne planeter med James Webb Space Telescope
- Sådan virker benzin
- Vil Saturns ringe virkelig 'forsvinde' inden 2025? En astronom forklarer
- Undersøgelse identificerer en måde at specifikt målrette mod og blokere sygdomsassocierede hvide …
- Miljøvenlige InSb/InP kolloide kvanteprikker til hurtige og følsomme kortbølgede infrarøde fotod…


