Hvor mange atomer er der i 1 gram guld?
```
Antal atomer =(masse af guld i gram) * (Avogadros tal) / (molær masse af guld)
```
hvor:
* Avogadros tal er antallet af atomer i et mol af et stof, hvilket er cirka 6,022 x 10^23 atomer/mol.
* Den molære masse af guld er massen af en mol guld, hvilket er cirka 196,97 gram/mol.
Derfor er antallet af atomer i 1 gram guld:
```
Antal atomer =(1 gram) * (6,022 x 10^23 atomer/mol) / (196,97 gram/mol) ≈ 3,06 x 10^21 atomer
```
Så der er cirka 3,06 x 10^21 atomer i 1 gram guld.
 Varme artikler
Varme artikler
-
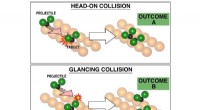 Kemikere fremmer evnen til at kontrollere kemiske reaktionerValget af påvirkningsparameteren er grundlæggende for resultatet af kemisk reaktion, som visualiseret her baseret på eksperimenter. Ved nul indvirkningsparameter, reaktionen øverst viste reproducerbar
Kemikere fremmer evnen til at kontrollere kemiske reaktionerValget af påvirkningsparameteren er grundlæggende for resultatet af kemisk reaktion, som visualiseret her baseret på eksperimenter. Ved nul indvirkningsparameter, reaktionen øverst viste reproducerbar -
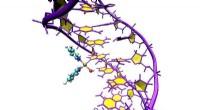 Hvordan interagerer metaller med DNA?Computersimuleringer viser den præcise placering af Pt103 i DNA. Kredit:Juan J. Nogueira, Universitetet i Wien I et par årtier, metalholdige lægemidler er med succes blevet brugt til at bekæmpe vi
Hvordan interagerer metaller med DNA?Computersimuleringer viser den præcise placering af Pt103 i DNA. Kredit:Juan J. Nogueira, Universitetet i Wien I et par årtier, metalholdige lægemidler er med succes blevet brugt til at bekæmpe vi -
 Genbrug af drivhusgasser:Nanopartikler på perovskitkrystaller undgår kokseffektFlorian Schrenk (til venstre) og Christoph Rameshan. Kredit:Vienna University of Technology Hvor som helst produktionen af skadelige drivhusgasser ikke kan forhindres, bør de omdannes til noget n
Genbrug af drivhusgasser:Nanopartikler på perovskitkrystaller undgår kokseffektFlorian Schrenk (til venstre) og Christoph Rameshan. Kredit:Vienna University of Technology Hvor som helst produktionen af skadelige drivhusgasser ikke kan forhindres, bør de omdannes til noget n -
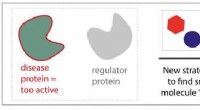 Sådan finder du molekylære lim til effektivt at målrette sygdommeNye strategier til små molekylære lim. Kredit:Eindhoven University of Technology Mange af de i øjeblikket tilgængelige lægemidler er ikke specifikke nok til effektivt at helbrede komplekse sygdomm
Sådan finder du molekylære lim til effektivt at målrette sygdommeNye strategier til små molekylære lim. Kredit:Eindhoven University of Technology Mange af de i øjeblikket tilgængelige lægemidler er ikke specifikke nok til effektivt at helbrede komplekse sygdomm
- Hvordan spredning af datacentre påvirker vandforsyningen i USA
- Forskellen mellem lige linjevind og tornadoer
- Hvem opfandt køleskabet?
- Tørke på tryk for at intensivere over det amerikanske sydvest
- Fiberoptisk transmission på 4000 km muliggjort af ultra-støjsvage optiske forstærkere
- Forskere kommer med teknologi til at genbruge brugt tøj i stedet for blot at brænde det


