Er det rigtigt, at elektronerne i et vandmolekyle tiltrækkes mere mod brintatomer?
Et atoms elektronegativitet refererer til dets evne til at tiltrække elektroner mod sig selv i en kemisk binding. Ilt er mere elektronegativt end brint, hvilket betyder, at det har et stærkere træk på elektronerne i de kovalente bindinger. Dette resulterer i en let polarisering af elektronskyen, hvor elektronerne er lidt tættere på oxygenatomet.
Det er dog vigtigt at bemærke, at elektrondensiteten i et molekyle ikke er statisk. Elektronerne bevæger sig konstant og deler sig mellem atomerne, og den nøjagtige fordeling af elektroner kan ændre sig over tid. Derfor er det ikke korrekt at sige, at elektronerne tiltrækkes mere mod brintatomerne i et vandmolekyle.
Sidste artikelHvor mange mol atomer er der i 1,00 lb bly?
Næste artikelHvad er pH-niveauet for aluminiumhydroxid?
 Varme artikler
Varme artikler
-
 En enklere model kommer til sagen med proteinerCecilia Clementi. Kredit:Jeff Fitlow/Rice University Beregningsmodeller er kommet langt i deres evne til at simulere de mest basale biologiske processer, såsom hvordan proteiner folder. En ny tekn
En enklere model kommer til sagen med proteinerCecilia Clementi. Kredit:Jeff Fitlow/Rice University Beregningsmodeller er kommet langt i deres evne til at simulere de mest basale biologiske processer, såsom hvordan proteiner folder. En ny tekn -
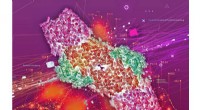 Energi efter behov:Lær af naturens katalysatorerKvantekemi, kvanteberegning, og Pacific Northwest National Laboratorys Energy Sciences Center kunne hjælpe forskere med at besvare det næste store spørgsmål inden for katalyse. (Billede af Timothy Hol
Energi efter behov:Lær af naturens katalysatorerKvantekemi, kvanteberegning, og Pacific Northwest National Laboratorys Energy Sciences Center kunne hjælpe forskere med at besvare det næste store spørgsmål inden for katalyse. (Billede af Timothy Hol -
 Røntgenlaserforskere udvikler en ny måde at se bakterier angribe antibiotikaEksperimentet blev udført på Coherent X-ray Imaging (CXI) instrument, der gør brug af den hurtige, strålende røntgenpulser fra Linac kohærente lyskilde. CXI anvender metoden diffraktion-før-ødelæggels
Røntgenlaserforskere udvikler en ny måde at se bakterier angribe antibiotikaEksperimentet blev udført på Coherent X-ray Imaging (CXI) instrument, der gør brug af den hurtige, strålende røntgenpulser fra Linac kohærente lyskilde. CXI anvender metoden diffraktion-før-ødelæggels -
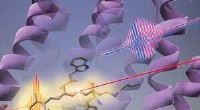 Proteinændringer går forud for fotoisomerisering af retinal kromoforFigur 1:RIKEN-forskere har fundet ud af, at lys (lang rød linje) først får proteinets form (lilla hvirvler) til at ændre sig, før den retinale kromofor (stick-lignende struktur) i bacteriorhodopsin ge
Proteinændringer går forud for fotoisomerisering af retinal kromoforFigur 1:RIKEN-forskere har fundet ud af, at lys (lang rød linje) først får proteinets form (lilla hvirvler) til at ændre sig, før den retinale kromofor (stick-lignende struktur) i bacteriorhodopsin ge
- Hvordan vores album med fuglesang-optagelser steg til #2 på ARIA-hitlisterne
- Det europæiske bilsalg accelererer til et årti-høj hastighed i oktober
- Indonesiens vulkan bøvser en enorm askesøjle
- Perseid Meteor -brusebadet er tilbage - Her er hvad du behøver at vide
- Gravitationsbølger kunne kaste lys over mørkt stof
- Hvad er eksemplerne på faststof-væske blandinger?


