Hvorfor er ioniske forbindelser hårde krystallinske faste stoffer?
Ioniske forbindelser har typisk høje gitterenergier, fordi de indeholder ioner med høje ladninger, såsom natrium- og chloridioner. De stærke elektrostatiske kræfter mellem disse ioner holder krystalgitteret tæt sammen, hvilket gør det svært at bryde fra hinanden. Det er derfor ioniske forbindelser er hårde faste stoffer.
Ud over at være hårde, er ioniske forbindelser også skøre. Det betyder, at de har en tendens til at gå i stykker, når de udsættes for stress. Det skyldes, at de elektrostatiske kræfter mellem ionerne er stærke, men de er ikke retningsbestemte. Det betyder, at de ikke yder nogen støtte mod forskydningskræfter. Når en ionforbindelse udsættes for stress, kan ionerne bevæge sig forbi hinanden, hvilket får krystallen til at bryde.
Hårdheden og skørheden af ioniske forbindelser gør dem nyttige til en række forskellige anvendelser, såsom i keramik og glas. Keramik fremstilles ved at opvarme en ionforbindelse, indtil den smelter, og derefter lade den afkøle langsomt. Dette gør det muligt for ionerne at omarrangere sig selv til en regulær krystalstruktur. Det resulterende materiale er hårdt og skørt, men det er også modstandsdygtigt over for varme og slid. Glas fremstilles ved at opvarme en ionforbindelse, indtil den smelter, og derefter hurtigt afkøle den. Dette forhindrer ionerne i at omarrangere sig selv til en regulær krystalstruktur. Det resulterende materiale er hårdt og skørt, men det er også gennemsigtigt.
 Varme artikler
Varme artikler
-
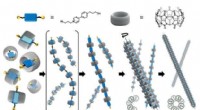 Selvsamlet kunstig mikrotubuli som LEGO byggeklodserHierarkisk selvsamling af polypseudorotaxaner til kunstige mikrotubuli. Kredit:Kimoon Kim (POSTECH) Simple LEGO klodser kan samles til mere komplicerede strukturer, som yderligere kan associeres t
Selvsamlet kunstig mikrotubuli som LEGO byggeklodserHierarkisk selvsamling af polypseudorotaxaner til kunstige mikrotubuli. Kredit:Kimoon Kim (POSTECH) Simple LEGO klodser kan samles til mere komplicerede strukturer, som yderligere kan associeres t -
 Undersøgelse kaster nyt lys over produktionen af hydroxylradikaler, som hjælper med at nedbryde …Et forskerhold, der omfattede Argonne-kemikeren Stephen Klippenstein, undersøgte produktionen af hydroxylradikaler, som hjælper med at nedbryde luftforurenende stoffer, i et nyt lys. Kredit:LALS STO
Undersøgelse kaster nyt lys over produktionen af hydroxylradikaler, som hjælper med at nedbryde …Et forskerhold, der omfattede Argonne-kemikeren Stephen Klippenstein, undersøgte produktionen af hydroxylradikaler, som hjælper med at nedbryde luftforurenende stoffer, i et nyt lys. Kredit:LALS STO -
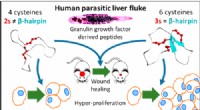 Et molekyle produceret af en thailandsk leverparasit kan være løsningen på de ikke-helende sårKredit:ACS Hver dag amputeres 12 australske diabetikere på grund af et sår, der ikke heler. Globalt set det er en hvert 30. sekund. Et molekyle produceret af en thailandsk leverparasit kan være l
Et molekyle produceret af en thailandsk leverparasit kan være løsningen på de ikke-helende sårKredit:ACS Hver dag amputeres 12 australske diabetikere på grund af et sår, der ikke heler. Globalt set det er en hvert 30. sekund. Et molekyle produceret af en thailandsk leverparasit kan være l -
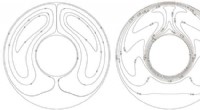 Parallel koblet cellecentreret endeligt volumen termisk gitter boltzmann metode på ustrukturerede g…Simuleringsresultater af naturlig konvektion i en koncentrisk ring ved Ra=5×10 4 , strømlines (venstre), temperaturkonturer (højre). Kredit:SIAT Gitter Boltzmann-metoden (LBM), som stammer fra g
Parallel koblet cellecentreret endeligt volumen termisk gitter boltzmann metode på ustrukturerede g…Simuleringsresultater af naturlig konvektion i en koncentrisk ring ved Ra=5×10 4 , strømlines (venstre), temperaturkonturer (højre). Kredit:SIAT Gitter Boltzmann-metoden (LBM), som stammer fra g
- Mantelstenen bag Yellowstones superudbrud strækker sig til det nordlige Californien
- Hvad er tyngdekraften på jorden under en solformørkelse?
- Et miljøvenligt batteri lavet af træ (Opdatering)
- Sådan konverteres RPM til MPH med en lommeregner
- Mikroskala termoforese til at karakterisere hits fra high-throughput screening
- Forældreinddragelse spiller en central rolle for børns akademiske præstationer, forskning viser


