Hvordan skriver man forbrændingsligningen for benzen trin for trin?
Trin 1:Identificer reaktanterne og produkterne.
I dette tilfælde er reaktanterne benzen (C6H6) og oxygen (O2), og produkterne er kuldioxid (CO2) og vand (H2O).
Trin 2:Skriv den ubalancerede kemiske ligning.
Ved at bruge reaktanterne og produkterne identificeret i trin 1 kan vi skrive den ubalancerede kemiske ligning som:
C6H6 + O2 → CO2 + H2O
Trin 3:Balancer kulstofatomerne.
Vi starter med at balancere kulstofatomerne. Der er 6 carbonatomer på venstre side af ligningen (i C6H6), så vi skal sikre os, at der også er 6 carbonatomer på højre side. Ved at placere en koefficient på 6 foran CO2 opnår vi dette:
C6H6 + O2 → 6CO2 + H2O
Trin 4:Balancer brintatomerne.
Dernæst afbalancerer vi brintatomerne. Der er 6 brintatomer på venstre side af ligningen (i C6H6), så vi skal også have 6 brintatomer på højre side. Ved at placere en koefficient på 3 foran H2O opnår vi dette:
C6H6 + O2 → 6CO2 + 3H2O
Trin 5:Balancer iltatomerne.
Til sidst balancerer vi iltatomerne. Der er 2 oxygenatomer på venstre side af ligningen (i O2), og der er i alt 12 oxygenatomer på højre side (i 6CO2 og 3H2O). For at balancere dette skal vi placere en koefficient på 15/2 foran O2:
C6H6+ (15/2)O2 → 6CO2 + 3H2O
Trin 6:Tjek for overordnet balance.
På dette tidspunkt er ligningen afbalanceret med hensyn til alle atomer. For at sikre overordnet balance kan vi verificere, at den samlede ladning på begge sider af ligningen er ens. I dette tilfælde har begge sider en total ladning på 0, så ligningen er afbalanceret.
Derfor er den afbalancerede forbrændingsligning for benzen:
C6H6 + (15/2)O2 → 6CO2 + 3H2O
 Varme artikler
Varme artikler
-
 Team opdager kontrol af cellesignalering ved hjælp af et kobolt (III) -nitrosylkompleksProfessor Jaeheung Cho (forrest til venstre) - Professor Daeha Seo (foran til højre), og forskerteam i Institut for Emerging Materials Science. Kredit:DGIST To professorers fælles forskerhold har
Team opdager kontrol af cellesignalering ved hjælp af et kobolt (III) -nitrosylkompleksProfessor Jaeheung Cho (forrest til venstre) - Professor Daeha Seo (foran til højre), og forskerteam i Institut for Emerging Materials Science. Kredit:DGIST To professorers fælles forskerhold har -
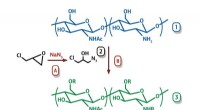 Kemikere får nyt materiale til antibakterielle madbelægningerRUDN University kemikere har udviklet en enkel og bekvem metode til fremstilling af derivater af den naturlige polymer chitosan. Disse derivater er ugiftige og har en udtalt antibakteriel aktivitet på
Kemikere får nyt materiale til antibakterielle madbelægningerRUDN University kemikere har udviklet en enkel og bekvem metode til fremstilling af derivater af den naturlige polymer chitosan. Disse derivater er ugiftige og har en udtalt antibakteriel aktivitet på -
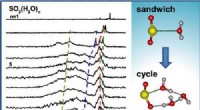 Forskere afslører trinvise hydreringsmotiver af svovldioxidGrafisk abstrakt. Kredit:The Journal of Physical Chemistry Letters (2022). DOI:10.1021/acs.jpclett.2c01472 Et forskerhold ledet af prof. Jiang Ling og Zhang Zhaojun fra Dalian Institute of Chemical
Forskere afslører trinvise hydreringsmotiver af svovldioxidGrafisk abstrakt. Kredit:The Journal of Physical Chemistry Letters (2022). DOI:10.1021/acs.jpclett.2c01472 Et forskerhold ledet af prof. Jiang Ling og Zhang Zhaojun fra Dalian Institute of Chemical -
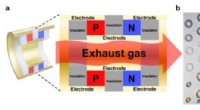 En termoelektrisk blæk, der gør bilens udstødningsrør til kraftgeneratorer3D-print af kraftproducerende TE-rør. a) Skema, der viser det kraftgenererende TE-rør fremstillet af 3D-printede p-type og n-type PbTe-rør forfra. b) Foto, der viser komponenterne til modulets samling
En termoelektrisk blæk, der gør bilens udstødningsrør til kraftgeneratorer3D-print af kraftproducerende TE-rør. a) Skema, der viser det kraftgenererende TE-rør fremstillet af 3D-printede p-type og n-type PbTe-rør forfra. b) Foto, der viser komponenterne til modulets samling


