Hvor mange ioner eller atomer af calcium og chlorid i 1,5 mol CaCl2?
1. Calcium (Ca) ioner :
- Hver formelenhed af CaCl2 indeholder en calciumion (Ca).
- I 1,5 mol CaCl2 er der 1,5 mol Ca-ioner.
- Avogadros tal fortæller os, at 1 mol af ethvert stof indeholder 6,022 × 10^23 partikler (atomer, ioner eller molekyler).
- Derfor indeholder 1,5 mol CaCl2 1,5 mol × 6,022 × 10^23 partikler/mol =9,033 × 10^23 Ca-ioner.
2. Chlorid (Cl) ioner :
- Hver formelenhed af CaCl2 indeholder to chloridioner (Cl).
- I 1,5 mol CaCl2 er der 1,5 mol Cl-ioner (da hvert CaCl2-molekyle bidrager med to Cl-ioner).
- Derfor indeholder 1,5 mol CaCl2 1,5 mol × 6,022 × 10^23 partikler/mol =9,033 × 10^23 Cl-ioner.
Så i 1,5 mol CaCl2 er der 9,033 × 10^23 calciumioner (Ca^2+) og 9,033 × 10^23 chloridioner (Cl^-).
 Varme artikler
Varme artikler
-
 En klar halvleder baseret på tin kunne forbedre solenergiproduktionenRåmaterialet, der bruges til at fremstille tindioxid-halvledere. Kredit:© 2020 Nakao et al. Mobilitet er en nøgleparameter for halvlederydelse og relaterer sig til, hvor hurtigt og nemt elektroner
En klar halvleder baseret på tin kunne forbedre solenergiproduktionenRåmaterialet, der bruges til at fremstille tindioxid-halvledere. Kredit:© 2020 Nakao et al. Mobilitet er en nøgleparameter for halvlederydelse og relaterer sig til, hvor hurtigt og nemt elektroner -
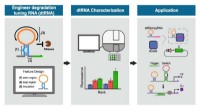 Lille teknik kan bringe store fremskridt inden for lægehjælpOvenstående grafik viser skemaer for en proces, der er central for forskning ledet af Xiao Wang og Alexander Green for at finde nye måder at genoprette menneskers sundhed ved at ombygge kroppens biome
Lille teknik kan bringe store fremskridt inden for lægehjælpOvenstående grafik viser skemaer for en proces, der er central for forskning ledet af Xiao Wang og Alexander Green for at finde nye måder at genoprette menneskers sundhed ved at ombygge kroppens biome -
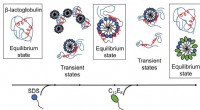 Fanget i sæbehånd:At forstå, hvordan sæbemolekyler hjælper proteiner med at komme ind og ud af …Resultater offentliggjort af AU-forskere afslører, at surfaktant-medieret udfoldning og genfoldning af proteiner er komplekse processer med flere strukturer til stede, og omarrangeringer sker på tidss
Fanget i sæbehånd:At forstå, hvordan sæbemolekyler hjælper proteiner med at komme ind og ud af …Resultater offentliggjort af AU-forskere afslører, at surfaktant-medieret udfoldning og genfoldning af proteiner er komplekse processer med flere strukturer til stede, og omarrangeringer sker på tidss -
 Fødevarekvalitetskontrol blev gjort hurtigere og lettereBaseret på ultrahøjtydende væskekromatografi-massespektrometri (UHPLC-MS) har videnskabsfolk ved det tekniske universitet i München (TUM) og Leibniz-instituttet for fødevarebiologi udviklet en ny meto
Fødevarekvalitetskontrol blev gjort hurtigere og lettereBaseret på ultrahøjtydende væskekromatografi-massespektrometri (UHPLC-MS) har videnskabsfolk ved det tekniske universitet i München (TUM) og Leibniz-instituttet for fødevarebiologi udviklet en ny meto
- Apple og Johnson &Johnson går sammen om undersøgelse for at reducere risikoen for slagtilfælde:Så…
- Opdag, hvordan du fokuserer på den mindste af de helt små
- Økonomien i at prioritere familiebånd i amerikansk immigrationspolitik
- Quantum dot ring lasere udsender farvet lys
- Fryser varmt vand hurtigere end koldt vand? Undersøgelse af Mpemba-effekten
- Cypern opfordrer til at udforske offshore-gas


