Er bagepulver en stærk base?
Natriumbicarbonat er klassificeret som en svag base. Stærke baser dissocieres fuldstændigt i vand, hvilket producerer en høj koncentration af hydroxidioner (OH-) og øger pH betydeligt.
På den anden side undergår svage baser som natriumbicarbonat delvis dissociation i vand, hvilket frigiver en lavere koncentration af hydroxidioner, hvilket resulterer i en mindre dramatisk stigning i pH.
Til sammenligning inkluderer nogle eksempler på stærke baser natriumhydroxid (NaOH) og kaliumhydroxid (KOH), som dissocierer helt i vand og skaber høje pH-niveauer.
Sidste artikelHvorfor kan en blanding ikke have en unik kemisk formel?
Næste artikelHvor kommer kulstoffet i dioxiden du udånder fra?
 Varme artikler
Varme artikler
-
 Hvordan en vietnamesisk rå svinekødssnack kunne hjælpe os med at holde maden frisk, naturligtVietnamesisk fermenteret svinekødssnack, Nem Chua. Kredit:RMIT University En traditionel vietnamesisk kødsnack kunne indeholde nøglen til at udvikle et sikkert og naturligt fødevarekonserveringsmi
Hvordan en vietnamesisk rå svinekødssnack kunne hjælpe os med at holde maden frisk, naturligtVietnamesisk fermenteret svinekødssnack, Nem Chua. Kredit:RMIT University En traditionel vietnamesisk kødsnack kunne indeholde nøglen til at udvikle et sikkert og naturligt fødevarekonserveringsmi -
 Konstruktion af et plast-spisende enzymKredit:University of Portsmouth Forskere har udviklet et enzym, der kan fordøje nogle af vores mest forurenende plastmaterialer, at levere en potentiel løsning på et af verdens største miljøproble
Konstruktion af et plast-spisende enzymKredit:University of Portsmouth Forskere har udviklet et enzym, der kan fordøje nogle af vores mest forurenende plastmaterialer, at levere en potentiel løsning på et af verdens største miljøproble -
 Skab en bedre paryk med kemiHår belagt med en nanokomposit (til venstre) ved hjælp af Langmuir-Blodgett-teknikken genererer meget mindre statisk elektricitet end ubehandlede hår (højre). Kredit:Tilpasset fra ACS Applied Material
Skab en bedre paryk med kemiHår belagt med en nanokomposit (til venstre) ved hjælp af Langmuir-Blodgett-teknikken genererer meget mindre statisk elektricitet end ubehandlede hår (højre). Kredit:Tilpasset fra ACS Applied Material -
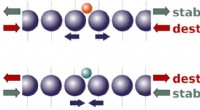 Ny teori viser, hvordan belastning giver bedre katalysatorerBrown University forskere har vist, at virkningerne af ekstern belastning på en katalysator afhænger af den indre belastning, der udøves af kemiske reaktanter. Den nye teoretiske ramme kunne være nytt
Ny teori viser, hvordan belastning giver bedre katalysatorerBrown University forskere har vist, at virkningerne af ekstern belastning på en katalysator afhænger af den indre belastning, der udøves af kemiske reaktanter. Den nye teoretiske ramme kunne være nytt
- Samarbejdsundersøgelser viser, at finere rå bomuld er bedst til afhjælpning af olieudslip
- Hvad er funktionerne for mRNA & tRNA?
- Sådan konverteres vindhastighed til Pressure
- Microsoft opfordrer til regulering af ansigtsgenkendende teknologi
- Petrichor:Hvad forårsager den jordagtige lugt efter regn?
- Bariumruthenat:Et højt udbytte, lethåndterlig perovskitkatalysator til oxidation af sulfider


