Hvordan er bor reaktivt i kemiske egenskaber?
1. Lav elektronegativitet :Bor har en relativt lav elektronegativitet (2,04) sammenlignet med mange andre grundstoffer. Det betyder, at den har en svag tiltrækning af elektroner, hvilket gør den tilbøjelig til at danne kovalente bindinger.
2. Elektronmangel :Bor eksisterer almindeligvis i en tre-valent tilstand, hvilket betyder, at det har tre valenselektroner. Denne elektronmangel driver dens reaktivitet, da den søger at fuldende sin oktet ved at acceptere eller dele elektroner.
3. Lewis Acid Adfærd :Bor fungerer som en Lewis-syre på grund af dets tomme p-orbital. Det accepterer let elektronpar fra Lewis-baser for at danne koordinerede kovalente bindinger. Denne adfærd gør den til en god elektronpar-acceptor.
4. Danning af kovalente bindinger :Bor danner let kovalente bindinger med elementer som brint, kulstof, oxygen, nitrogen og halogener. Disse kovalente bindinger skyldes deling af elektronpar mellem bor og de andre atomer.
5. Høj ioniseringsenergi :Bor har en relativt høj første ioniseringsenergi (8,3 eV) sammenlignet med andre gruppe 13 grundstoffer. Det betyder, at det kræver en betydelig mængde energi at fjerne dens yderste elektron, hvilket gør det mindre sandsynligt, at det danner ionbindinger.
6. Hydriddannelse :Bor danner stabile hydrider kendt som boraner, såsom diboran (B2H6) og boran (BH3). Boraner er karakteriseret ved tre-center to-elektronbindinger, hvor to elektroner er delt mellem tre atomer.
7. Reaktivitet med ilt :Bor reagerer let med oxygen og danner forskellige forbindelser. For eksempel danner det boroxid (B2O3), når det opvarmes i luft, hvilket er en almindelig komponent i borosilikatglas og keramiske glasurer.
8. Kompleks dannelse :Bor danner komplekse forbindelser med forskellige ligander på grund af dets evne til at acceptere elektronpar. Denne egenskab udnyttes i adskillige applikationer, såsom i borbaserede lægemidler og katalysatorer.
Overordnet set stammer bors kemiske reaktivitet fra dets elektronmangel, lave elektronegativitet og tendens til at danne kovalente bindinger og komplekser. Disse egenskaber gør det til et alsidigt element med en bred vifte af anvendelser i forskellige industrier.
Sidste artikelHvordan får du metan i kroppen?
Næste artikelHvad er metalloider i naturen sure eller basiske?
 Varme artikler
Varme artikler
-
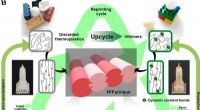 Upcycling af plast gennem dynamisk tværbindingCirkulær modeldesign af upcycling af termoplast til genanvendelig vitrimer til FFF. (A) Skematisk diagram, der sammenligner karakteristika for traditionelle termoplast, termohærdende og vitrimere. (B)
Upcycling af plast gennem dynamisk tværbindingCirkulær modeldesign af upcycling af termoplast til genanvendelig vitrimer til FFF. (A) Skematisk diagram, der sammenligner karakteristika for traditionelle termoplast, termohærdende og vitrimere. (B) -
 En rhodiumbaseret katalysator til fremstilling af organosilicium ved hjælp af mindre ædle metallerEt billede af hydrosilyleringsreaktionen ved anvendelse af den SiO2-understøttede katalysator bestående af et immobiliseret Rh-kompleks og tertiære aminer, med en omsætning på 260 (venstre) og nærmer
En rhodiumbaseret katalysator til fremstilling af organosilicium ved hjælp af mindre ædle metallerEt billede af hydrosilyleringsreaktionen ved anvendelse af den SiO2-understøttede katalysator bestående af et immobiliseret Rh-kompleks og tertiære aminer, med en omsætning på 260 (venstre) og nærmer -
 Laser spor terapi, næringsstoffer, toksinerI biologiske systemer, kulstof-14 kan bruges som et biokemisk sporstof til at spore mikrodoser af næringsstoffer, toksiner og terapeutika hos mennesker og dyr. Kredit:Lawrence Livermore National Labor
Laser spor terapi, næringsstoffer, toksinerI biologiske systemer, kulstof-14 kan bruges som et biokemisk sporstof til at spore mikrodoser af næringsstoffer, toksiner og terapeutika hos mennesker og dyr. Kredit:Lawrence Livermore National Labor -
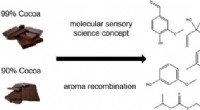 Duften af mørk chokolade, afmystificeretKredit:American Chemical Society Chokolade er en af de mest forbrugte godbidder rundt om i verden, og lugten alene er normalt nok til at fremkalde stærke trang fra selv de mest disciplinerede sp
Duften af mørk chokolade, afmystificeretKredit:American Chemical Society Chokolade er en af de mest forbrugte godbidder rundt om i verden, og lugten alene er normalt nok til at fremkalde stærke trang fra selv de mest disciplinerede sp
- Sådan måles sheave Diameter
- Er chokolade virkelig godt for mig?
- Liste over værdifulde naturressourcer i de vestlige Forenede Stater
- Gamle amerikanere lavede kunst dybt inde i hulernes mørke zoner i hele sydøsten
- Modellering af hver bygning i Amerika starter med Chattanooga
- En ny metode til at udløse regn, hvor der er knaphed på vand


