Når temperaturen af en gas med fast volumen stiger, vil trykket?
 Varme artikler
Varme artikler
-
 Ny udvikling inden for kontaktlinser til rød-grøn farveblindhed ved hjælp af simpelt farvestofKredit:University of Birmingham Forskere ved University of Birmingham har udviklet en kontaktlinse, der kan hjælpe mennesker med farveblindhed blot ved at bruge et billigt farvestof, ifølge forskn
Ny udvikling inden for kontaktlinser til rød-grøn farveblindhed ved hjælp af simpelt farvestofKredit:University of Birmingham Forskere ved University of Birmingham har udviklet en kontaktlinse, der kan hjælpe mennesker med farveblindhed blot ved at bruge et billigt farvestof, ifølge forskn -
 Byggesæt til specialdesignede produkterFra venstre mod højre:Dr. Yan-Ni Shi, Prof. Helge Bode, Janik Kranz, Peter Grün og Andreas Tietze. Kredit:Jürgen Lecher, Goethe Universitet Mikroorganismer samler ofte naturlige produkter svarende
Byggesæt til specialdesignede produkterFra venstre mod højre:Dr. Yan-Ni Shi, Prof. Helge Bode, Janik Kranz, Peter Grün og Andreas Tietze. Kredit:Jürgen Lecher, Goethe Universitet Mikroorganismer samler ofte naturlige produkter svarende -
 Fælder for energikildemolekyler i cellerKredit:Natalia Deryugina Et team af forskere, inklusive en RUDN-kemiker, har syntetiseret nye molekyler, der tilhører klassen af calixarener, skållignende hule strukturer. Disse stoffer ser ud t
Fælder for energikildemolekyler i cellerKredit:Natalia Deryugina Et team af forskere, inklusive en RUDN-kemiker, har syntetiseret nye molekyler, der tilhører klassen af calixarener, skållignende hule strukturer. Disse stoffer ser ud t -
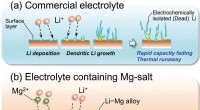 Forskere tager skridt mod sikrere batterier ved at trimme litiumgreneSkematisk illustration af den foreslåede undertrykkende effekt af Li dendritisk vækst ved tilsætning af Mg-salt. Kredit:Royal Society of Chemistry Et samarbejdende team af forskere fra Shinshu Uni
Forskere tager skridt mod sikrere batterier ved at trimme litiumgreneSkematisk illustration af den foreslåede undertrykkende effekt af Li dendritisk vækst ved tilsætning af Mg-salt. Kredit:Royal Society of Chemistry Et samarbejdende team af forskere fra Shinshu Uni
- Etiopien åbner anlæg for at omdanne affald til energi
- At klappe, eller ikke at flappe? Flagrende vinger kan være mere effektivt end faste vinger, viser u…
- Hvad er forskellene mellem trin- og kædepolymerisationsreaktion?
- Godkendelse af hasselnøddernes geografiske oprindelse
- Hvordan går en slug flytte?
- Nyt elektrodemateriale udviklet til at øge opladningskapaciteten af lithium-batterier


