Hvad hvis HCl og Na2SO4 blandes. Er det en farlig reaktion?
1. Syre-Base-reaktion :HCl er en stærk syre, mens Na2SO4 er et salt, der kan undergå hydrolyse i vand. Når HCl tilsættes til vand, dissocieres det til hydrogenioner (H+) og chloridioner (Cl-). H+ ionerne fra HCl reagerer med vandmolekylerne og danner hydroniumioner (H3O+).
2. Danning af hydrerede ioner :Na2SO4 dissocieres til natriumioner (Na+) og sulfationer (SO42-), når de opløses i vand. Sulfationerne forbliver intakte og deltager ikke i nogen væsentlige reaktioner med hydroniumionerne.
3. Neutralisering :Hydroniumionerne (H3O+) fra HCl reagerer med de hydroxidioner (OH-) der er til stede i vand gennem en proces kaldet neutralisering. Denne reaktion producerer vandmolekyler og frigiver varme.
Den overordnede reaktion kan repræsenteres som:
HCl + Na2SO4 + H2O → NaCl + H2SO4 + H2O
De dannede produkter er natriumchlorid (NaCl), svovlsyre (H2SO4) og vand (H2O). Svovlsyre er en stærk syre, men dens koncentration i den resulterende opløsning vil være lav på grund af vandets fortyndingseffekt.
Sammenfattende fører blanding af HCl og Na2SO4 ikke til en farlig reaktion. De vigtigste dannede produkter er NaCl, H2SO4 og vand. Reaktionen er i det væsentlige en syre-base-neutraliseringsproces.
Sidste artikelHvad sker der, hvis oxidatom bliver til et oxygenatom?
Næste artikelHvorfor er C2H4 Ethylen upolær?
 Varme artikler
Varme artikler
-
 Lille volumen, høj-throughput organisk synteseByggestenstilgang til at forberede kompleks ─B(OH) 2 del indeholdende molekyler i stort antal. Kredit:Dömling Lab/Science Advances Universitetet i Groningen professor i lægemiddeldesign, Alexand
Lille volumen, høj-throughput organisk synteseByggestenstilgang til at forberede kompleks ─B(OH) 2 del indeholdende molekyler i stort antal. Kredit:Dömling Lab/Science Advances Universitetet i Groningen professor i lægemiddeldesign, Alexand -
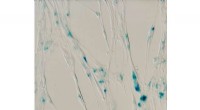 Celler holder op med at dele sig, når dette gen går i højt gear, undersøgelse finderÆldrende celler under et mikroskop. Cellerne - humane lungefibroblaster - blev ældre, efter at de eller nærliggende celler blev gensplejset til at øge aktiviteten af CD36-genet. Områder farvet med b
Celler holder op med at dele sig, når dette gen går i højt gear, undersøgelse finderÆldrende celler under et mikroskop. Cellerne - humane lungefibroblaster - blev ældre, efter at de eller nærliggende celler blev gensplejset til at øge aktiviteten af CD36-genet. Områder farvet med b -
 Ny metode til at måle cellestivhed kan føre til forbedrede kræftbehandlingerI fremtiden, læger kunne bruge den metode, forskerne udviklede, til at spore en patient over tid for at se, hvordan et lægemiddel påvirker patientens kræftceller, senior forfatter Amy Rowat sagde. Kre
Ny metode til at måle cellestivhed kan føre til forbedrede kræftbehandlingerI fremtiden, læger kunne bruge den metode, forskerne udviklede, til at spore en patient over tid for at se, hvordan et lægemiddel påvirker patientens kræftceller, senior forfatter Amy Rowat sagde. Kre -
 Undersøgelsen sigter mod at øge antitumoral aktivitet af forbindelse ekstraheret fra en Amazon-pla…Uncaria guianensis, i flor, Cacuri, Venezuela. CC3.0 Forskere i Brasilien har udarbejdet modificerede former af alkaloiderne produceret af Uncaria guianensis , en træagtig vin, der er hjemmehøre
Undersøgelsen sigter mod at øge antitumoral aktivitet af forbindelse ekstraheret fra en Amazon-pla…Uncaria guianensis, i flor, Cacuri, Venezuela. CC3.0 Forskere i Brasilien har udarbejdet modificerede former af alkaloiderne produceret af Uncaria guianensis , en træagtig vin, der er hjemmehøre
- Kosmisk simulering afslører, hvordan sorte huller vokser og udvikler sig
- Undersøgelse undersøger, hvordan man kan reducere dårlig adfærd på arbejdspladsen
- Ny undersøgelse forklarer oprettelsen af dødbringende firenado i Californien
- 1 død, 100, 000 fordrevet, da tyfonen blæser nær Filippinerne
- Hvordan ved du, hvor en fisk går hen? Forskere adresserer huller i havdyrsporingsdata
- Ingen bevis for, at afhorning af sorte næsehorn påvirker artens reproduktion eller overlevelse neg…


