Hvor mange gram ilt skal der til for at producere 95,6 g aluminiumoxid?
Ud fra den kemiske formel kan vi se, at for hver 2 mol aluminium (Al) er der 3 mol ilt (O).
Først skal vi beregne antallet af mol produceret aluminiumoxid:
Mol af aluminiumoxid =masse / molær masse
Mol aluminiumoxid =95,6 g / 101,96 g/mol
Mol af aluminiumoxid =0,937 mol
Da der er 3 mol ilt for hver 2 mol aluminiumoxid, kan vi beregne de nødvendige mol ilt:
Mol ilt =(3 mol O / 2 mol Al2O3) × mol aluminiumoxid
Mol ilt =(3/2) × 0,937 mol
Mol ilt =1,406 mol
Endelig kan vi omdanne mol oxygen til gram ved hjælp af den molære masse af oxygen (16 g/mol):
Oxygenmasse =mol ilt × molær masse
Oxygenmasse =1,406 mol × 16 g/mol
Oxygenmasse =22,5 g
Derfor skal der cirka 22,5 gram ilt til for at producere 95,6 gram aluminiumoxid.
Sidste artikelHvad forbinder fosfatbindinger med?
Næste artikelHvilke af disse er i halogenfamilien fluor neon lithium eller bismuth?
 Varme artikler
Varme artikler
-
 Undervisning i CRISPR og antibiotikaresistens til gymnasieeleverElever på Evanston Township High School tester BioBits-sæt, udviklet på Northwestern University. Kredit:Claire Barclay Hvordan kan gymnasieelever lære om en teknologi så kompleks og abstrakt som C
Undervisning i CRISPR og antibiotikaresistens til gymnasieeleverElever på Evanston Township High School tester BioBits-sæt, udviklet på Northwestern University. Kredit:Claire Barclay Hvordan kan gymnasieelever lære om en teknologi så kompleks og abstrakt som C -
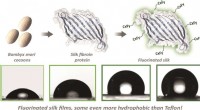 Forskere bruger modificerede silkeproteiner til at skabe nye nonstick-overfladerGrafisk abstrakt. Kredit:ChemBioChem (2022). DOI:10.1002/cbic.202200429 Forskere ved Tufts University har udviklet en metode til at lave silkebaserede materialer, der nægter at holde sig til vand,
Forskere bruger modificerede silkeproteiner til at skabe nye nonstick-overfladerGrafisk abstrakt. Kredit:ChemBioChem (2022). DOI:10.1002/cbic.202200429 Forskere ved Tufts University har udviklet en metode til at lave silkebaserede materialer, der nægter at holde sig til vand, -
 Nikkelkatalysator letter oprettelsen af en enkelt stereoisomer med to kirale centreAlkyl-alkylbindingsdannelse. (A) Katalysatorstyret stereoselektivitet-tidligere arbejde. (B) Katalysatorstyret stereoselektivitet-denne undersøgelse. ee, enantiomert overskud; M, metal; R, substituent
Nikkelkatalysator letter oprettelsen af en enkelt stereoisomer med to kirale centreAlkyl-alkylbindingsdannelse. (A) Katalysatorstyret stereoselektivitet-tidligere arbejde. (B) Katalysatorstyret stereoselektivitet-denne undersøgelse. ee, enantiomert overskud; M, metal; R, substituent -
 Fødevareforskere skaber nye magnetiske nanopartikler til hurtig screening af pesticidrester i grøn…Figur illustrerer processen involveret i at bruge polystyrencoatede magnetiske nanopartikler (mikromagneter) til at udvinde spor af pesticidrester fra vegetabilske prøver. Kredit:Yu Xi Fødevarefor
Fødevareforskere skaber nye magnetiske nanopartikler til hurtig screening af pesticidrester i grøn…Figur illustrerer processen involveret i at bruge polystyrencoatede magnetiske nanopartikler (mikromagneter) til at udvinde spor af pesticidrester fra vegetabilske prøver. Kredit:Yu Xi Fødevarefor
- Små generatorer omdanner spildvarme til strøm
- Undersøgelse af lovende fotovoltaisk materiale fører til opdagelse af en ny stoftilstand
- Costco eller Amazon Prime? Flere shoppere vælger begge dele
- Næsten halvdelen af nye lærere overvejer at forlade inden for 10 år, ifølge ny undersøgelse
- Defekt kulstof forenkler produktionen af brintoverilte
- Forudsige, hvornår onlinesamtaler bliver giftige


