Hvordan holder kemisk energi molekyler sammen?
Der er tre hovedtyper af kemiske bindinger:kovalente bindinger, ionbindinger og hydrogenbindinger. Kovalente bindinger dannes, når to atomer deler elektroner. Ionbindinger dannes, når et atom overfører elektroner til et andet atom. Hydrogenbindinger dannes, når et brintatom, som er bundet til et stærkt elektronegativt atom, danner en svag binding med et andet elektronegativt atom.
Styrken af en kemisk binding afhænger af flere faktorer, herunder elektronegativiteten af de involverede atomer, bindingslængden og bindingsvinklen. Elektronegativitet er et mål for et atoms evne til at tiltrække elektroner. Jo mere elektronegativt et atom, jo stærkere bindinger vil det danne. Bindingslængde er afstanden mellem kernerne i to bundne atomer. Jo kortere bindingslængden er, jo stærkere bindingen. Bindingsvinkel er vinklen mellem to bindinger, der deler et fælles atom. Jo mindre bindingsvinklen er, jo stærkere bindinger.
Kemisk energi er afgørende for livet. Det bruges til at holde molekyler sammen, til at give energi til kemiske reaktioner og til at transportere energi gennem hele kroppen.
Sidste artikelHvorfor deler grundstofferne i gruppe 16 lignende kemiske egenskaber?
Næste artikelHvad er en Chem 13 laboratorietest til?
 Varme artikler
Varme artikler
-
 Nye keramiske nanofiber svampe kan bruges til fleksibel isolering, vandrensningForskere har udviklet et svampelignende materiale fremstillet af keramiske nanofibre. Materialet bevarer den varmebestandighed, der gør keramik nyttig i højtemperaturindstillinger, men er også meget d
Nye keramiske nanofiber svampe kan bruges til fleksibel isolering, vandrensningForskere har udviklet et svampelignende materiale fremstillet af keramiske nanofibre. Materialet bevarer den varmebestandighed, der gør keramik nyttig i højtemperaturindstillinger, men er også meget d -
 Video:Hvordan kemi kan forbedre billige varm kakaoKredit:The American Chemical Society Ingen kan rigtig godt lide billigt varmt kakaopulver. Det er klumpet, den er for tynd, og den efterlader skummel rester bagved. Men blanding af varm kakao er
Video:Hvordan kemi kan forbedre billige varm kakaoKredit:The American Chemical Society Ingen kan rigtig godt lide billigt varmt kakaopulver. Det er klumpet, den er for tynd, og den efterlader skummel rester bagved. Men blanding af varm kakao er -
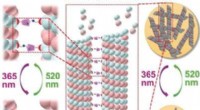 Lysstyret reversibel aggregering af mikrotubuli medieret af paclitaxel-modificeret cyclodextrinKredit:Wiley En kombination af naturlige mikrotubuli og syntetiske makrocykliske receptorer giver mulighed for lyskontrollerede, reversibel aggregering af mikrotubulierne til større nanostrukturer
Lysstyret reversibel aggregering af mikrotubuli medieret af paclitaxel-modificeret cyclodextrinKredit:Wiley En kombination af naturlige mikrotubuli og syntetiske makrocykliske receptorer giver mulighed for lyskontrollerede, reversibel aggregering af mikrotubulierne til større nanostrukturer -
 Forskere udvikler tilgang til vedvarende energi til fremstilling af ammoniakWilliam Schneider. Kredit:University of Notre Dame Forskere ved University of Notre Dame udvikler en tilgang til vedvarende energi til at syntetisere ammoniak, en væsentlig komponent af gødning, d
Forskere udvikler tilgang til vedvarende energi til fremstilling af ammoniakWilliam Schneider. Kredit:University of Notre Dame Forskere ved University of Notre Dame udvikler en tilgang til vedvarende energi til at syntetisere ammoniak, en væsentlig komponent af gødning, d


