Hvad er tendenser blandt grundstofferne for atomstørrelse?
1. Atomradius falder generelt over en periode (række) fra venstre mod højre. Dette skyldes, at antallet af protoner i kernen stiger over en periode, hvilket øger den elektrostatiske tiltrækning mellem den positivt ladede kerne og de negativt ladede elektroner. Som et resultat bliver elektronerne trukket tættere på kernen, hvilket resulterer i et fald i atomradius.
2. Atomradius øges generelt ned ad en gruppe (søjle) fra top til bund. Dette skyldes, at nye elektronskaller tilføjes, efterhånden som du går ned ad en gruppe, og hver ny skal er større end den forrige. De yderste elektroner i atomet er placeret i den yderste skal, og de er de mest løst holdt. Som et resultat oplever de mindre elektrostatisk tiltrækning fra kernen, hvilket giver dem mulighed for at være længere fra kernen. Dette resulterer i en stigning i atomradius.
3. Metallers atomstørrelse er generelt større end ikke-metallers. Dette skyldes, at metaller har en lavere elektronegativitet end ikke-metaller. Elektronegativitet er et mål for et atoms evne til at tiltrække elektroner. Jo mere elektronegativt et atom er, jo mere tiltrækker det elektroner. Metaller har en lavere elektronegativitet end ikke-metaller, så de tiltrækker elektroner mindre stærkt. Som følge heraf holdes valenselektronerne i metaller mere løst og kan lettere fjernes fra atomet. Dette resulterer i en større atomradius for metaller.
4. Atomstørrelsen af ædelgasser er generelt den største i en periode. Det skyldes, at ædelgasser har en fuldstændig yderste elektronskal. En fuldstændig yderste elektronskal betyder, at ædelgassen har en meget lav elektronegativitet og ikke tiltrækker elektroner særlig kraftigt. Som et resultat er valenselektronerne i ædelgasser meget løst holdt og kan let fjernes fra atomet. Dette resulterer i den største atomradius for ædelgasser.
Disse er de generelle tendenser for atomstørrelse blandt grundstofferne. Der er dog nogle undtagelser fra disse tendenser, såsom lanthanid- og actinid-serien.
Sidste artikelHvordan forbereder du HCL-løsning i laboratoriet?
Næste artikelSammenhæng mellem masse og volumen af en væske?
 Varme artikler
Varme artikler
-
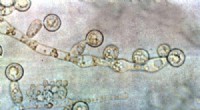 Forskere udvikler unik polymerbelægning til at tackle skadelige svampeCandida albicans. Kredit:Wikipedia. Forskere fra University of Nottingham har udviklet en ny måde at kontrollere skadelige svampe på, uden behov for at bruge kemiske bioaktive stoffer som fungicid
Forskere udvikler unik polymerbelægning til at tackle skadelige svampeCandida albicans. Kredit:Wikipedia. Forskere fra University of Nottingham har udviklet en ny måde at kontrollere skadelige svampe på, uden behov for at bruge kemiske bioaktive stoffer som fungicid -
 Teamet tester virkningerne af ilt på uranVist på en stor computerskærm er et Raman-spektrum af uranoxidpartikler dannet inde i holdets reaktionskammer på bænken. Det viste uranoxidspektrum er for U3 O8 . Kredit:Julie Russell/LLNL Et team
Teamet tester virkningerne af ilt på uranVist på en stor computerskærm er et Raman-spektrum af uranoxidpartikler dannet inde i holdets reaktionskammer på bænken. Det viste uranoxidspektrum er for U3 O8 . Kredit:Julie Russell/LLNL Et team -
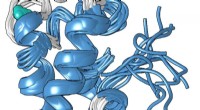 Bakterielt protein kan hjælpe med at finde materialer til din næste smartphoneEn strukturel model af den kompakte metalbundne form af lanmodulinproteinet, som er 100 millioner gange bedre til at binde sig til lanthanider-de sjældne jordartsmetaller, der bruges i smartphones og
Bakterielt protein kan hjælpe med at finde materialer til din næste smartphoneEn strukturel model af den kompakte metalbundne form af lanmodulinproteinet, som er 100 millioner gange bedre til at binde sig til lanthanider-de sjældne jordartsmetaller, der bruges i smartphones og -
 Faststof-elektrolyt med lithium-ion-ledningsevne, der kan sammenlignes med flydende elektrolytterLithiumamid-borhydrid er en lovende kandidat til en fast elektrolyt. Den krystallinske struktur af dette materiale består af to undergitre, vist i forskellige farver. Under passende forhold, lithium i
Faststof-elektrolyt med lithium-ion-ledningsevne, der kan sammenlignes med flydende elektrolytterLithiumamid-borhydrid er en lovende kandidat til en fast elektrolyt. Den krystallinske struktur af dette materiale består af to undergitre, vist i forskellige farver. Under passende forhold, lithium i
- Vilde gener hos husdyr:Hvordan vi kan overlade vores afgrøder ved hjælp af deres fjerne slægtning…
- Hvem har det bedre, og hvem har det værst fire år efter udbruddet af COVID? Det økonomiske billed…
- De fleste byer i delstaten São Paulo har lav potentiel kapacitet til at tilpasse sig klimaændringe…
- Nanosvamp lægemiddelleveringssystem mere effektivt end direkte injektion
- NASA siger farvel til Earth Observing-1 (EO-1) satellit efter 17 år
- Fem ting at vide om Grønland


