Hvad måler en opløsnings evne til at neutralisere syre?
1. pH-værdi:
- pH er et mål for surhedsgraden eller basiciteten af en opløsning på en skala fra 0 til 14, hvor 0 er stærkt surt, 7 er neutralt og 14 er stærkt basisk.
- En opløsning med en pH større end 7 betragtes som basisk og kan neutralisere syrer.
2. Alkalinitet:
- Alkalinitet refererer til en opløsnings evne til at neutralisere syrer. Det udtrykkes i form af mængden af syre, der kræves for at bringe opløsningens pH til et specificeret niveau, normalt pH 7.
- Alkalinitet måles almindeligvis ved titrering med en stærk syre, såsom saltsyre (HCl), indtil endepunktet er nået (pH 7).
3. Basiskoncentration:
- Koncentrationen af hydroxidioner (OH-) i en opløsning bestemmer dens basicitet.
- Jo højere koncentrationen af OH- ioner er, jo stærkere er basen og jo større er dens evne til at neutralisere syrer.
- Basekoncentrationen kan måles ved hjælp af forskellige metoder, såsom titrering eller ion-selektive elektroder.
4. Syre-base titrering:
- Syre-basetitrering involverer gradvis tilsætning af en kendt koncentration af syre til en opløsning af base, indtil ækvivalenspunktet er nået, hvor de tilsatte mol syre er støkiometrisk ækvivalente med de tilstedeværende mol base.
- Mængden af syre, der kræves for at nå ækvivalenspunktet, angiver opløsningens basicitet eller neutraliserende kapacitet.
Det er vigtigt at bemærke, at forskellige syrer og baser kan have varierende styrker, så det er nødvendigt at overveje den specifikke syre og base, der er involveret, når neutraliseringskapaciteten af en opløsning bestemmes.
Sidste artikelHvad sker der, når man blander sukker og vand?
Næste artikelHvad er antallet af neutroner i atom I131?
 Varme artikler
Varme artikler
-
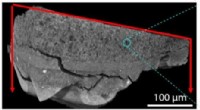 Forskere udforsker gammel maling i mikroskopiske detaljer for at informere bevaringsindsatsenEn røntgenmikrotomografiskanning af en malingsprøve (til venstre) viser en tilfældig fordeling af komponenter i en malingsprøve, og en zoomet visning ved hjælp af en teknik kendt som fototermisk induc
Forskere udforsker gammel maling i mikroskopiske detaljer for at informere bevaringsindsatsenEn røntgenmikrotomografiskanning af en malingsprøve (til venstre) viser en tilfældig fordeling af komponenter i en malingsprøve, og en zoomet visning ved hjælp af en teknik kendt som fototermisk induc -
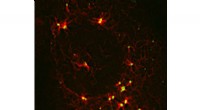 Kaster lys på en skyggefuld organisatorisk hub i cellerEt stort protein koordinerer cellulære komponenter, der kræves til mikrotubulussamling. Kredit:James Goldenring, Vanderbilt Universitet På cellulært niveau, vi hænger alle sammen med sarte tråde.
Kaster lys på en skyggefuld organisatorisk hub i cellerEt stort protein koordinerer cellulære komponenter, der kræves til mikrotubulussamling. Kredit:James Goldenring, Vanderbilt Universitet På cellulært niveau, vi hænger alle sammen med sarte tråde. -
 Forskere skaber fermenteret juice og funktionelt brød til behandling af anæmiKredit:South Ural State University (SUSU) Et team af russiske forskere fra South Ural State University og deres egyptiske kolleger fremstiller sunde funktionelle fødevarer. Brød og drikkevarer rig
Forskere skaber fermenteret juice og funktionelt brød til behandling af anæmiKredit:South Ural State University (SUSU) Et team af russiske forskere fra South Ural State University og deres egyptiske kolleger fremstiller sunde funktionelle fødevarer. Brød og drikkevarer rig -
 Ny teknik bruger skabeloner til at guide selvfoldende 3D-strukturerForskere fra NC State University har udviklet en ny teknik til at kontrollere selvfoldende tredimensionelle (3D) strukturer. Specifikt, forskerne bruger skabeloner til at begrænse deformation i visse
Ny teknik bruger skabeloner til at guide selvfoldende 3D-strukturerForskere fra NC State University har udviklet en ny teknik til at kontrollere selvfoldende tredimensionelle (3D) strukturer. Specifikt, forskerne bruger skabeloner til at begrænse deformation i visse
- Tør Ice Vs. Flydende kvælstof
- Ny synergistisk enkeltatom-katalysatortilgang bryder forgængernes aktivitetsbegrænsning
- Muon -detektor vigtig for billeddannelse og overvågning af kuldioxidlagringssteder
- Ny rekord om presning af lys til ét atom:Atomic Lego guider lys under et nanometer
- Lyft, bildelsproducent Magna partner på autonome køretøjer
- Forvent færre, men mere destruktive landfaldende tropiske cykloner


